.
|
Un nouveau-nť boit
quotidiennement un volume de lait notť V ťgal ŗ 700 mL. La
concentration molaire de la carnitine dans le lait C est ťgale ŗ 8,0 x
10-5 mol.L-1.
Montrer
que la quantitť de matiŤre n de carnitine absorbťe par le nourrisson
quotidiennement est ťgale ŗ 5,6 x 10-5 mol.
n = CV = 0,700 *8,0 10-5 =5,6 10-5 mol.
Dťterminer
la masse de carnitine absorbťe par le nouveau-nť.
Donnťe : Masse molaire de la carnitine : M = 161 g.mol-1.
m = n M = 5,6 10-5*161 =9,0 10-3 g = 9,0 mg.
Cette masse est trŤs faible, quelques milligrammes. Peut-on pour autant
se passer de cette espŤce chimique ? Justifier la rťponse.
Non, cette espŤce est indispensable : elle
contribue au transport des acides gras ŗ l’intťrieur de la mitochondrie.
Dans
le texte introductif, il est mentionnť que la carnitine contribue au
transport des acides gras vers les mitochondries oý ils sont oxydťs.
Lors
d’une oxydation, il y a : Indiquer la ou les
bonne(s) rťponse(s).
a)
gain d’ťlectrons. Faux.
b) perte d’ťlectrons. Vrai.
c) gain de protons H+.Faux. d) perte de protons H+.
Faux.
Le lait maternel peut Ítre
remplacť par des laits maternisťs en poudre auxquels on ajoute une eau
minťrale adaptťe.
L’ťtiquette de cette eau minťrale est reprťsentťe ci-dessous. On se
propose dans cet exercice de vťrifier expťrimentalement sa teneur en
ions hydrogťnocarbonate HCO3-. L’ion
hydrogťnocarbonate est la base du couple acide/base (CO2, H2O)
/ HCO3-.
Dťfinir une base
selon BrŲnsted.
Une base est une espŤce, ion ou molťcule, susceptible de gagner un
proton H+.
Le pKa du couple (CO2,
H2O) / HCO3-
est ťgal ŗ 6,3.
Tracer
le diagramme de prťdominance des espŤces.
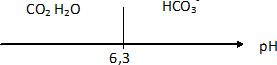
Le pH de l'eau est ťgal ŗ 7,2.
Quelle
est l'espŤce chimique prťdominante ? Justifier.
A pH supťrieur au pKa, la forme HCO3-
prťdomine.
On dose un volume Vb=50,0 mL d'eau minťrale par une solution
d'acide chlorhydrique de concentration Ca = 2,0 10-2
mol/L.
Choisir
le bon dispositif de dosage.
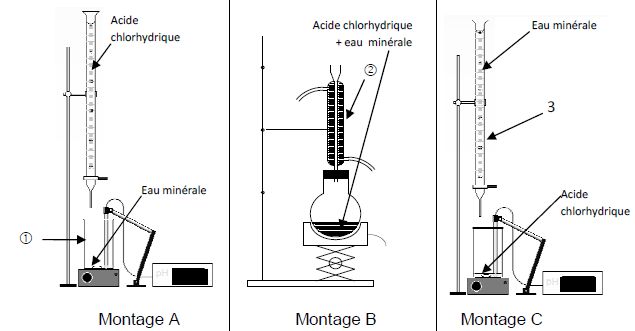
Le montage A est correct, l'espŤce ŗ doser est dans le becher, la
solution titrante est dans la burette graduťe.
Nommer
les ťlťments 1, 2 et 3.
1 : becher ; 2 : rťfrigťrant ŗ eau ; 3 : burette graduťe.
Dťterminer
graphiquement le point ťquivalent notť E.
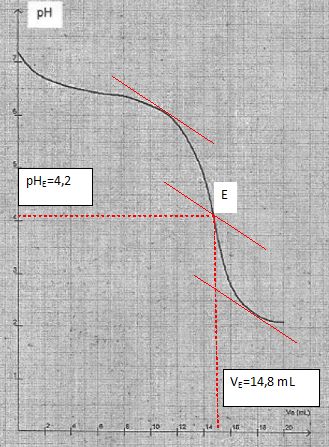
|
La
rťaction support du titrage est HCO3- + H3O+
---> CO2 + 2H2O.
Dťfinir
l’ťquivalence.
A l'ťquivalence les quantitťs de matiŤre des rťactifs sont en
proportions stoechiomťtriques. Avant l'ťquivalence, l'un des rťactifs
est en excŤs, aprŤs l'ťquivalence, l'autre rťactif est en excŤs.
Donner
la relation entre la quantitť de matiŤre nb d'ion
hydrogťnocarbonate dosť et la quantitť de matiŤre naE d'ion oxonium
apportťe ŗ l'ťquivalence.
nb
=naE.
A
l'ťquivalence Ca VaE = CbVb
et on admet que VaE = 14,6 mL.
Vťrifier
que Cb = 5,8 10-3 mol/L.
Cb
= Ca
VaE /Vb
=2,0 10-2*14,6 / 50,0 = 5,8 10-3 mol/L.
Calculer
la concentration massique en ion hydrogťnocarbonate. M(HCO3-)
= 61 g/mol.
mmassique = Cb
M(HCO3-) = 5,8
10-3*61
=0,356 ~0,36 g/L ou 3,6 102 mg/L.
Cette valeur est en accord avec les indications de l'ťtiquette ( 360
mg/L ).
|
|