|
|
| L'ibuprofŤne est une molťcule de formule brute C13H18O2.
Son nom en nomenclature officielle est acide
2-(4-isobutylphťnyl)propanoÔque. De part ses propriťtťs
anti-inflammatoire, antalgique et antipyrťtique, elle constitue le
principe actif de divers mťdicaments. | 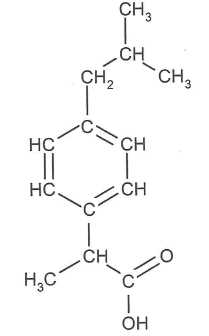 |
La molťcule d'ibuprofŤne.
Entourer le groupe caractťristique associť ŗ la fonction acide carboxylique.
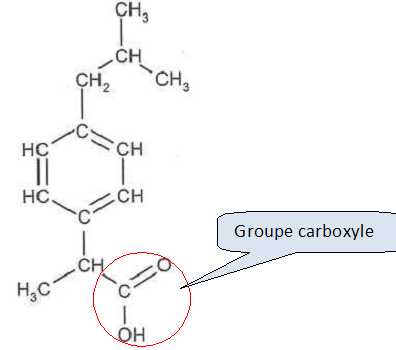
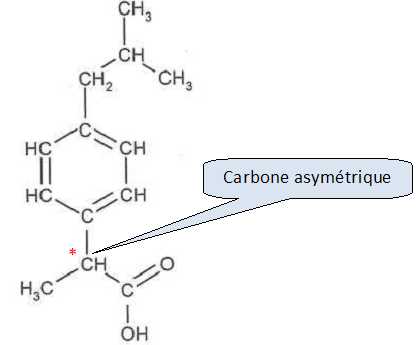
La molťcule d'ibuprofŤne est chirale. Expliquer la cause de cette chilaritť en la nommant et en la repťrant.
Cette
molťcule possŤde un atome de carbone asymťtrique, c'est ŗ dire un atome
de carbone tťtragonal liť ŗ 4 atomes ou groupes d'atomes diffťrents.
Une molťcule possťdant un atome de carbone asymťtrique est chirale.
Cette chiralitť entraÓne l'existence de deux ťnantiomŤres de l'ibuprofŤne. Comment reconnaÓtre si deux molťcules sont ťnantiomŤres ? ( aucun schťma n'est atendu ).
Une
molťcule chirale n'est pas superposable ŗ son image dans un miroir. La
molťcule et son image dans un miroir constitue un couple d'ťnantiomŤres.
Deux ťnantiomŤres sont 2 isomŤres de configuration, images l'un de l'autre dans un miroir.
Deux ťnantiomŤres ne diffťrent que par leur propriťtťs optiques; ils sont
sťparables.
Complťter la reprťsentation de Cram suivante et schťmatiser le deuxiŤme ťnantiomŤre.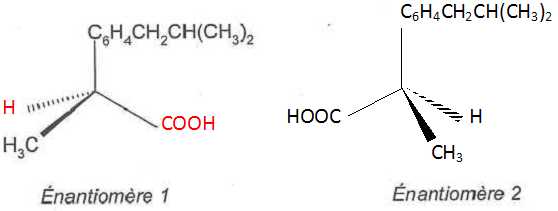 . .
Divers
techniques d'analyse ont permis de connaÓtre la structure de la
molťcule d'ibuprofŤne. Les spectroscopies IR et RMN en sont deux
exemples.
|
.
|
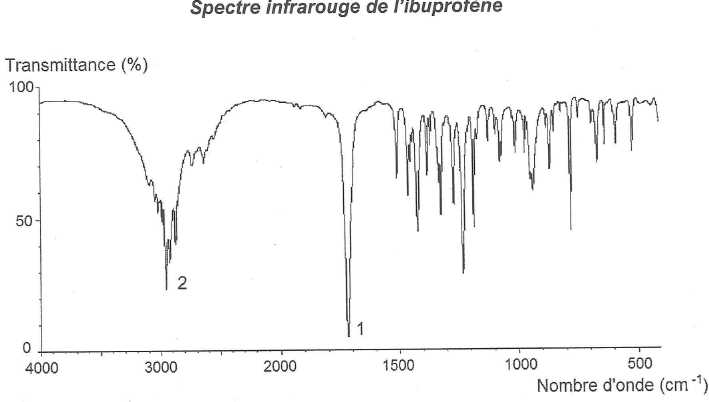
Donner l'origine des bandes d'absorption 1 et 2 du spectre IR.
(1) bande fine et forte vers 1720 cm-1due au groupe C=O de la fonction acide carboxylique.
(2) bande large multipe vers 3000 cm-1 due au liaison C-H et ŗ la liaison O-H associťe par liaisons hydrogŤne.
|
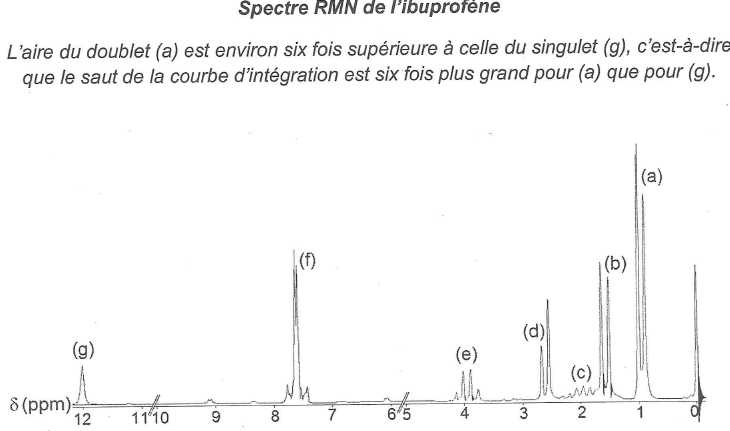
Sur
la formule semi-dťveloppťe de l'ibuprofŤne, entourer la ou les atomes
d'hydrogŤne associťs au signal (g) du spectre RMN. Justifier. Expliquer
pourquoi (g) est un singulet. MÍmes questions pour le signal (a). (g) : singulet : ce proton n'est couplť avec aucun autre proton, il n'y a donc aucun "proton proche voisin".
L'aire
du doublet (a) est environ 6 fois plus grande que l'aire du pic (g) :
le signal (g) correspond sans doute ŗ un seul proton. Enfin le
dťplacement chimique proche de 12 ppm fait penser au proton d'un acide
carboxylique.
(a) : doublet : ces protons ťquivalents sont couplťs
avec un seul autre proton ( un seul proton "proche voisin"). L'aire du
doublet laisse penser ŗ 6 protons. Enfin le dťplacement chimique proche
de 1 ppm est compatible avec deux groupes mťthyle CH3. | 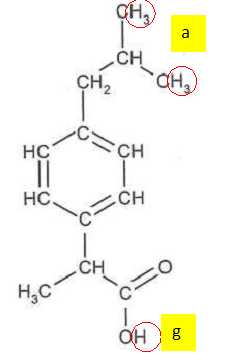 |
|
|