|
Electrolyse : traitement d'effluents : concours technicien supťrieur de l'industrie et des mines 2011. |
||||||
|
||||||
|
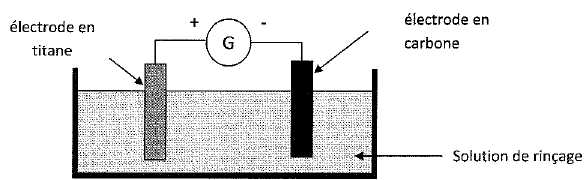
On s'intťresse ŗ une technique ťlectrochimique qui vise ŗ respecter la teneur officielle en cuivre dissous dans les effluents qui rťsultent des opťrations de rinÁage. Le second rinÁage s'effectue en circuit fermť. Les eaux de rinÁage sont envoyťes sur des cellules d'ťlectrodťposition fonctionnant en continu, qui permettent de rťutiliser ces eaux. La cuve d'ťlectrodťposition contient une ťlectrode en titane et une ťlectrode en carbone. Ces deux ťlectrodes sont immergťes dans la solution de rinÁage et sont alimentťes par un gťnťrateur de courant continu.
n(e-) = 2 nCu =2*4,110 = 8,220 ~8,2 mol. Exprimer la quantitť d'ťlectricitť Q utilisťe par la cellule durant l'opťration. Q = n(e-) F ave F le faraday ( 96500 C). Exprimer puis calculer l'intensitť du courant I supposťe constante. Q = I Dt ; I = n(e-) F / Dt = 8,220 *96500 /(6*3600) =3,67 ~3,7 A.
IntťrÍt du procťdť. Dans l'installation industrielle, deux appareils montťs en parallŤle sur le circuit des eaux de rinÁage assurent cette fonction d'ťlimination des ions Cu2+. Cela permet, par un dispositif annexe contenant un jeu d'ťlectrodes supplťmentaire, de rťcupťrer le dťpŰt de cuivre solide tout en permettant ŗ l'unitť de traitement de fonctionner sans interruption. Une mťthode plus classique consiste ŗ prťcipiter les ions Cu2+aq prťsents dans les eaux de rinÁage sous forme d'hydroxyde de cuivre (II), par ajout d'une solution d'hydroxyde de sodium ( Na+aq + HO-aq). La rťaction est alors : Cu2+aq + 2 HO-aq= Cu(OH)2(s). Calculer la masse de prťcipitť d'hydroxyde de cuivre obtenu lors de la prťcipitation de 4,11 mol d'ion cuivre (II) et la comparer avec la masse de cuivre obtenue prťcťdemment. Il se forme = 4,11 mol d'hydroxyde de cuivre (II) ; M(Cu(OH)2) = 63,5 +2*17 =97,5 g/mol. m = 4,11 *97,5 ~401 g, environ 1,5 fois la masse de cuivre dťposťe ŗ la cathode. Ce rťsultat nous permet d'ťtablir une comparaison des deux procťdťs ( ťlectrodťposition et prťcipitation ) sur la base des produits obtenus dans chaque cas. Quel est le produit obtenu qu'il faudra extraire des eaux de rinÁage, puis traiter chimiquement pour le recycler ? Il faut exttraire l'hydroxyde de cuivre (II) solide par filtration. Lequel des deux procťdťs donne un produit directement utilisable ? L'ťlectrodťposition donne du cuivre mťtallique directement utilisable.
|
||||||
|
|