|
.
|
|
Gťnťralitťs sur la chromatographie.
Rappelez le principe de toute mťthode chromatographique.
La chromatographie est une
mťthode de sťparation et d'identification des
constituants d'un mťlange.
La chromatographie est basťe
sur la diffťrence de solubilitť d'une
substance dans deux phases non miscibles:la phase
stationnaire liťe au support et la phase mobile ou
solvant.
Plus une substance est soluble dans
la phase mobile, plus elle est entraÓnťe par
cette phase; inversement, une substance peu soluble dans la
phase mobile migre peu.
Un fluide appelť phase
mobile parcourt un tube appelť colonne. Cette colonne
peut contenir des "granulťs" poreux (colonne remplie)
ou Ítre recouverte ŗ l'intťrieur d'un
film mince (colonne capillaire). Dans les deux cas, la
colonne est appelťe phase stationnaire.
A l'instant initial, le
mťlange ŗ sťparer est injectť
ŗ l'entrťe de la colonne oý il se dilue
dans la phase mobile qui l'entraÓne ŗ travers
la colonne. Si la phase stationnaire a ťtť
bien choisie, les constituants du mťlange,
appelťs gťnťralement les
solutťs, sont inťgalement retenus lors de la
traversťe de la colonne.
De ce phťnomŤne
appelť rťtention il rťsulte que les
constituants du mťlange injectť se
dťplacent tous moins vite que la phase mobile et que
leurs vitesses de dťplacement sont
diffťrentes. Ils sont ainsi ťluťs de la
colonne les uns aprŤs les autres et donc sťparťs.
Un dťtecteur placť
ŗ la sortie de la colonne couplť ŗ un
enregistreur permet d'obtenir un tracť appelť
chromatogramme. En effet, il dirige sur un enregistreur un
signal constant appelť ligne de base en
prťsence du fluide porteur seul ; au passage
de chaque solutť
sťparť il conduit dans le temps ŗ
l'enregistrement d'un pic.
Dans des conditions
chromatographiques donnťes, le "temps de
rťtention" (temps au bout duquel un composť
est ťluť de la colonne et
dťtectť), caractťrise qualitativement
une substance. L'amplitude de ces pics, ou encore l'aire
limitťe par ces pics et la prolongation de la ligne
de base permet de mesurer la concentration de chaque
solutť dans le mťlange
injectť.
C'est en jouant sur la nature de
l'ťluant (et dans une moindre mesure sur la nature du
support) que l'on parvient ŗ sťparer les
constituants d'un mťlange.
Quels sont les phťnomŤnes mis en jeu dans le cas d’une chromatographie d’adsorption ? De partage ?
La chromatographie de
partage :
Elle est basťe sur la diffťrence de solubilitť du solutť dans la phase mobile et la phase stationnaire
C'est une chromatographie
liquide-liquide. La phase stationnaire est un liquide
fixť sur un support inerte. Cette chromatographie est
ainsi dťnommťe car elle est basťe sur
le partage du solutť dans les deux phases liquides ( Chromatographie
d'adsorption :
C'est une chromatographie
liquide-solide. La phase stationnaire est un adsorbant
solide polaire.
- La chromatographie d'adsorption
en phase inverse :
C'est une chromatographie
liquide-solide dans laquelle la phase stationnaire est
apolaire.
Citez un exemple de phase stationnaire utilisťe en chromatographie d’adsorption et en chromatographie de partage.
La phase stationnaire est un solide ŗ grand pouvoir d'adsorption
: oxyde d'aluminium, les silicates de magnťsium, les gels de silice.
Chromatographie
de partage liquide liquide : la phase stationnaire est trŤs fine couche
de liquide adsorbť sur un solide inerte. Groupements silanols polaires
( phase normale ) ou greffons akyles apolaires ayant de 8 ŗ
18 atomes de carbone ( phase inverse ).
|
Analyse de conservateurs prťsents dans un produit cosmťtique.
On cherche ŗ analyser par chromatographie en phase liquide ou HPLC trois conservateurs :
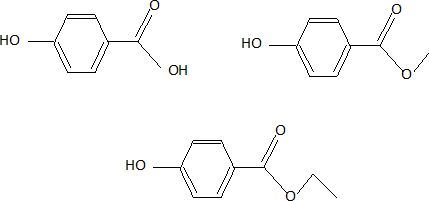
- l’acide para-hydroxybenzoÔque ; - le para-hydroxybenzoate de mťthyle - le para-hydroxybenzoate d’ťthyle.
Les conditions d’analyse retenues sont les suivantes :
- colonne C18, 4x125 mm ; - ťluant : mťlange 70% A et 30% B avec : - A = H2O, 0.1 % d’acide trifluoroacťtique B = acťtonitrile,
- dťbit phase mobile 1 mL/min ; - dťtecteur UV-visible 254 nm - boucle d’injection 10 mL.
Donnez les formules semi-dťveloppťes de ces trois composťs.
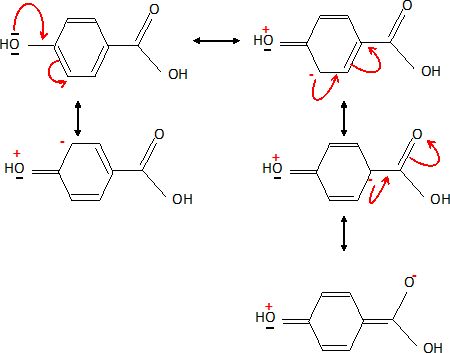
Donnez les formes mťsomŤres de l’acide para-hydroxybenzoÔque.
Que signifie le terme C18 de la phase stationnaire ?
les groupes alkyles greffťs sur la phase stationnaire comptent 18 atomes de carbone.
Quel est le rŰle de l’acide prťsent dans la phase mobile ?
En milieu basique, le phťnol se trouverait sous la forme d'ion
phťnolate, l'acide carboxilique serait en partie sous forme d'ion
carboxylate et les esters pourraient Ítre en partie saponifiťs.
Le milieu acide ťvite ces rťactions.
Prťvoir en le justifiant l’ordre d’ťlution de ces composťs. Quel type d’interaction assure leur sťparation ?
La phase stationnaire est apolaire ; la phase mobile est polaire : les espŤces les plus polaires migrent le plus vite.
Dans l'ordre, du plus rapide au moins rapide : acide
parahydroxybenzoÔque, parahydroxybenzoate de mťthyle,
parahydroxybenzoate d'ťthyle.
Interaction ťlectrostatique dipŰle dipole, liaisons hydrogŤne.
Les temps de rťtention obtenus sont trop longs : comment modifier l’ťluant pour diminuer ces temps de rťtention ?
Modifier la polaritť de l'ťluant.
HPLC : ťlution graduťe :
sur une colonne apolaire, en utilisant une phase
mobile eau/mťthanol, les composants les plus hydrophobes sont ťluťs avec une
concentration ťlevťe en mťthanol alors que les composants plus hydrophiles sont
ťluťs prťfťrentiellement avec une concentration faible en mťthanol.
Vous souhaitez dans les conditions dťcrites prťcťdemment quantifier ces trois conservateurs dans un shampooing :
– en quoi les conditions chromatographiques dťcrites permettent-elles d’envisager d’effectuer un ťtalonnage externe ?
On injecte successivement un volume V constant d’une solution ťtalon (concentration en ťlťment ŗ doser connue Cref) et la solution ŗ doser (concentration inconnue Ci). Comparer les chromatogrammes pour en dťduire la concentration.
Crťf = k Arťf ; Ci = k Ai ; Ci =Crťf Ai / Arťf avec A : aire du pic.
Le spectre IR du para-hydroxybenzoate de mťthyle est reprťsentť ci-dessous ; retrouvez les bandes caractťristiques de cette molťcule.
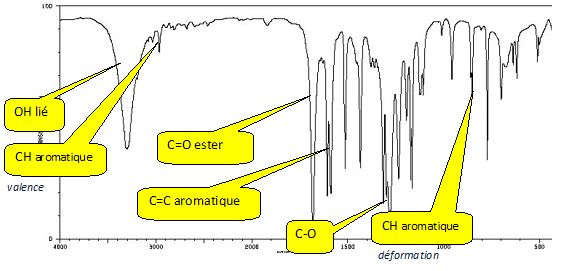
Pourquoi la bande ŗ environ 3400 cm-1 est-elle large ?
Groupe O-H ( phťnol) associassions par liaison hydrogŤne.
Le spectre RMN 1H du para-hydroxybenzoate de mťthyle est reprťsentť ci-dessous, l’intťgration est prťcisťe en dessous de chaque signal.
Attribuez les diffťrents signaux, en prťcisant pour chacun d’eux le dťplacement chimique, la multiplicitť et l’intťgration.
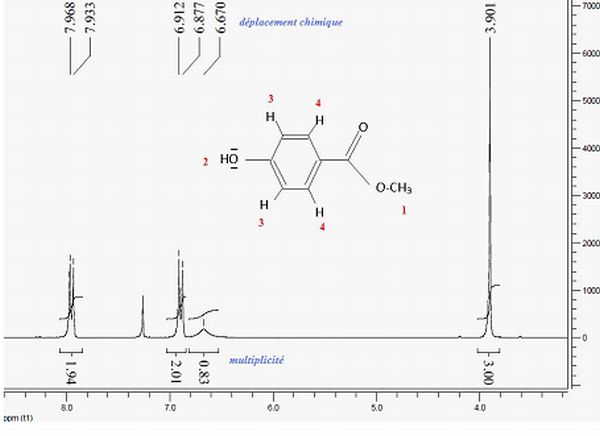
1 : trois protons, d = 3,9 ppm, aucun proche voisin, donc singulet.
2 : 1 proton, d = 6,67 ppm, aucun proche voisin, donc singulet.
3 : deux protons, d = 6,9 ppm, un proche voisin, donc doublet.
4 : deux protons, d = 7,9 ppm, un proche voisin, donc doublet.
|
On
rťalise une analyse par spectromťtrie de masse (impact ťlectronique) du
parahydroxybenzoate de mťthyle. Le spectre obtenu est reprťsentť
ci-dessous.
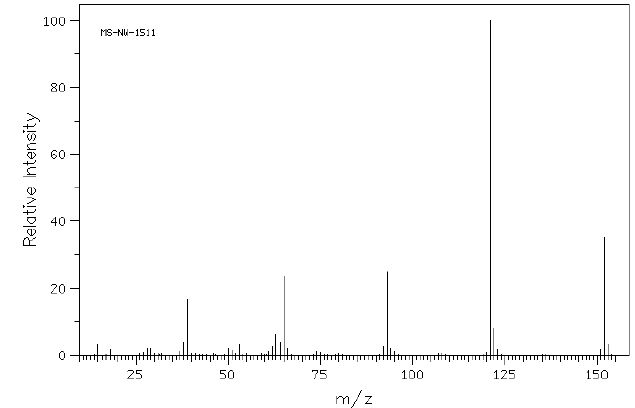
Que signifie le rapport m/z ? Rapport masse sur charge.
Quel est le pic molťculaire ? Pic ŗ m/z =152.
Quel est le pic le plus abondant ? Proposez une structure pour ce fragment.
Pic ŗ m/z = 121.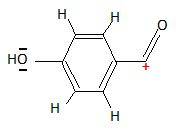
|
|





