.
|
|
Aspect
stťrťochimique.
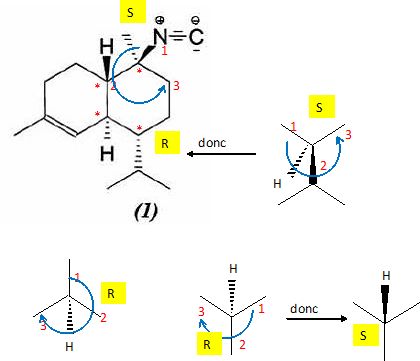
Repťrer
par un
astťrisque les carbones asymťtriques du composť 1. Combien
d'isomŤres de configuration de configuration possŤde ce composť. Donner
la configuration absolue de chaque carbone asymťtrique.
4 atomes de carbone asymťtrique, donc au maximum 24
=16 isomŤres. Deux de ces atomes de carbone asymťtrique appartiennent
aux deux cycles, il y aura donc moins de 16 isomŤres. Certaines
conformations sont bloquťes pour ťviter de trop fortes tensions.
Que
signifie le symbole (+) dans(+)-10-isocyanato-4-cadinŤne ?
Une molťcule dextrogyre a la propriťtť de faire
dťvier le plan de polarisation de la lumiŤre polarisťe vers la droite
d'un observateur qui reÁoit la lumiŤre. Une molťcule dextrogyre est
notťe avec un (+) devant sa nomenclature. Le pouvoir rotatoire, dťterminť
expťrimentalement, est positif.
Formation
du composť 5.
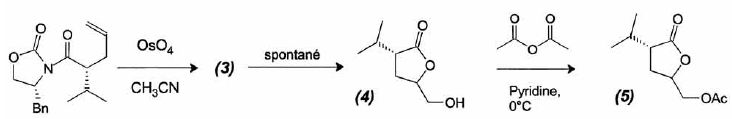
Ac dťsigne le groupe acťthyle et Bn le groupe benzyle.
Donner
la formule topologique de (3). Quelle(s)
fonction(s) possŤde le composť (4) ?
cis hydroxylation viccinale d'une olťfine par OsO4.
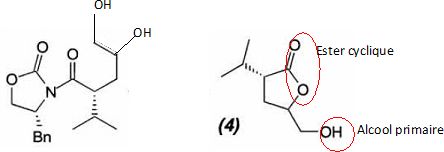
Un ester cyclique est encore appelť lactone.
|
Formation du
composť 10.
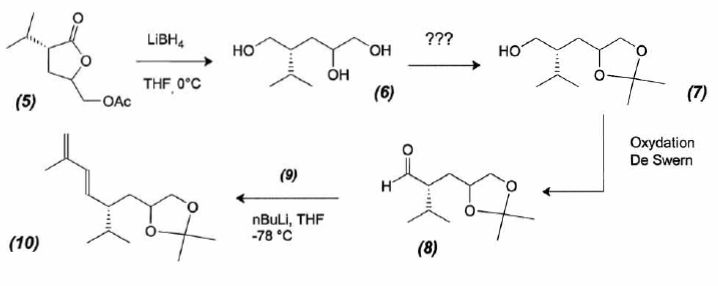
Quel type de
rťaction rťalise t-on avec LiBH4 ?
On rťalise des rťductions :
aldehyde, cťtone, ester, chlorure d'acyle sont rťduits en alcool ; les
lactones conduisent ŗ des diols.
Proposer
un rťactif et des conditions opťratoires pour raliser la transformetion
(6) ---> (7). Quel est le nom donnť ŗ cette rťaction ? Proposer un
mťcanisme rťactionnel.
Le diol est protťgť par la formation
d’un acťtal cylique en utilisant la propanone en prťsence d'un
catalyseur ( acide paratoluŤnesulfonique).
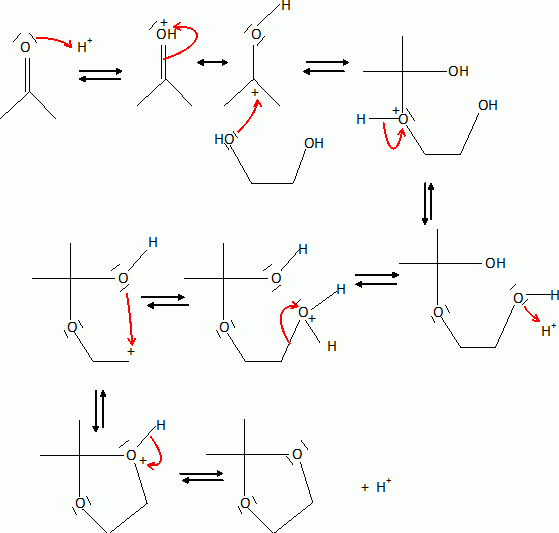
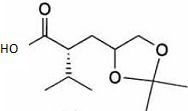
Le composť (7) est oxydť dans des
conditions douces ( Swern ) pour donner l'aldehyde (8).
Donner la formule
topologique du produit que l'on obtiendrait si on utilisait un oxydant
fort ( K2Cr2O7 par exemple ).
De plus en milieu acide, on risque d'hydrolyser l'acťtal cyclique.
Le rťactif (9) est prťparť par action du phosphite de triťthyle ( P(OEt)3)
sur le 3-chloro-2-mťthylprop-1-Ťne.
A l'aide du schťma
de Lewis de P(OEt)3, justifier la
nuclťophilie du phosphite de triťthyle. En dťduire la formule
topologique du cation (9).
Gr‚ce au
doublet libre prťsent sur l'atome de phosphore, le phosphite de triťthyle est un
composť trŤs nuclťophile.
Le phosphite de triťthyle
et un halogťnure d’alkyle rťagissent selon un mťcanisme de substitution
nuclťophile SN2.
L'action du buthyllithium sur (9) donne un composť (9'). Rťaction
d'Arbuzov.

A
quelle rťaction classique, le passage de (8) ŗ (10) peut-il
s'apparenter ?
Rťaction
de Wittig : action d'un ylure de phosphore sur un dťrivť carbonylť.
Cette
rťaction nťcessite un chauffage ŗ reflux assez long ( 9 jours ).
Quel est le rŰle
d'un chauffage ŗ reflux ? Faire un schťma soignť et annotť du chauffage
ŗ reflux.
Le chauffage ŗ reflux permet d'accťlťrer une rťaction lente en
travaillant ŗ tempťrature modťrťe, tout en ťvitant les pertes de
matiŤre. Les vapeurs
se condensent dans le rťfrigťrant ŗ eau et retombent dans le milieu
rťactionnel.
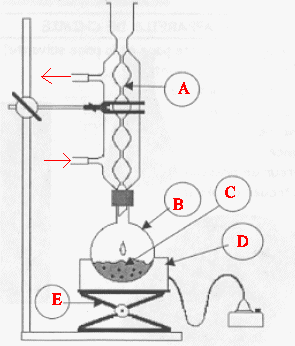
A : rťfrigťrant ŗ eau ; B :
ballon ; C : milieu rťactionnel ; D : chauffe ballon ; E : ťlťvateur ŗ
croisillons.
Dťterminer
la configuration de la double liaison C=C non terminale du composť (10).
Configuration (E).
La rťaction ne forme que ce stťrťoisomŤre de (10). Comment
qualifie-t-on une telle rťaction ?
Rťaction stťrťospťcifique.
|
|







