|
Le dioxygŤne et la vie marine : concours Capes 2012. |
||||||
|
||||||
|
2H3O++2e- = H2(g) + 2H2O ; 3H2O =ĹO2(g) +2H3O++2e-. Donner pour chaque couple de l'eau, le potentiel d'ťlectrode. E1 =Eį(H3O+/ H2(g)) +0,03 log ([H3O+]2 / PH2) ; E1 = -0,06 pH -0,03 log PH2 = E1 = -0,06 pH si PH2= 1 bar. E2 =Eį(O2(g)/ H2O) +0,03 log ( [H3O+]2 PĹO2) ; E2 = 1,26-0,06 pH +0,03 log PĹO2 E2 = 1,26-0,06 pH si PO2= 1 bar. Placer les deux droites frontiŤres sur le diagramme prťcťdent et discuter de la stabilitť des espŤces du manganŤse dans l'eau en fonction du pH. 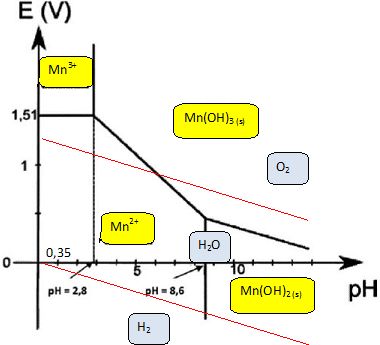 Mn2+, Mn(OH)2 appartiennent au domaine de stabilitť de l'eau : ces deux espŤces sont stables en solution aqueuses. A pH < 6, Mn3+, Mn(OH)3 ne font pas partie du domaine de stabilitť de l'eau : ces deux espŤces sont instables en solution aqueuses. A pH > 6, Mn(OH)3 appartient au domaine de stabilitť de l'eau : cette espŤce est stable.
Dosage du dioxygŤne dissous par la mťthode de Winkler. On recueille V0 = 50,0 mL d'eau de mer dans un flacon presque rempli ŗ ras bord. On ajoute rapidement 0,5 mL du rťactif 1 ( solution de chlorure de manganŤse II de concentration molaire environ 3 mol/L ) et 0,5 mL du rťactif 2 ( solution d'iodure de potassium de concentration molaire environ 3 mol/L et d'hydroxyde de sodium de concentration molaire environ 8 mol/L ). On constate rapidement la formation d'un prťcipitť blanc. Le mťlange est agitť pendant 3 heures. Un prťcipitť brun est alors prťsent dans le flacon. AprŤs ce dťlai, le flacon est rapidement dťbouchť et l'ťchantillon est acidifiť aux environ de pH =1,5 par addition d'acide sulfurique ŗ 10 mol/L. On constate ladisparition rapide du prťcipitť et l'apparition d'une belle couleur orangťe. Les rťactifs 1 et 2 sont trŤs concentrťs, ce qui permet d'affirmer qu'ils sont en trŤs large excŤs. La totalitť de la solution est titrťe par une solution de thiosulfate de sodium ( 2Na+, S2O32-) de concentration molaire C1 = 5,0 10-3 mol/L. Ecrire l'ťquation de la rťaction de formation du prťcipitť blanc. Mn2+aq + 2HO-aq = Mn(OH)2 (s). Ce prťcipitť est-il stable en prťsence de dioxygŤne ? Justifier ŗ l'aide du diagramme E-pH. Mn(OH)2 (s) et O2 appartiennent ŗ des domaines distincts : Mn(OH)2 (s) n'est pas stable en prťsence de O2. Ecrire l'ťquation de la rťaction correspondant ŗ la formation du prťcipitť brun. Justifier que cette transformation soit lente. 2Mn(OH)2 (s) + ĹO2 aq + H2O(l) = 2Mn(OH)3 (s). (0) " Le mťlange est agitť pendant 3 heures. Un prťcipitť brun est alors prťsent dans le flacon" : la transformation est donc lente. Lors de l'ajout d'acide sulfurique, le prťcipitť brun disparaÓt. Ecrire l'ťquation de la rťaction de dissolution de ce prťcipitť. Mn(OH)3 (s) + 3H3O+aq = Mn3+aq + 6H2O(l). (1) Donner l'ťquation de la rťaction simultanťe de formation du diiode. Mn3+aq +e- =Mn2+aq ; DrGį1 = - F Eį(Mn3+aq /Mn2+aq ) =-96500*1,51. ĹI2aq +e- =I-aq ; DrGį2 = - F Eį(I2aq /I-aq ) =-96500*0,62. I-aq + Mn3+aq = ĹI2aq +Mn2+aq. (2) K = [Mn2+aq][I2aq]Ĺ / ([Mn3+aq][I-aq]). Calculer la constante d'ťquilibre thermodynamique de cette derniŤre rťaction. DrGį = -RT ln K = DrGį1 -DrGį2 =-F(Eį(Mn3+aq /Mn2+aq ) - Eį(I2aq /I-aq )) =-96500*(1,51-0,62) = -8,59 104 J mol-1. ln K =8,59 104 /(8,31*298) =34,7 ; K = 1,15 1015. Aux 50 mL de la solution prťlevťs il est nťcessaire d'ajouter un volume Veq de solution de thiosulfate de sodium pour observer l'ťquivalence. Ecrire l'ťquation support du titrage. Comment repŤre t-on l'ťquivalence ? I2aq +2S2O32-aq = 2I-aq +S4O62-aq.(3) En prťsence de diiode, l'empois d'amidon donne une teinte violet foncť. Etablir l'expression de la concentration molaire en dioxygŤne dissous dans l'eau de mer en fonction de Veq, V0 et C1. D'aprŤs (3) : n(I2aq) = Ĺn(S2O32-aq) ; d'aprŤs (2) n(I2aq) = Ĺn(Mn3+aq) ; d'aprŤs (1) n(Mn(OH)3 (s)) = n(Mn3+aq) ; d'aprŤs (0) n(O2 aq) = 0,25 n(Mn(OH)3 (s)) d'oý : n(O2 aq) =0,25 n(S2O32-aq) = 0,25C1 Veq. [O2 aq] =0,25C1 Veq / V0.
|
||||||
|
|
