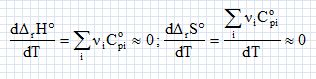|
Par
chauffage du carbonate de cobalt, on obtient le monoxyde de cobalt CoO.
Si on porte CoO ŗ haute tempťrature, il est converti en Co3O4.
On ťtudie ici l'ťquilibre entre les deux oxydes :
6CoO(s) + O2(g) =2Co3O4(s). (1)
Le dioxygŤne gazeux sera considťrť comme un gaz parfait. Les deux solides CoO(s) et Co3O4(s) sont non miscibles.
|
|
On considŤre que l'enthalpie standard de la rťation (1) est pratiquement indťpendante de la tempťrature.
Montrer que l'entropie standard de la rťaction est aussi indťpendant de la tempťrature.
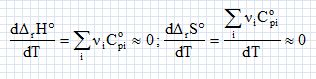
Exprimer l'enthalpie libre standard de la rťaction (1) en fonction de la tempťrature T.
Constituant
|
O2(g) |
CoO(s) |
Co3O4(s) |
DfHį ( kJ mol-1)
|
0
|
-237,9
|
-891,0
|
Sį( J K-1 mol-1)
|
205,2
|
53,0
|
102,5
|
DrGį =DrHį - T DrSį.
DrHį = 2 DfHį(Co3O4(s))-DfHį(O2(g) )-6 DfHį(CoO(s)).
DrHį = 2*(-891,0) -6(-237,9) = -354,6 kJ mol-1.
DrSį = 2 Sį(Co3O4(s))-Sį(O2(g) )-6 Sį(CoO(s)).
DrSį = 2*102,5 -205,2-6*53 = -318,2 J K-1 mol-1.
DrGį =-354,6 +0,3182 T.
Exprimer puis calculer
la constante d'ťquilibre Kį1 de la rťaction (1) ŗ 1150 K.
DrGį = -RT ln Kį1 ; ln K = -DrGį / (RT).
DrGį =-354,6 +0,3182 *1150 =11,33 kJ mol-1 = 1,133 103 J mol-1.
ln Kį1 =- 1,133 103 / (8,314*1150) =-1,185 ; Kį1 = 0,306.
En dťduire la pression de dioxygŤne d'ťquilibre Pťq.
Kį1 =Pį / Pťq ; Pťq = Pį / Kį1= 1,0 / 0,306 = 3,27.
|
.
Dťfinir puis calculer la variance du systŤme ŗ l'ťquilibre entre les deux oxydes et le dioxygŤne et conclure.
La variance, notťe v, d'un systŤme physicochimique ŗ l'ťquilibre est
ťgale au nombre de variables intensives indťpendantes que
l'expťrimentateur peut fixer.
v = N-R+2-j.
N = 3 constituants ; R = une relation entre les trois constituants ; 2 paramŤtres intensifs, tempťrature et presssion ; j : 3 phases.
v = 3-1+2-3 = 1.
Un seul paramŤtre intensif, tempťrature ou pression, peut Ítre fixť par
l'expťrimentateur. L'ťtat d'ťquibre du systŤme est alors dťcrit.
Un rťcipient de volume V0 = 10 L contient initialement n1 = 1,00 mol de monooxyde de cobalt CoO(s) , et n2 = 0,300 mol de dioxygŤne gazeux. Le rťcipient est maintenu ŗ la tempťrature de 1150 K.
Indiquer si le monooxyde de cobalt est oxydť dans les conditions initiales.
Qr i = Pį/PO2 ; PO2 =n2 RT / V0 =0,300 *8,314*1150 / 0,010 =2,87 105 Pa = 2,87 bar.
Qr i = 1 / 2,87 = 0,35.
Qr i > Kį1, donc ťvolution du systŤme dans le sens indirect, rťduction de Co3O4(s).
A la tempťrature constante T = 1150 K, le rťcipient subit une compression de volume jusqu'ŗ atteindre un volume final VF = 1,00 L.
Rechercher le domaine des valeurs du volume du rťcipient pour lequel l'oxydation du monooxyde de cobalt a lieu.
Qr i < Kį1, PO2 > Pťq ; n2 RT / V > Pťq ; V < n2 RT / Pťq ;
V < 0,300*8,314*1150 / (3,27 105 ) ; V < 8,77 10-3 m3 ; V < 8,77 L.
Indiquer les espŤces prťsentes dans le rťcipient en fonction du volume V.
10 > V > 8,77 L : O2(g) et CoO(s).
V = 8,77 L : ťtat d'ťquilibre entre les tois espŤces O2(g), CoO(s) et Co3O4(s).
Si V < 8,77 L, ťvolution du systŤme dans le sens direct jusqu'ŗ ce que Qr = Kį1.
|
avancement (mol)
|
6CoO(s)
|
+ O2(g)
|
=2Co3O4(s)
|
| initial |
0
|
1,00
|
0,300
|
0
|
en cours
|
x
|
1,00-6x
|
0,300-x
|
2x
|
ťquilibre
|
xťq
|
1,00-6xťq ~ 0
|
0,300-xťq |
xťq |
xťq ~1/6 et 0,300-xťq = 0,300-1/6 =0,133 mol.
V = nRT / Pťq = 0,133 *8,314 *1150 / (3,27 105 ) =3,9 10-3 m3 = 3,9 L.
Si 1,0 < V < 3,9 L, le systŤme ťvolue vers l'ťtat d'ťquilibre,
les trois espŤces sont prťsentes ( CoO(s) a pratiquement totalement
disparu ).
Si 3,9 < V < 8,77 L, l'ťtat d'ťquilibre est atteint, les trois espŤces sont prťsentes.
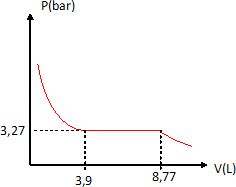
Exprimer la pression P dans l'enceinte en fonction de V et tracer l'allure de la courbe P en fonction de V.
1,0 < V < 3,9 : P = (n2-n1/6) RT / V ; 3,9 < V < 8,77 L : P = 3,27 bar ; 8,77 < V < 10 L : P = n2 RT / V.
|
|