|
|
Les
solutions aqueuses d'acide phosphorique de qualitť alimentaire ont une
densitť comprise entre 1,6 et 1,7 pour un pourcentage massique d'acide
phosphorique allant de 75 ŗ 85 %.
Indiquer
comment prťparer 1,00 L d'une solution d'acide phosphorique ŗ 0,10
mol/L ŗ partir d'une solution commerciale ( 75 % en masse, densitť d =
1,60).
Solution commerciale : masse d'acide pur dans 1 L : 1,60 *0,75 =1,2 kg ;
concentration : 1,2 103 / M(acide phosphorique) = 1,2 103 / 98 =12,2 mol/L.
Facteur de dilution F = 12,2 / 0,1 = 122.
Prťlever 1000 / 122 ~8,2 mL de solution commerciale ŗ l'aide d'une
pipette jaugťe et placťe dans une fiole jaugťe de 1,00 L contenant au
2/3 d'eau distillťe. Complťter avec de l'eau distillťe jusqu'au trait
de jauge. Agiter pour rendre homogŤne.
le graphe pH = f(v) obtenu lors de la simulation du dosage de 20,0 mL
de la solution obtenue par une solution d'hydroxyde de sodium de
concentration molaire 0,20 mol/L est donnť.
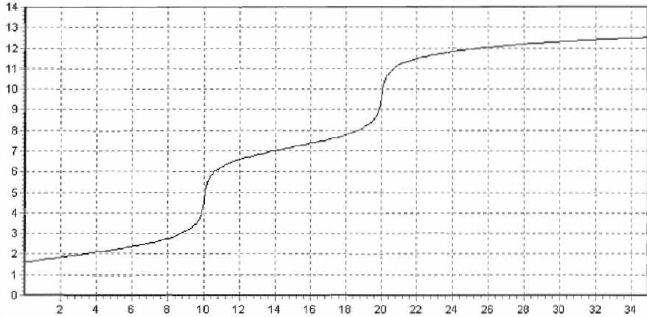
Ecrire les ťquations de la rťaction correspondant ŗ chacune des parties de la courbes.
De 0 ŗ 10 mL : H3PO4aq + HO-aq = H2PO4-aq + H2O(l).
De 10 ŗ 20 mL : H2PO4-aq+ HO-aq = HPO42-aq + H2O(l).
Pourquoi n'observe-t-on que deux sauts de pH alors que l'acide phosphorique est un triacide ?
HPO42-aq + HO-aq = PO43-aq + H2O(l).
La troisiŤme aciditť est trop faible pour Ítre dosťe : la transformation n'est pas totale ŗ l'ťquivalence.
Pourquoi faut-il ťtalonner les solutions de soude destinťes aux titrages acido-basiques des acides faibles ?
Le dioxyde de carbone de l'atmosphŤre est soluble dans l'eau. Il rťagit
avec les ions hydroxyde. La solution de soude est carbonatťe et sa
concentration change.
Quel est le rŰle de chaque ťlectrode utilisťe pour un dosage pHmťtrique ? Quelle est l'opťration prťalable ŗ un titrage pH-mťtrique ?
L'ťlectrode de verre, ťlectrode de mesure est sensible ŗ la
concentration aux ions oxonium ; l'autre ťlectrode sert de rťfťrence.
L'ťlectrode combinťe mesure Everre - Erťfťrence
et traduit cette diffťrence en unitť pH gr‚ce ŗ l'ťtalonnage prťalable
ŗ partir de deux solutions tampon ťtalon ŗ tempťrataure donnťe.
|
.
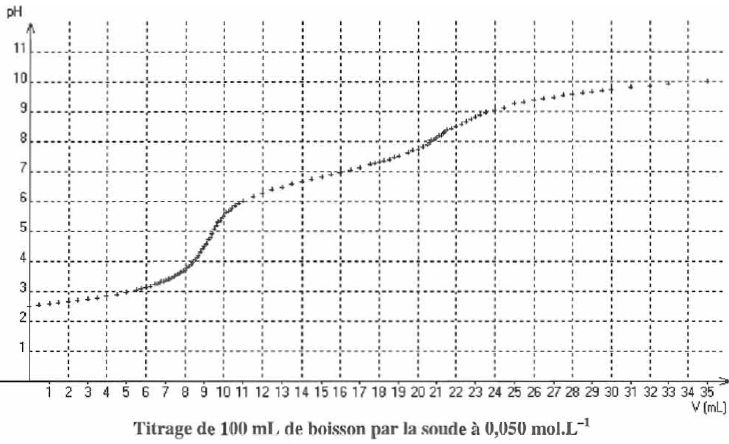
En exploitant le premier saut de pH ( Vťq = 9,4 mL ), ťvaluer la concentration en acide phosphorique dans la boisson.
Si seul l'acide phosphorique est dosť : H3PO4aq + HO-aq = H2PO4-aq + H2O(l).
A l'ťquivalence n(H3PO4aq) = n(HO-aq) = 0,050*9,4 = 0,47 mmol dans 100 mL de boisson titrťe.
[acide phosphorique ] = 0,47 / 100 = 4,7 10-3 mol/L.
Si seul l'acide phosphorique ťtait dosť, quelle valeur atteindrait-on pour la seconde ťquivalence ?
2*9,4 = 18,8 mL.
Si le dťgazage a ťtť effectuť de maniŤre ŗ atteindre l'ťquilibre thermodynamique ŗ 298 K, quelle influence quantitative a la prťsence de CO2 aq sur les volumes aux ťquivalences ?
nCO2aq ťtant trŤs faible, sa prťsence n'aurait aucune influence.
Obtention d'acide phosphorique en TP.
Dans
un becher de 600 mL, introduire 300 mL d'acide sulfurique ŗ 0,5 mol/L
et ajouter petit ŗ petit sous agitation 15,5 g de phosphate
tricalcique. AprŤs une quinzaine de minutes, filtrer, rťcupťrer fe
filtrat et le laver ŗ l'eau distillťe. Sťcher ŗ l'ťtuve ŗ 50 įC pendant
30 min et peser.
Prťlever 50 mL de filtrat prťcťdent et diluer 10 fois. A l'aide des
indicateurs hťlianthine et phťnolphtalťine, rťaliser les dosages
concordants de 20,0 mL de la solution obtenue par la soude ŗ 0,100
mol/L.
Expťrimentalement, le prťcipitť est un solide blanc et les volumes obtenus aux ťquivalences lors des dosages sont Vťq1 = 8,6 mL pour le virage de l'hťlianthine et Vťq2 = 14,4 mL pour le virage de la phťnolphtalťine.
Lors du dosage, ťcrire le(s) ťquation(s) de la rťaction traduisant la transformation jusqu'au virage de l'hťlianthine.
Le phosphate tricalcique et en dťfaut et l'acide sulfurique en excŤs.
On dose donc les deux aciditťs de l'acide sulfurique en excŤs et la
premiŤre aciditť de l'acide phosphorique au virage de l'hťlianthine :
H2SO4aq + HO-aq = HSO4-aq + H2O(l).
HSO4-aq + HO-aq = SO42-aq + H2O(l).
H3PO4aq + HO-aq = H2PO4-aq + H2O(l).
On dťfinit le rendement en acide comme la quantitť de matiŤre d'ion H+ produite rapportť ŗ la quantitť de matiŤre de H+ initial : h = 3 nH3PO4 formť / (2 nH2SO4 initial).
Montrer
que la quantitť d'acide sulfurique de dťpart n'a pas besoin d'Ítre
connue prťcisťment pour ťvaluer le rendement dťfini. Calculer ce
rendement.
A la premiŤre ťquivalence, virage de l'hťlianthine : 2 nH2SO4 dosť + nH3PO4 = Vťq1 CHO-.
Entre les deux ťquivalences, la transformation est modťlisťe par : H2PO4-aq+ HO-aq = HPO42-aq + H2O(l).
nH3PO4 = (Vťq2-Vťq1 ) CHO-.
Ca3PO4(s) + 3H2SO4aq = 2H3PO4aq + 3Ca2SO4(s). nH2SO4 rťagi = 1,5 nH3PO4 ;
nH2SO4 initial = nH2SO4 dosť + 1,5 nH3PO4 =ĹVťq1 CHO- - ĹnH3PO4 + 1,5 nH3PO4 =ĹVťq1 CHO-+ nH3PO4 ;
nH2SO4 initial =ĹVťq1 CHO-+ (Vťq2-Vťq1 ) CHO- =CHO-(Vťq2 -0,5Vťq1).
2nH2SO4 initial =CHO-(2Vťq2 -Vťq1).
h = 3(Vťq2-Vťq1 ) / (2Vťq2 -Vťq1) = 3(14,4-8,6) / (28,8-8,6) =17,4 / 20,2 =0,86.
|
.
|