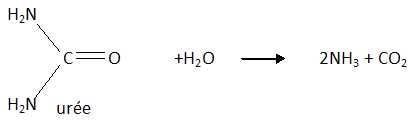.
|
|
Le
chlore est un élément important dans le traitement de l'eau et c'est
sous la forme d'acide hypochloreux ( HClO) que son action désinfectante
est la plus efficace. l'acide hypochloreux peut aussi agir sur les
molécules organiques suivant trois modes d'action : l'oxydation des
alcools, l'addition sur les alcčnes, la synthčse de chloramines.
L'oxydation
du butan-1-ol par l'acide hypochloreux conduit ŕ un composé qui réagit
avec la liqueur de Fehling et avec la DNPH, ainsi qu'ŕ la formation de
l'ion chlorure.
Donner
le nom et la formule du composé obtenu.
Un
test positif ŕ la DNPH indique la présence du groupe carbonyle
>C=O
; un test positif avec la liqueur de Fehling indique la présence d'un
aldehyde, le butanal CH3-CH2-CH2-CHO.
Ecrire les
demi-équation redox puis l'équation bilan de la réaction.
Réduction :
HClO aq +2e- +H+aq = Cl-
aq+ H2O(l).
Oxydation : CH3-CH2-CH2-CH2OH =
CH3-CH2-CH2-CHO
+2e- +2 H+aq.
HClO aq +2e- +H+aq
+CH3-CH2-CH2-CH2OH = Cl-
aq+ H2O(l)+CH3-CH2-CH2-CHO
+2e- +2 H+aq.
Simplifier : HClO
aq + CH3-CH2-CH2-CH2OH = Cl-
aq + H2O(l)+CH3-CH2-CH2-CHO
+ H+aq.
Donner le
nom et la formule du composé obtenu si on utilise un excčs d'oxydant.
On obtient
l'acide butanoďque : CH3-CH2-CH2-CO2H.
|
On
considčre la réaction de l'acide hypochloreux sur l'alcčne de formule CH3-CH=CH-CH3.
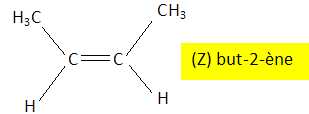
Nommer
l'alcčne et donner la formule du stéréoisomčre Z.
A
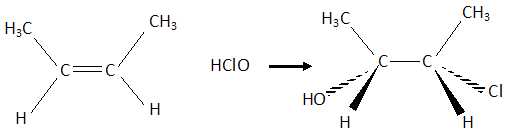
l'aide des formules semi-développées, écrire l'équation de la réaction
d'addition de l'acide hypochloreux sur l'alcčne.
.
Dans
les piscines, des chloramines sont produites par l'action de l'acide
hypochloreux sur les matičres azotées laissées par les baigneurs et
notamment l'urée contenue dans la sueur. Celle-ci s'hydrolyse en
ammoniac qui réagit par la suite avec l'acide hypochloreux produisant
de la monochloramine, responsable de l'odeur chlorée des piscines.
La formule brute de l'urée est CH4N2O.
Donner sa
formule semi-développée puis écrire l'équation de son hydrolyse.
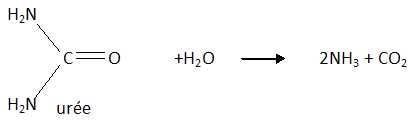
Ecrire la
réaction entre l'ammoniac et l'acide hypochloreux qui conduit ŕ la
monochloramine.
NH3 + HClO ---> Cl-NH2 + H2O.
|
|