Un
amateur d'arťomodťlisme souhaite protťger des rayures les piŤces en
aluminium prťsentes dans son modŤle rťduit d'avion. Pour cela, il
utilise un traitement de surface qui consiste ŗ anodiser l'aluminium afin de le durcir. En effet une couche d'alumine Al2O3
de trŤs faible ťpaisseur recouvre naturellement l'aluminium mais cette
couche fine est sujette ŗ la dťtťrioration. L'anodisation consiste ŗ
oxyder en surface la piŤce en aluminium ; la couche d'alumine ainsi
formťe est plus ťpaisse et garantit une plus grande duretť.
|
|
Couples oxydant / rťducteur : Al2O3(s) /Al(s) ; O2(g) / H2O(l) ; H+aq / H2(g).
NA = 6,02 1023 mol-1 ; e = 1,6 10-19 C ; M(Al2O3) = 102 g/mol ; r(Al2O3) = 4,0 g cm-3.
Principe de l'anodisation.
La piŤce d'aluminium propre est utilisťe comme anode de l'ťlectrolyse d'une solution aqueuse d'acide sulfurique ( 2H+aq + SO42-aq)
de concentration molaire en solutť apportť c =2,0 mol/L. La cathode est
constituťe d'une barre de graphite. On utilise un gťnťrateur de tension
et un ampŤremŤtre.
Indiquer le sens conventionnel du courant et le sens de circulation des ťlectrons.
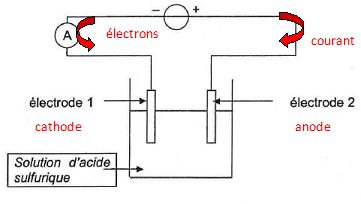
Un dťgagement gazeux se produit ŗ la cathode.
Ecrire
la demi-ťquation (1) d'oxydo-rťduction expliquant cette observation en
utilisant l'un des couples citťs. Justifier le choix de ce couple.
Une rťduction se produit ŗ la cathode nťgative. L'oxydant de l'un des
couple conduit ŗ un gaz, le rťducteur de ce mÍme couple. Seul le
couple H+aq / H2(g) convient.
2H+aq + 2e- = H2(g). (1).
L'aluminium doit Ítre oxydť. Indiquer l'emplacement du graphite et celui de la piŤce.
Une oxydation se produit ŗ l'anode positive ( piŤce en aluminium ) ; une rťduction a lieu ŗ la cathode nťgative ( graphite).
Ecrire la demi ťquation (2) relative au couple Al2O3(s) /Al(s).
2Al(s) + 3H2O= Al2O3(s) + 6H+aq + 6e- (2).
En dťduire que l'ťquation d'oxydo-rťduction de la rťaction d'ťlectrolyse est .
2Al(s) + 3H2O= Al2O3(s) + 3H2(g).
Multiplier (1) par 3 et ajouter ŗ (2) :
6H+aq + 6e- = 3H2(g).
2Al(s) + 3H2O + 6H+aq + 6e- = 3H2(g) + Al2O3(s) + 6H+aq + 6e-.
Simplifier l'ťcriture : 2Al(s) + 3H2O= Al2O3(s) + 3H2(g).
S'agit-il d'une transformation spontanťe ou forcťe ? Justifier.
L'ťlectrolyse est une transformation forcťe, nťcessitant un apport d'ťnergie sous forme ťlectrique.
|
.
Etude quantitative de l'ťlectrolyse.
La surface de la piŤce ŗ anodiser est S = 9,0 cm2. L'intensitť du courant est maintenue ŗ I = 120 mA pendant la durťe Dt = 18 min.
Exprimer la quantitť de matiŤre d'ťlectrons ťchangťs en fonction de I, Dt, NA et e.
Quantitť d'ťlectricitť Q = I Dt = n(e-) NA e ; n(e-) = I Dt / (NA e).
Quelle relation existe-t-il entre la quantitť de matiŤre d'alumine formťe et n(e-) ?
2Al(s) + 3H2O= Al2O3(s) + 6H+aq + 6e- (2).
n(Al2O3) = n(e-)/ (6NA e) M(Al2O3).
Montrer que la masse maximale d'alumine formťe est : m = IDt / (6NA e) M(Al2O3). Calculer sa valeur.
m = n(alumine) M(Al2O3) = n(e-) M(Al2O3) / 6 ;
m = I Dt / (6NA e) M(Al2O3).
m = 0,120 * 18*60 / (6*6,02 1023*1,60 10-19) *102 =2,2873 10-2 ~2,3 10-2 g.
Le rendement r de l'ťlectrolyse est de 90 %.
En dťduire la masse d'alumine rťellement formťe.
2,2873 10-2 *0,90 = 2,059 10-2 ~2,1 10-2 g.
L'amateur souhaite obtenir une couche d'alumine d'une ťpaisseur minimale d = 7,0 Ķm sur toute la surface.
Calculer le volume V' d'alumine ŗ dťposer.
V' = S d = 9,0 * 7,0 10-4 = 6,3 10-3 cm3.
Dťterminer la masse m' correspondante.
m' = V' r(Al2O3) = 5,147 10-3 *4,0 =2,52 10-2 ~2,5 10-2 g.
L'ťpaisseur minimale d'alumine souhaitťe n'est pas obtenue.
Quels paramŤtres de l'ťlectrolyse peut-il modifier pour augmenter la quantitť d'alumine dťposťe ?
L'intensitť du courant et la durťe de l'ťlectrolyse peuvent Ítre augmentťes.
|
|
