Eau
oxygťnťe ŗ 10 volumes.
Pour dťsinfecter une plaie au genou d'une personne agťe, j'ai utilisť
une solution d'eau oxygťne ŗ 10 volumes comme antiseptique. J'ai
observť des marques d'rritation et de brulures.
Le titre, notť T, d'une eau oxygťnťe est un nombre ťgal au volume de
dioxygŤne exprimť en litres que libŤre un litre de solution d'eau
oxygťnťe dans les conditions normales de tempťrature et de pression.
|
|
L'eau
oxygťnťe est une solution aqueuse de peroxyde d'hydrogŤne H2O2.
Le peroxyde d'hydrogŤne a la particularitť d'^tre soit oxydant soit
rťducteur. L'eau oxygťnťe appartient donc ŗ deux couples
oxydant / rťducteur.
Pour vťrifiier le titre d'une eau oxygťnťe on rťalise un dosage. Cette
eau oxygťnťe est dosťe par une solution de permanganate de potassium de
concentration c1 = 1,0 mol/L. On prťlŤve un
volume V2 = 10 mL d'eau oxygťnťe.
Complťter
le schťma suivant.
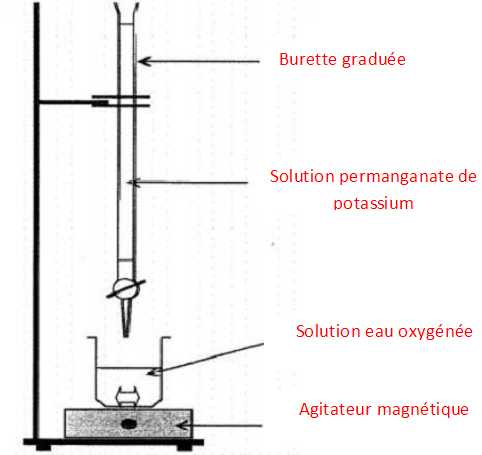
|
.
Les deux couples
oxydant / rťducteur utilisťs dans ce dosage sont : O2
/ H2O2 et MnO4-
/Mn2+. On donne les demi-ťquations
d'oxydorťduction :
MnO4- + 8H+
+ 5e- = Mn2+ + 4H2O
(1)
O2
+ 2H+ + 2e- =H2O2
(2)
A partir de ces deux
demi-ťquations, recopier et complťter l'ťquation de la rťaction du
dosage donnťe ci-dessous:
MnO4- + ....H2O2
+.......H+ --> ..... +......+ ........
2 fois (1) : 2MnO4- + 16H+
+ 10e- = 2Mn2+ + 8H2O
5 fois (2) ťcrire en sens inverse : 5
H2O2 =5O2
+ 10H+ + 10e- .
Ajouter : 2MnO4- + 16H+
+ 10e- + 5 H2O2
= 2Mn2+ + 8H2O
+5O2
+ 10H+ + 10e- .
Simplifier : 2MnO4-
+ 6H+ + 5 H2O2
= 2Mn2+ + 8H2O
+5O2 .
Dťfinir l'ťquivalence
d'un dosage.
A l'ťquivalence les quantitťs de matiŤre des rťactifs sont en
proportions stoechiomťtriques. Avant l'ťquivalence, l'un des rťactifs
est en excŤs ; aprŤs l'ťquivalence, l'autre rťactif est en excŤs.
A l'ťquivalence nH2O2 = 2,5 n MnO4-.
On note VE le volume de permanganate de
potassium versť ŗ l'ťquivalence et c2 la
concentration de la solution d'eau oxygťnťe.
Etablir
la relation entre c1, c2, V2 et VE ŗ
l'ťquivalence.
nH2O2 =c2 V2
; n MnO4-= c1 VE
et nH2O2 = 2,5 n MnO4-
d'oý : c2 V2
=2,5 c1 VE .
Montrer
que c2 = 2,7
mol/L si VE = 10,8 mL.
c2 =2,5 c1 VE
/ V2 =2,5 *1,0 *10,8 / 10 =2,7 mol/L.
La relation entre le titre T et
la concentration molaire c d'une eau oxygťnťe est T = 11,2 c.
En
dťduire le titre T de la solution d'eau oxygťnťe.
T = 11,2 *2,7 =30,24 ~30 volumes.
Le
stagiaire a t-il utilisť une solution de mauvais titre qui pourrait
expliquer la brŻlure de la personne agťe ?
Oui, le titre dťterminť expťrimentalement est trois fois supťrieur ŗ 10 volumes.
|
|
|
