Le
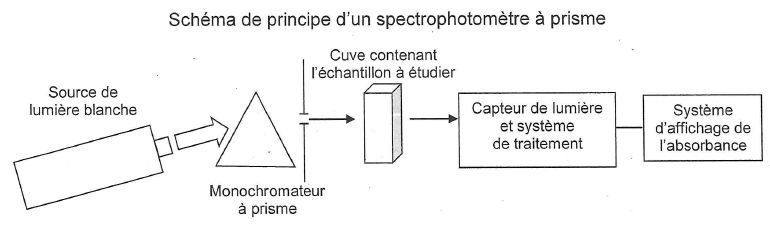
principe de la spectrophotomťtrie repose sur la mesure de l'absorbance
A de l'espŤce X en solution dans un solvant Y. cette grandeur est le
rťsultat de la comparaison de deux intensitťs lumineuses : celle d'une
radiation monochromatique ayant traversťe une cuve transparente
contenant le solvant Y, et celle de la mÍme radiation ťlmergent de la
mÍme cuve contenant la solution de l'espŤce X dans le solvant Y.
|
|
LumiŤre et
spectrophotomťtrie.
Donner les valeurs
limites des longueurs d'onde du spectre visible dans le vide et les
couleurs correspondantes.
400 nm : violet ; 800 nm : rouge.
Situer,
du point de vue de leur longueur d'onde, les rayonnements ultraviolets
et infrarouges par rapport au visible.
Les longueurs d'onde des UV sont infťrieures ŗ 400 nm ; celles des
infrarouges sont supťrieures ŗ 800 nm.
Le rŰle du monochromateur dans un spectrophotomŤtre est de sťlectionner
une radiation monochromatique particuliŤre.
Donner la dťfinition
d'une lumiŤre monochromatique.
Une lumiŤre monochromatique est constituťe d'une onde possťdant une
seule frťquence, c'est ŗ dire une seule couleur.
Certains monochromateurs comportent un prisme en verre.
Dťfinir
l'indice de rťfraction n d'un milieu transparent.
L'indice de rťfraction est le rapport de la cťlťritť de la lumiŤre dans
le vide ŗ celui de la cťlťritť de la lumiŤre dans le milieu transparent.
De
quel paramŤtre caractťristique d'une radiation lumineuse dťpend
l'indice n pour un milieu transparent donnť ?
L'indice de rťfraction dťpend de la longueur d'onde de la radiation
lumineuse.
Le prisme de verre dťcompose la lumiŤre blanche.
Nommer le phťnomŤne
responsable de cette dťcomposition et le dťcrire briŤvement.
Un prisme
de verre disperse ( phťnomŤne de dispersion) la lumiŤre blanche. A la
sortie du prisme on observe un arc en ciel, le bleu ťtant plus dťviť
que le rouge.
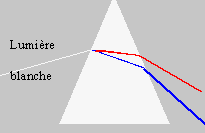
Lors d'une rťfraction air-verre, la dťviation
d'une radiation lumineuse est d'autant plus importante que la longueur
d'onde de la radiation est faible. Sans faire de calcul
complťter la
figure en y faisant figurer le trajet d'un rayon lumineux bleu et
d'un rayon lumineux rouge ŗ l'intťrieur du prisme et aprŤs sa sortie.
|
.
Dosage colorimťtrique par ťtalonnage.
On
se propose de dťterminer la concentration en diiode dans une teinture
d'iode officinale. On dilue 200 fois la teinture d'iode trop
concentrťe pour une ťtude spectrophotomťtrique directe. La
solution diluťe est notťe S.
Par ailleurs, on dispose d'un ensemble de solutions aqueuses de diiode notťes Di de concentrations connues toutes diffťrentes. Ces solutions ont des colorations proches de la solution S.
Masse molaire de l'iode M = 127 g/mol.
On peut trouver expťrimentalement un encadrement de la concentration en
diiode de la solution S, sans utiliser de spectrophotomŤtre.
Expliquer briŤvement la mťthode.
On rťalise une ťchelle de teintes ŗ partir de solutions de concentrations connues de diiode. On situe la solution S
par comparaison dans cette gamme de teintes.
Pourquoi lors de la mise en oeuvre de cette mťthode, faut-il que les rťcipients utilisťs soient tous identiques ?
On
compare les teintes de solutions de concentrations connues ŗ celle de
la solution S, dont la couleur doit Ítre situťe dans la gamme.
La comparaison n'est possible et fiable que si tous les rťcipients sont identiques.
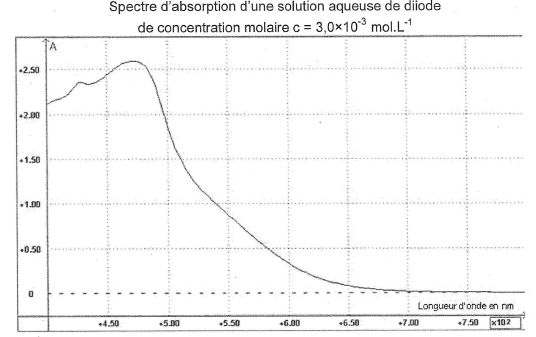
A l'aide d'un spectrophotomŤtre, on mesure l'absorbance Ai de chaque solution Di de diode, puis celle de la solution S.
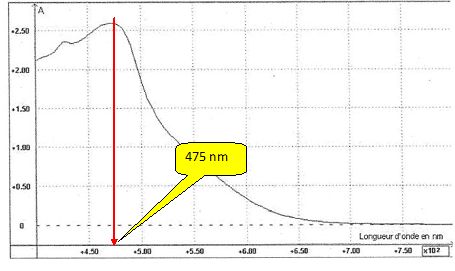
Donner la valeur d'une longueur d'onde qui vous paraÓt bien appropriťe et justifier.
On choisit une longueur d'onde pour laquelle la solution prťsente un maximum d'absorption.
On obtient les rťsultats suivants :
concentration C ( Ķmol/L)
|
50
|
100
|
250
|
500
|
750
|
1000
|
absorbance A
|
0,041
|
0,10
|
0,22
|
0,46
|
0,70
|
0,87
|
Absorbance de la solution S : A = 0,78.
La courbe d'ťtalonnage de l'absorbance en fonction de la concentration
est fournie ci-dessous. La relation entre l'absorbance A et la
concentration C est appelťe loi de Beer-Lambert. Elle s'ťcrit A = k C
avec k une constante et C la concentration molaire de l'espŤce colorťe
dans la solution.
La courbe d'ťtalonnage est-elle en accord avec cette loi ? Justifier.
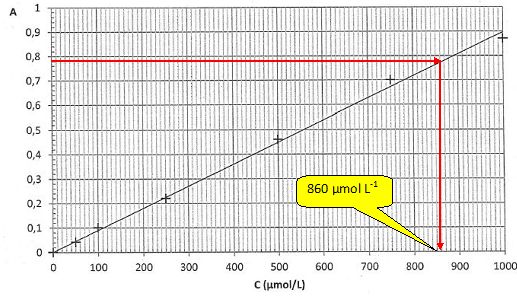
La
courbe est une droite passant par l'origine ; son ťquation est de la
forme A = k C, ce qui est en accord avec la loi de Beer-Lambert.
Dťterminer graphiquement la concentration molaire CS exp en diiode de la solution S. En dťduire la concentration molaire Cexp en diiode de la teinture d'iode officinale.
CS exp = 860 Ķmol /L ~8,6 102 Ķmol /L Cexp = 200 CS exp =200 *8,60 10-4 =0,172~0,17 mol/L.
La teinture d'iode officinale est ťtiquetťe ŗ 5,0 % en masse de diiode. Sa masse volumique est r = 9,0 102 g/L.
Vťrifier que la concentration massique Cm en diiode attendue dans cette teinture est 45 g/L.
Masse de un litre de solution : 900 g ; masse de diiode dans un litre de solution : Cm = 900*0,05 =45 g /L.
En dťduire la concentration molaire attendue Ca en diiode dans cette teinture.
Ca = Cm / M(I2) = 45/(127*2) =0,177 ~0,18 mol/L.
Calculer l'ťcart relatif entre la valeur expťrimentale ŗ la valeur attendue et conclure.
|Cexp-Ca| *100 / Ca= (0,177-0,172) *100 / 0,177 =2,8 %.
Cet ťcart est trŤs faible, les rťsultats expťrimentaux sont en accord avec l'indication de l'ťtiquette.
|
|
|




