|
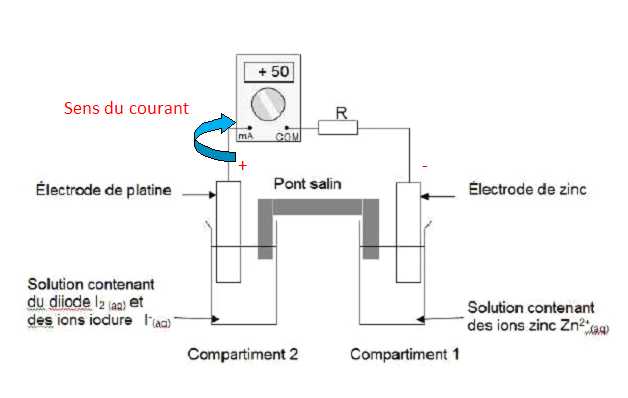
Dosage pour dťterminer la durťe de fonctionnement d'une pile, bac S Polynťsie 2012. |
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
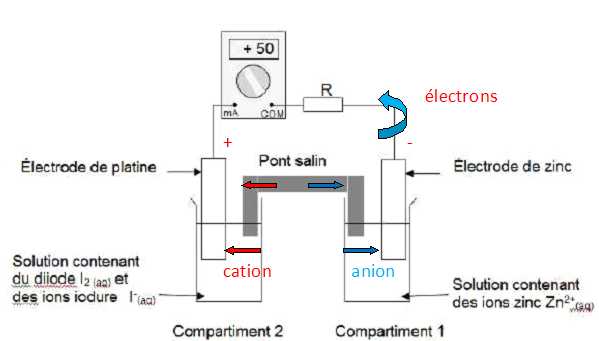
Donner l’expression du quotient de rťaction initial Qri et calculer sa valeur. Qri = [I-(aq)]02 [Zn2+(aq)]0 / [I2(aq)]0 =(5,0 ◊ 10-2)2*1,0 ◊ 10-1 / 1,0 ◊ 10-1 = 2,5 10-3. La constante d’ťquilibre associťe ŗ l’ťquation de la rťaction ayant pourrťactifs le zinc mťtal et le diiode en solution aqueuse est K = 1046 ŗ la tempťrature T = 25 įC. Prťvoir le sens d’ťvolution spontanťe du systŤme chimique constituant la pile. Qri < K, donc ťvolution spontanťe dans le sens direct. Que peut-on dire de l’ťvolution de la concentration molaire en diiode dans le compartiment 2 lorsque la pile fonctionne ? Justifier ŗ partir de l’expression du quotient de rťaction Qr. Lors du fonctionnement de la pile Qr tend vers K : Qr augmente fortement. Qr = [I-(aq)]2 [Zn2+(aq)] / [I2(aq)]. [I-(aq)], [Zn2+(aq)] augmente, [I2(aq)], un rťactif, diminue.
Durťe de fonctionnement de la pile. On laisse fonctionner la pile pendant la durťe Dt. On suppose que l’intensitť I du courant dťbitť par la pile reste constante et ťgale ŗ 50 mA. Pour dťterminer la quantitť de matiŤre de diiode ayant ťtť consommťe pendant le fonctionnement de la pile, on dose le diiode restant dans le compartiment 2 de la pile avec une solution incolore de thiosulfate de sodium (2 Na+ (aq) + S2O32-(aq)) de concentration molaire en solutť apportť C1 = 2,0 ◊ 10-1 mol.L-1. On prťcise que la couleur brune de la solution du compartiment 2 est due ŗ la prťsence de diiode, seule espŤce colorťe mise en jeu. Le volume de solution de thiosulfate de sodium versť ŗ l’ťquivalence est V1,E = 14,7 mL. L’ťquation de la rťaction servant de support au dosage est : 2S2O32-(aq) + I2(aq) = S4O62-(aq) + 2 I-(aq). Faire un schťma annotť du dispositif expťrimental de dosage. 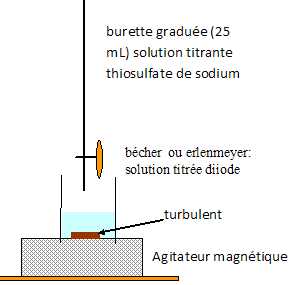 Dťfinir l’ťquivalence d’un dosage. Comment la repŤre-t-on ici ? A l'ťquivalence les quantitťs de matiŤre des rťactifs sont en proportions stoechiomťtriques. Avant l'ťquivalence, l'un des rťactifs est en excŤs, aprŤs l'ťquivalence, l'autre rťactif est en excŤs. En prťsence d'empois d'amidon, le diiode donne une teinte violette foncť. l'ťquivalence est repťrťe par la disparition de cette couleur. Quantitť de matiŤre de diiode consommť. Complťter le tableau d’avancement On note x l’avancement de la rťaction de dosage.
n2 -xťq=0 ; n2 = xťq ; de plus n1-2xťq= 0 soit n1=2xťq ; de plus n1=C1V1,E ; par suite n2 = ĹC1V1,E = 0,5 *0,20 *14,7 10-3 = 1,47 10-3 ~1,5 10-3 mol. En dťduire la quantitť de matiŤre ncons(I2) de diiode consommť lors du fonctionnement de la pile. n0(I2) = [I2(aq)]0 V = 0,10 *0,100 = 1,0 10-2 mol. ncons(I2) = n0(I2) - n2 = 1,0 10-2 -1,47 10-3 ~8,5 10-3 mol.
|
||||||||||||||||||||||||||||||
|
|