Les
solutions aqueuses d'ammoniac sont obtenues par dissolution du gaz
ammoniac dans l'eau. L'ammoniac dissous NH3aq
est l'espŤce basique du couple ion ammonium / ammoniac.
|
|
Ecrire
l'ťquation de la rťaction de l'ion ammonium avec l'eau et donner
l'expression de la constante d'acidiitť du couple ion
ammonium / ammoniac.
NH4+aq +H2O(l)
=NH3aq
+H3O+aq. Ka
= [H3O+aq][NH3aq]
/ [NH4+aq].
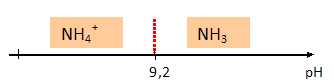
Etablir le
diagramme de prťdominance relatif au couple ion ammonium / ammoniac et
donner l'espŤce prťdominante dans la solution ťtudiťe dont
le pH est 10,2.
pKa( NH4+aq
/ NH3aq) = 9,2 ; ŗ pH
supťrieur ŗ pKa, la forme base NH3aq prťdomine.
On dťcide de titrer un volume VB=10,0 mL de
solution aqueuse d'ammoniac de concentration CB
= 0,100 mol/L.
On utilise une burette de 25 mL et on dispose de plusieurs flacons
d'acide chlorhydrique H3O+aq
+Cl-aq dont les concentrations sont : C1
=1,00 10-2 mol/L ; C2 =1,00 10-1
mol/L ; C3
=1,00 mol/L.
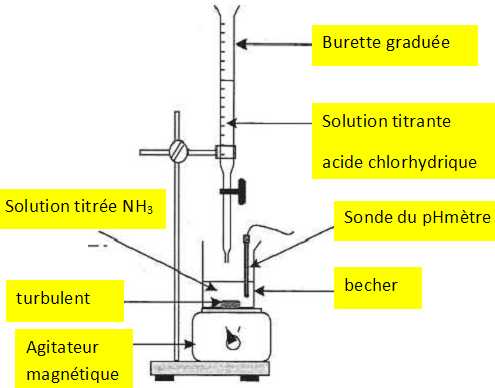
Lťgender
le dispositif de titrage.
Donner
l'ťquation de la rťaction support du titrage.
NH3aq +H3O+aq =NH4+aq
+H2O(l).
|
Dťterminer le volume de la chute Va
de burette pour atteindre l'ťquivalence pour chacune des
trois solutions d'acide chlorhydrique.
A l'ťquivalence Va Cacide
= CB VB ; Va = CB
VB / Cacide.
Va
1= CB VB
/ C1 = 0,100*10,0 / 1,00 10-2= 100 mL ; Va 2=
CB VB / C2 = 0,100*10,0 / 1,00 10-1= 10,0 mL ;
Va
3= CB VB
/ C3 = 0,100*10,0 / 1,00 = 1,00 mL.
En dťduire
la solution du laboratoire la mieux adaptťe ŗ ce titrage.
(1) ne convient pas, il faudrait remplir plusieuurs fois la burette ;
(3) : le volume d'acide est trop petit, imprťcision sur le volume VA
; (2) convient.
On
donne la courbe obtenue lors de ce titrage.
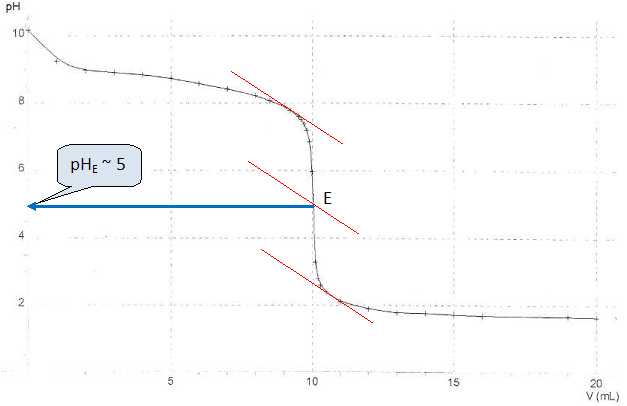
Quel
indicateur colorť convient le mieux ? Indiquer la variation de couleur
observťe.
|
couleur
forme acide |
zone de virage |
couleur
forme base |
| carmin
indigo |
bleu |
11,6 - 14,0 |
jaune |
| thymolphtalťine |
incolore |
9,3 - 10,5 |
bleu |
| bleu
de bromothymol |
jaune |
6,0 - 7,6 |
bleu |
| vert
de bromocrťsol |
jaune |
3,8 - 5,4 |
bleu |
La zone de virage de
l'indicateur colorť doit contenir le pH du point ťquivalent : le vert
de bromocrťsol convient.
La couleur passe
du bleu au jaune.
Quand
le bleu apparaÓt.
Dans une fiole jaugťe de volume V = 100,0 mL, un chimiste rťalise le
mťlange suivant :
VM =20,0 mL d'une solution de molybdate
d'ammonium de concentration CM =4,0 10-2
mol/L ; 10 mL d'acide sulfurique ŗ 4,5 mol/L ; VF
= 20,0 mL d'une solution de fructose de concentration CF
=2,0 10-4 mol/L.
Le mťlange est complťtť ŗ 100,0 mL avec de l'eau distillťe.
La solution S obtenue, initialement incolore, est rťpartie dans des
tubes ŗ essai placťs dans un bain-marie. Une coloration bleue de plus
en plus intense apparaÓt peu ŗ peu dans chaque tube. Les tubes sont
sortis du bain-marie les uns aprŤs les autres ŗ diffťrents instants et
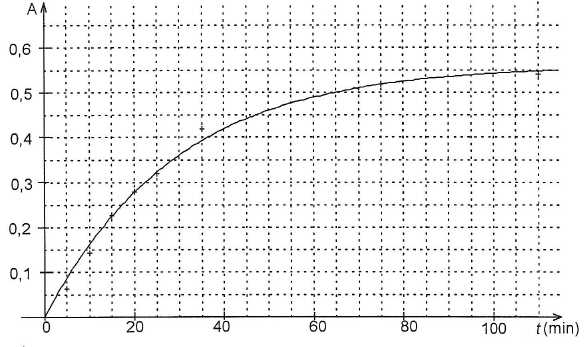
plongťs dans de l'eau glacťe pendant quelques minutes. L'absorbance de
la solution S ŗ ces diffťrents instants est mesurťe ŗ une longueur
d'onde de 720 nm. La mesure de l'absorbance en fonction du temps est
donnťe. L'absorbance A est reliťe ŗ la concentration C de l'espŤce
colorťe par la relation : A = k C oý k est une constante.
Lors de cette rťaction, le fructose (F) est oxydť en un produit (F')
incolore. Le molybdate d'ammonium notť Mo(ox) est rťduit en Mo(red).
L'ťquation de la rťaction peut s'ťcrire :
F + Mo(ox) = F' + Mo(red) (1).
Dťterminer
l'espŤce responsable de la couleur bleu.
Fructose, Mo(ox), F' sont incolores ; Mo(red) est responsable de la
couleur bleue.
L'allure
de la courbe est-elle en cohťrence avec l'observation expťrimentale ?
Interprťter.
" Une coloration bleue de plus en plus intense apparaÓt peu ŗ peu " :
la concentration en Mo(red) augmente ; l'absorbance est proportionnelle
ŗ la concentration de l'espŤce colorťe : A augmente avec le
temps.
En
dťduire l'expression de la concentration [Mo(red)] en fonction de
l'absorbance A mesurťe.
A = k [Mo(red)] ; [Mo(red)] = A / k
On
donne l'expression de la vitesse volumique de la rťaction :v = 1/V
dx/dt.
Complťter
le tableau d'ťvolution de la transformation (1).
| ťtat |
avancement
(mol) |
F |
+Mo(ox) |
=F' |
+Mo(red) |
| initial |
0 |
VFCF
=0,020*2,0 10-4
=4,0 10-6. |
VMCM
=0,020*4,0 10-4
=8,0 10-6. |
0 |
0 |
| en
cours |
x |
VFCF
-x = 4,0 10-6-x |
VMCM -x
= 8,0 10-6-x |
x |
x |
| fin |
xf |
4,0 10-6-xf |
8,0 10-6-xf |
xf |
xf |
Montrer
que l'absorbance est proportionnelle ŗ l'avancement ŗ tout instant.
[Mo(red) ]= x / V ; A = k [Mo(red) ] = k/V x avec V
constant.
Montrer
que la vitesse volumique de la rťaction peut s'ťcrire : v = 1/k dA/dt.
v = 1/V dx/dt avec x = A V/k ; dx/dt = V/k dA/dt d'oý : v = 1/k dA/dt.
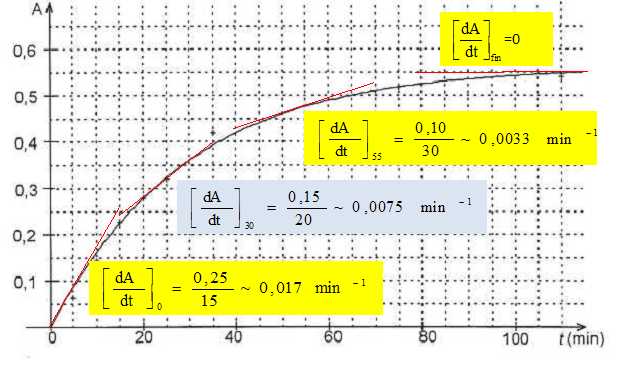
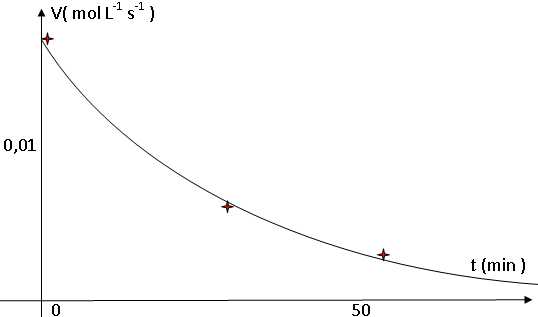
Tracer
l'allure de l'ťvolution de la vitesse volumique au cours du temps.
Indiquer
si la variation de l'intensitť de la couleur est mieux dťtectťe par le
chimiste pendant la premiŤre ou la deuxiŤme heure de l'enregistrement.
Pendant la premiŤre heure, l'absorbance passe de zťro ŗ 0,50 ; pendant
la deuxiŤme heure, l'absorbance passe de 0,50 ŗ 0,55.
L'absorbance est proportionnelle ŗ la concentration de l'espŤce colorťe
: la variation de la couleur est grande durant la premiŤre
heure.
Au bout d'une durťe suffisamment longue, l'ansorbance atteint sa valeur
finale Afin = 0,56.
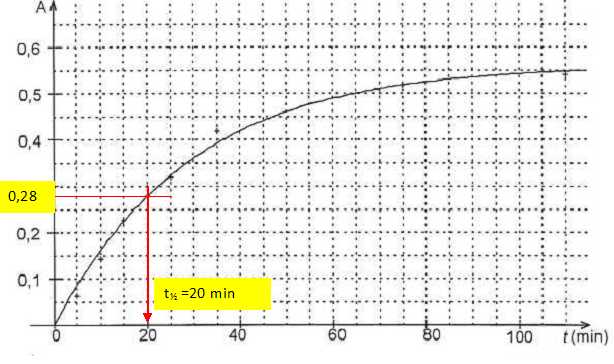
Dťterminer
la valeur du temps de demi-rťaction. Justifier.
L'absorbance ťtant proportionnelle ŗ l'avancement et l'avancement au
temps de demi-rťaction ťtant ťgal ŗ la moitiť de l'avancement final, on
recherche l'abscisse correspondant ŗ l'absorbance Ĺ Afin =
0,28.
Pendant les cinq premiŤres minutes, le chimiste s'inquiŤte car il ne
voit aucune apparition de la couleur prťvue.
Proposer
une modification du protocole permettant une diminution de la valeur du
temps de demi-rťaction.
Travailler ŗ une tempťrature un peu plus ťlevťe.
|
|
|






