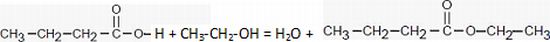L'ananas
est sans doute le plus emblťmatique des fruits tropicaux. Son parfum
unique et sa couronne verdoyante lui ont valu, dans bien des pays, le
surnom de ę roi des fruits Ľ.
L'arŰme trŤs attrayant de l'ananas a ťtť l'objet de beaucoup de travaux
d'analyse : plus de 280 substances aromatiques ont ťtť identifiťes.
Tenter de recrťer l’odeur et la saveur si subtiles de l’ananas demeure
un dťfi de taille pour le chimiste.
L’arŰme artificiel d’ananas est obtenu industriellement en mťlangeant
sept esters, trois acides carboxyliques et sept huiles essentielles.
Les trois composťs majoritaires de ce mťlange sont le butanoate
d’ťthyle (22%),
l’ťthanoate d’ťthyle (15%) et l’acide butanoÔque (12%). D’aprŤs
orkos.com et Introduction to Organic Laboratory Techniques, A
Contemporary Approach de Donald L. Pavia
|
|
L’objectif
de cet exercice est d’ťtudier d’une part la prťparation de l’acide
butanoÔque ŗ partir du beurre et d’autre part la rťaction de synthŤse
du butanoate d’ťthyle. L’acide butanoÔque et le butanoate d’ťthyle sont
deux espŤces chimiques prťsentes dans l’ananas.
Prťparation de l’acide butanoÔque ŗ partir du beurre.
L’acide butanoÔque peut Ítre prťparť ŗ partir de la butyrine que l’on trouve dans le beurre.
…tape 1 : la butyrine rťagit ŗ chaud avec une solution aqueuse concentrťe d’hydroxyde de sodium (Na+ + HO-)aq.
AprŤs refroidissement et autres traitements, on obtient du savon.
…tape 2 : on dissout le savon obtenu prťcťdemment dans de l’eau chaude et on le fait rťagir avec une solution d’acide chlorhydrique (H3O+ + Cl -)aq. On obtient de l’acide butanoÔque.
Donnťes :
La butyrine est un corps gras de formule semi-dťveloppťe :
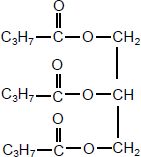
l’ťquation de la rťaction chimique entre la butyrine et la solution d’hydroxyde de sodium est :
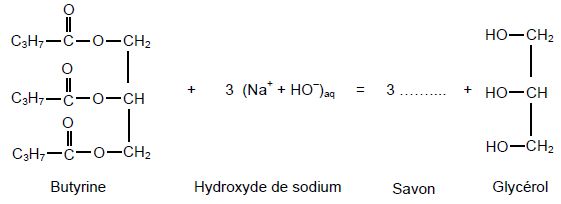
Comment s’appelle la rťaction chimique qui consiste ŗ faire rťagir la butyrine avec la solution
d’hydroxyde de sodium ?
Hydrolyse basique ou saponification d'un ester.
Donner la formule du savon obtenu et identifier sa partie hydrophobe.
C3H7-COO- + Na+. La partie hydrophobe est la chaÓne carbonťe C3H7-.
Lors de l’ťtape 2, une rťaction acido-basique mettant en jeu l’ion butanoate C3H7-COO- se produit.
…crire l’ťquation de cette rťaction chimique.
C3H7-COO- aq +H3O+aq = C3H7-COOH aq + H2O(l)
Exprimer la constante d’ťquilibre de cette rťaction. Calculer sa valeur ŗ 25įC.
C3H7-COOH / C3H7-COO- pKa= 4,8.
K = [C3H7-COOH] / ([C3H7-COO-][H3O+]) =1 / Ka = 104,8= 1,6 10-5.
|
.
SynthŤse du butanoate d’ťthyle.
Le butanoate d’ťthyle a pour formule semi-dťveloppťe :
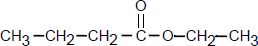
Il est synthťtisť en faisant rťagir l'acide butanoÔque (A) et un alcool (B).
ņ quelle famille de composťs organiques appartient le butanoate d’ťthyle ? Ester.
…crire l’ťquation de la rťaction chimique de synthŤse du butanoate d’ťthyle en utilisant les formules semi-dťveloppťes.
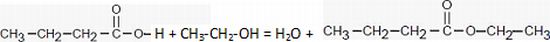
Donner le nom de l'alcool (B). Ethanol ou alcool ťthylique.
Rappeler les caractťristiques de cette transformation chimique.
Lente, pratiquement athermique, limitťe par l'hydrolyse de l'ester.
SynthŤse au laboratoire.
Dans un ballon, on mťlange une quantitť de matiŤre nA = 0,22 mol d’acide butanoÔque (A) avec un volume VB = 12,8 mL d’alcool (B). On ajoute environ 1 mL d’une solution concentrťe d’acide sulfurique et
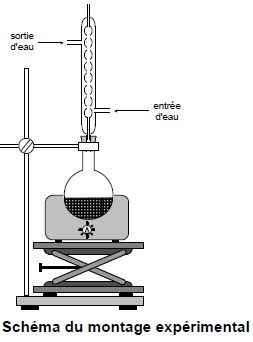
quelques grains de pierre ponce. On rťalise le montage ci-dessous et on chauffe ŗ ťbullition pendant 30 minutes.
On refroidit ensuite le ballon sous le robinet d’eau froide, puis on
verse son contenu dans un rťcipient contenant de l’eau salťe. On
observe deux phases liquides que l’on sťpare ŗ l’aide d’une ampoule ŗ
dťcanter. La phase organique est alors lavťe et sťchťe. On obtient une masse mE = 14,8 g de butanoate d’ťthyle (E).
Nom
|
Masse molaire ( g/mol)
|
Masse volumique ( g/mL)
|
acide butanoÔque (A)
|
MA=88
|
rA =0,96
|
alcool (B)
|
MB=46 |
rB =0,79 |
butanoate d'ťthyle (E)
|
ME=116 |
rE =0,88 |
Comment nomme-t-on le montage ci-dessus ? Chauffage ŗ reflux.
L’acide sulfurique concentrť ajoutť dans le mťlange rťactionnel sert de catalyseur.
Quel est le rŰle d’un catalyseur ?
Le catalyseur augmente la vitesse de la rťaction sans modifier la composition du mťlange ŗ l'ťquilibre.
Donner l’expression littťrale de la quantitť de matiŤre nB d’alcool introduite dans le ballon.
masse : m = VB rB ; nB = m/MB = VB rB /MB.
Le mťlange d’acide butanoÔque (A) et d’alcool (B) est ťquimolaire. Calculer le rendement de la synthŤse.
rendement = nE rťelle / nE thťorique max ; nE rťelle = mE / ME = 14,8 / 116 = 0,128 mol ; nE thťorique max = nA = 0,22 mol.
Rendement = 0,128/0,22 ~0,58 ( 58 %).
On souhaite augmenter la quantitť maximale de butanoate d’ťthyle produit. Plusieurs propositions sont envisagťes :
Proposition 1 : ajouter l’alcool (B) en excŤs au 0,22 mol d’acide butanoÔque ;
Proposition 2 : doubler le volume d’acide sulfurique ;
Proposition 3 : remplacer l’acide butanoÔque par l’anhydride correspondant.
Quelle(s) est (sont) celle(s) qui le permet(tent) (aucune justification n’est demandťe) ?
Propositions 1 et 3.
|
|