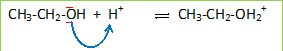Pendant
longtemps la chirurgie a ťtť confrontťe au problŤme de la douleur des
patients.
Ne disposant d’aucun produit permettant de la soulager, le mťdecin ne
pouvait
pratiquer une opťration ę ŗ vif Ľ du patient.
L'ťther diťthylique ťtait connu depuis le XVIŤme siŤcle,
mais ce n'est qu'en 1840 que William T G Morton eut l'idťe de
l'utiliser afin d'endormir un patient. Et il fallu attendre l'automne
1846 pour que, dans deux amphithťatres combles, le docteur John Warren,
assistť de William Morton, rťussisent deux opťrations chirurgicales
indolores pour les patients. L'anesthťsie venait de naÓtre et allait
permettre l'essor rapide de la chirurgie....
|
|
Composť
|
ťthanol
|
ťther
diťthylique
|
eau
|
ťthylŤne
( ťthŤne)
|
Formule
brute
|
C2H6O
|
C4H10O |
H2O
|
C2H4
|
Tempťrature
d'ťbullition ( sous 1 bar)
|
78
įC
|
25
įC
|
100įC
|
-104įC
|
Masse
molaire ( g/mol)
|
46
|
74
|
18
|
28
|
Masse volumique d’une solution aqueuse
d’hydroxyde
de sodium : r = 1,0 g.mL-1 ;
Masse
volumique de l’ťthanol : rťthanol
= 0,81 g.mL-1 ;
Masse
volumique de l’ťther diťthylique : rťther
= 0,71 g.mL-1 ;
L’eau
et l’ťther ne sont pas miscibles ; la
tempťrature du laboratoire est de 20įC.
SynthŤse de
l’ťther
diťthylique : choix d'un protocole.
La synthŤse de l’ťther diťthylique peut se faire par
dťshydratation de l’ťthanol. Cependant selon les conditions opťratoires
choisies, la dťshydratation peut aboutir ŗ deux produits diffťrents.
Les deux ťquations de
rťaction correspondantes sont les suivantes :
CH3-CH2-OH → CH2=CH2
+ H2O
2 CH3-CH2-OH
→
CH3-CH2-O-CH2-CH3 + H2O
La tempťrature joue un rŰle important dans l’orientation de
la rťaction : une tempťrature moyenne favorise la formation de
l’ťther
diťthylique, une tempťrature ťlevťe celle de l’ťthylŤne.
Complťter
le tableau :
Conditions
opťratoires
|
Tempťrature
įC
|
Nom du
produit
|
Catťgorie
de la rťaction
en chimie organique
|
| (1)
: vapeurs d’ťthanol sur de
l’alumine |
300 |
ťthylŤne |
ťlimination |
| (2)
: ťthanol chauffť en
prťsence d’un acide
fort. |
140
|
ťther
diťthylique
|
substitution
|
|
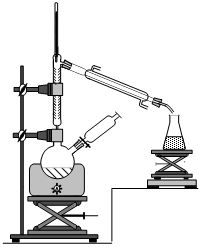
Pour
synthťtiser l’ťther
diťthylique, on suit le protocole expťrimental suivant :
- rťaliser un
montage de
distillation fractionnťe dans lequel un ballon bicol supporte une
colonne ŗ
distiller ainsi qu’une ampoule de coulťe ;
- verser 25 mL
d’ťthanol dans le
ballon et placer dans l’ampoule de coulťe 10 mL d’un acide fort,
l’acide
sulfurique concentrť ;
- sous agitation,
verser goutte
ŗ goutte l’acide sulfurique dans le mťlange, puis chauffer ;
- rťcupťrer le
distillat lorsque
la tempťrature en tÍte de colonne est ŗ 35įC ;
- verser le
distillat dans une
ampoule ŗ dťcanter, ajouter une solution aqueuse d’hydroxyde de sodium
Na+(aq)
+ HO-(aq) ;
- rťcupťrer la phase contenant l'ťther diťthylique.
|
|
|
Pourquoi
faut-il mettre l’erlenmeyer de rťcupťration du distillat dans un bain
de
glace ?
Sous une pression de 1 bar, la tempťrature d'ťbullition de l'ťther
diťthylique est ťgale ŗ 35 įC : l'ťther s'ťvapore facilement ŗ la
tempťrature du laboratoire, d'oý l'utilisation d'un bain de glace.
Malgrť les
prťcautions
prises, la formation d’ťthylŤne peut avoir lieu de faÁon minoritaire
mais pour
autant on ne le trouve pas dans le distillat.
ņ l’aide des donnťes,
proposer une explication.
A
la tempťrature du laboratoire, ŗ la tempťrature du bain de glace,
l'ťthylŤne est un gaz (Tťbullition = -104 įC ).
Calculer
la quantitť de matiŤre d’ťthanol introduite dans le ballon et la masse
attendue
d’ťther diťthylique.
m(ťthanol)
= Vťthanol rťthanol
= 25*0,81 = 20,25 g.
n(ťthanol) = m / Mťthanol = 20,25 / 46 =0,4402 ~0,44 mol.
D'aprŤs les nombres stoechiomťtriques de l'ťquation n(ťther) =
Ĺn(ťthanol) = 0,22 mol.
m(ťther) = n(ťther) Mťther = 0,22 *74 =16,288 ~16 g.
Le
distillat obtenu prťsente un caractŤre acide. Quelle ťtape du
protocole permet
d’ťliminer les traces acides du distillat ? Justifier.
"ajouter une
solution aqueuse d’hydroxyde de sodium Na+(aq)
+ HO-(aq) ".
Rťaction acide base entre l'acide sulfurique et l'hydroxyde de sodium :
H3O+aq + HO-aq ---> 2H2O.
Oý
se trouve l’ťther diťthylique dans l’ampoule ŗ dťcanter ? Justifier.
La phase aqueuse, la plus dense, occupe la partie infťrieure ; la phase
ťthťrťe, la moins dense, occupe la partie supťrieure de l'ampoule ŗ
dťcanter.
Etude du mťcanisme de la synthŤse
de l'ťther diťthylique.
Le mťcanisme rťactionnel proposť pour la rťaction de
dťshydratation conduisant ŗ l’ťther diťthylique est proposť ci-dessous.
Il
comporte trois ťtapes.
Etape (a) : CH3-CH2-OH + H+
 CH3-CH2-OH2+ CH3-CH2-OH2+
Etape
(b) : CH3-CH2-OH2+ + CH3-CH2-OH
 CH3-CH2-OH+-CH2-CH3
+
H2O CH3-CH2-OH+-CH2-CH3
+
H2O
Etape (c) :
CH3-CH2-OH+-CH2-CH3  CH3-CH2-O-CH2-CH3 +
H+ CH3-CH2-O-CH2-CH3 +
H+
A
l’aide de vos connaissances sur les sites donneurs et accepteurs de
doublets
d’ťlectrons, expliquer l’ťtape (a) du mťcanisme.
L'atome d'oxygŤne possŤde deux doublets libres : il joue le rŰle de
donneur d'ťlectrons ; H+ prťsente un dťfaut
d'ťlectrons et joue le rŰle d'accepteur.
Recopier
l’ťquation de l’ťtape (a) et faire
apparaÓtre la flŤche courbe schťmatisant le transfert ťlectronique.
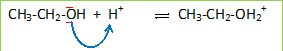
En observant les
ťquations
des ťtapes (a) et (c), justifier que
l’acide sulfurique n’est pas un rťactif
dans cette synthŤse. Quel peut alors Ítre son rŰle dans la synthŤse ?
L'acide sulfurique apporte des ions oxonium consommť ŗ l'ťtape a. Ces
ions sont rťgťnťrťs ŗ l'ťtape c : l'ion oxonium joue le rŰle de
catalyseur et non pas celui de rťactif.
Techniques
d'analyses des espŤces chimiques intervenant dans la rťaction.
Les
techniques utilisťes sont la spectroscopie infrarouge IR
et la spectromťtrie RMN du proton.
On donne
pages 8 et 9 deux spectres RMN du proton et deux
spectres infrarouge (IR) correspondant ŗ l’ťther diťthylique et ŗ
l’ťthanol
ainsi qu’une table de donnťes de spectroscopie infrarouge IR.
| Liaison |
C-C
|
C-O
|
O-H
acide carboxylique |
C-H
|
O-H
alcool
|
| Nombre
d'onde ( cm-1) |
1000-1250
|
1050-1450
|
2500-3200
|
2800-3000
|
3200-3700
|
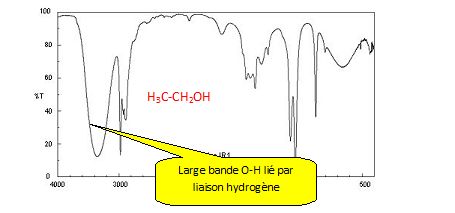
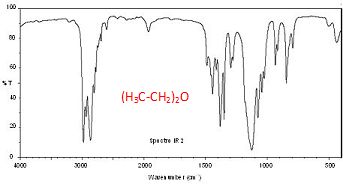
Associer
chaque spectre infrarouge IR et RMN ŗ la molťcule
correspondante en justifiant.
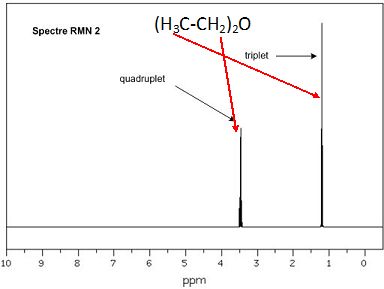
Attribuer
un signal RMN ŗ chaque groupe de protons chimiquement ťquivalents et
justifier sa multiplicitť pour chacun des signaux.
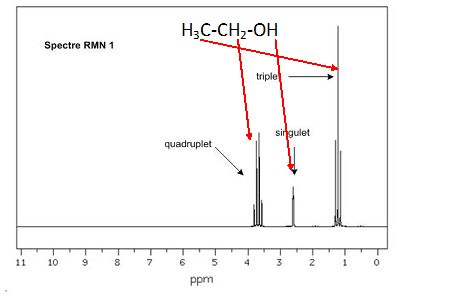 |
CH3
: ces protons ťquivalents ont 2 protons proches voisins, on observe un
triplet.
CH2 : ces protons ťquivalents ont 3 protons proches voisins,
on observe un quadruplet.
OH : ce proton n'a aucun proton proche voisin, on observe un singulet.
|
|
CH3
: ces protons ťquivalents ont 2 protons proches voisins, on observe un
triplet.
CH2 : ces protons ťquivalents ont 3 protons proches voisins,
on observe un quadruplet. |
|
|
La kťtamine.
ņ
l’heure
actuelle, du fait de son extrÍme inflammabilitť, de ses nombreux effets
secondaires, de sa toxicitť ainsi que du risque ťlevť de dťpendance
qu’il
entraÓne, l’ťther diťthylique n’est pratiquement plus utilisť comme
anesthťsiant, et d’autres molťcules beaucoup plus spťcifiques l’ont
remplacť.
C’est le cas par exemple de la kťtamine, qui contient un mťlange
ťquimolaire
des deux molťcules ci-dessous.
Reproduire la
formule
topologique de la molťcule A. Entourer et identifier les groupes
caractťristiques prťsents dans cette molťcule.
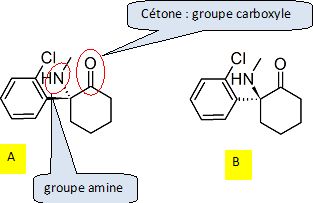
Quelle
est la diffťrence entre les molťcules A et B ?
A et B sont deux ťnantiomŤres : configuration spatiale diffťrente
autour de l'atome de carbone asymťtrique.

Du
fait de son action rapide, la kťtamine est principalement
utilisťe en mťdecine d’urgence. Elle est le plus souvent administrťe
via une
injection intraveineuse unique avec une dose de l’ordre de 2 mg par kg
de corps
humain et sa demi-vie d’ťlimination est de 2 ŗ 4 heures.
Par
analogie avec le temps de demi-rťaction dťfini en
cinťtique chimique, proposer une
dťfinition au terme de ę demi-vie
d’ťlimination Ľ donnť dans le texte.
Durťe au bout de laquelle la moitiť de la kťtamine administrťe
initialement est ťliminťe de l'organisme.
|
|
|