|
Utilisation du (+)-camphre comme source
d'auxiliaire chiral :
concours
Capes 2011 |
|||||||
|
|||||||
|
La stéréochimie initiale du camphre naturel : le(+)-camphre va permettre de synthétiser une molécule énantiomčriquement pure : le chlorure de (+)-(1S, 4S)- camphanoyle, un intermédiaire de synthčse des urololctones, dérivés des hexoses communément appelés " sucres nus". On considčre la séquence réactionnelle suivante : 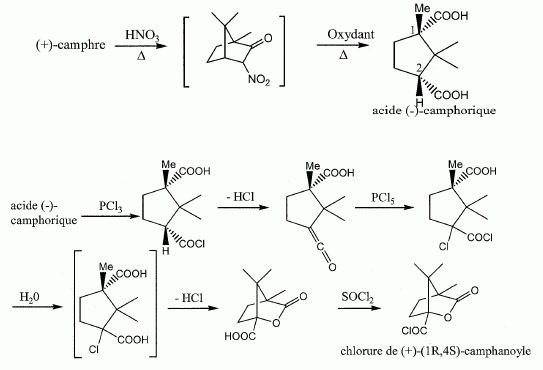 Etude de la synthčse de l'acide (-)-camphorique. Qui a introduit la notion de stéréoisomčres ? Sur quelle molécule ? Comment a-t-elle été mise en évidence ? Louis pasteur observe en 1849 que certains sels de l'acide tartrique ( tartrates ) ont la propriété de faire tourner un rayon de lumičre polarisée plane. Que signifie le (-) dans " acide (-)-camphorique" ? Il existe deux variétés de substances optiquement actives : les substances lévogyres qui font tourner le plan de polarisation vers la gauche et les substances dextrogyres qui font tourner ce plan vers la droite. Par convention, une molécule lévogyre est notée (-), et une molécule dextrogyre est notée (+). Quel appareil utilise-t-on pour le mettre en évidence ? L' instrument qui permet de mesurer les rotations optiques est le polarimčtre.
Donner les
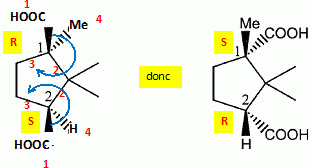
configuration absolues des carbones asymétriques de l'acide camphorique
en justifiant. Les deux groupes prioritaires -COOH se trouvent du męme côté du cycle : donc isomčres cis. Etude de la chloration de l'acide(-)-camphorique. On utilise deux dérivés de chloration ŕ base de phosphore : le pentachlorure de phosphore et le trichlorure de phosphore. A partir de quelle matičre Brand at-il découvert le phosphore en 1669 ? D'oů vient le nom phosphore ? Brand découvre le phosphore ŕ partir de l'urine. Le nom vientdu mot grec phosphoros qui signifie porteur de lumičre. Donner la configuration électronique de l'atome de phosphore. 1s2 2s2 2p6 3s2 3p3. Préciser la ligne, la colonne et le bloc de l'élément phosphore. "3s2 3p3" : 3č ligne ; colonne 15 (VA) et bloc : p. Cet élément vérifie-t-il la rčgle de l'octet dans PCl3 ? dans PCl5 ? Justifier le cas échéans pourquoi le phosphore peut ne pas vérifier la rčgle de l'octet. Le phosphore vérifie la rčgle de l'octet dans PCl3, mais pas dans PCl5 ( 10 électrons sur la couche externe ). Les orbitales 3 d proches sont vacantes et peuvent donc ętre utilisées. Il y a 9 orbitales atomiques caractérisées par le nombre quantique n = 3. Etude du chlorure de(+)-(1R, 4S)-camphanoyle. Quel est le nom de la molécule SOCl2 ? Chlorure de thionyle Donner la structure de Lewis de cette molécule. Donner sa géométrie ŕ l'aide de la théorie VSEPR en justifiant.
Quelle est la fonction obtenue lors de l'action de ce réactif sur un acide carboxylique ? Les acides carboxyliques sont transformés en chlorure d'acyle. Donner les produits secondaires obtenus lors de l'action de SOCl2 sur un acide carboxylique. RCOOH + SOCl2 = RCOCl + HCl + SO2. ( chlorure d'hydrogčne et dioxyde de soufre ). On présente cette synthčse comme présentant une rétention de configuration. Est-ce contradictoire avec le fait de passer de l'énantiomčre (+) au (-) puis au (+) ? Justifier. Rétention de configuration : l'arrangement spatial des substituants autour du site de réaction est identique dans le réactif et dans le produit. Une séquence de deux inversions de type SN2 ne change pas la configuration.
Le camphre comme intermédiaire de synthčse. Il s'agit de transformer le bornéol en isobornéol en formant le camphre comme produit intermédiaire. Pour simplifier le schéma réactionnel, il ne sera représenté qu'un seul stéréoisomčre du bornéol, du camphre et de l'isobornéol. 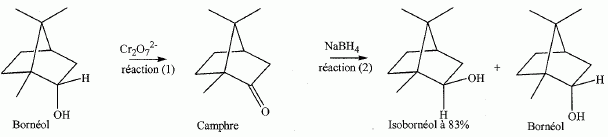 Donner la définition d'isomčres. Deux isomčres ont la męme formule brute mais des arrangements spatiaux différents ( formule semi-développées différentes ). Quel type de stéréoisomčrie existe-t-il entre le bornéol et l'isobornéol ? Ce sont deux énantiomčres. Le carbone porteur du groupe OH change de configuration. Donner le nom de la substance NaBH4. Borohydrure de sodium ou tétrahydridoborate de sodium. A quelle famille de réaction appartient la réaction (1). Justifier en déterminant le nombre d'oxydation du carbone fonctionnel dans le bornéol et le camphre. Réaction d'oxydoréduction : le nombre d'oxydation du carbone fonctionnel dans le bornéol ( un alcool) est : alcool H3COH : 3 + n.o(C) -2+1 = 0 ; n.o(C) = -II. Dans une cétone ou un aldehyde H2CO : 2+n.o(C) -2 = 0 d'oů n.o(C) = 0 dans le camphre. La stéréochimie de la réaction (2) est particuličrement intéressante. Cette réaction est dite stéréosélective. L'ion hydrure peut attaquer en endo, il se forme l'isobornéol ŕ 83% ou en exo, il se forme le bornéol. Justifier cette stéréosélectivité ŕ l'aide d'un mécanisme réactionnel. Le carbone porteur du groupe cétone, hybridé sp2, est plan. L'ion hydrure attaque de préférence du côté opposé au pont, côté le moins encombré. BH4- est source d'hydrure : BH4- = H- + BH3. 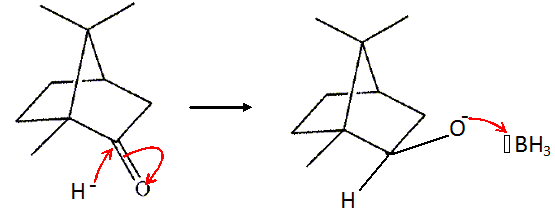
|
|||||||
| |
|||||||
|
|