|
Autour de l'eau oxygťnťe : bts chimiste 2011. |
||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||
Calcul d’une ťnergie de liaison.
|
|
|
ťtude de la structure d’un solide ionique
L’eau oxygťnťe peut Ítre ťgalement prťparťe
en traitant du peroxyde de baryum BaO2 par de l’acide sulfurique. Le
peroxyde de baryum est obtenu par action du dioxygŤne sur l’oxyde de baryum BaO,
solide ionique dont la structure est ťtudiťe ici. Donner la structure
ťlectronique de l’ion Ba2+. 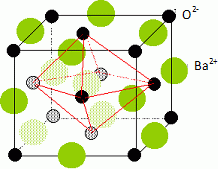 La masse volumique de l’oxyde de
baryum est ρ = |
Etude thermodynamique de la dismutation de l’eau
oxygťnťe
Vťrifier que le
potentiel standard du couple H2O2(aq)/H2O(l)
vaut 1,77 V.
Eį(O2(g) / H2O(l)) = 1,23 V. Eį(O2(g) / H2O2(aq))= 0,69 V.
(1) ĹO2(g) +2H+aq + 2e- = H2O(l) ; DGį1 =-2FEį(O2(g) / H2O(l)).
(2) O2(g) +2H+aq + 2e- = H2O2(aq) ; DGį2 =-2FEį(O2(g) / H2O2(aq)).
(3) H2O2(aq) + 2H+aq + 2e- =2 H2O(l). DGį3 =-2FEį(H2O2(aq)/H2O(l)).
2 fois (1) -(2) donne (3) : -4 FEį(O2(g) / H2O(l)) + 2 FEį(O2(g) / H2O2(aq)) = -2FEį(H2O2(aq)/H2O(l)).
Eį(H2O2(aq)/H2O(l)) = 2 Eį(O2(g) / H2O(l)) -Eį(O2(g) / H2O2(aq)) =2*1,23-0,69 = 1,77 V.
En dťduire que, au
moins ŗ pH = 0, l’eau oxygťnťe se dismute. ťcrire
l’ťquation de la rťaction de dismutation faisant intervenir une mole de H2O2
et dťfinir la constante de rťaction correspondante Kį.
Eį(O2(g) / H2O(l)) = 1,23 V.
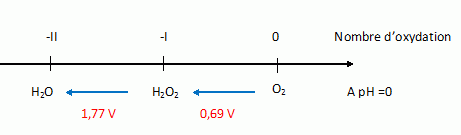
Il y a dismutation d'une espŤce si celle-ci est ťcrite ŗ droite d'une autre espŤce avec un potentiel infťrieur : (4) H2O2(aq) =ĹO2(g) + H2O(l).
Calculer Kį ŗ 298 K.
de plus DGį4 = -RT ln Kį ; ln Kį =1,08 F/(RT) = 42. Kį =1,7 1018.
|
|
L’eau oxygťnťe, au laboratoire, peut Ítre
utilisťe comme oxydant ou comme rťducteur.
…crire l’ťquation de la rťaction de
l’eau oxygťnťe avec le permanganate de potassium en prťsence d’acide sulfurique.
2 fois {
MnO4- + 8H+ +
5e- = Mn2+ + 4H2O
} rťduction
5 fois
{H2O2 = O2 +
2H+ + 2e- }
oxydation
2 MnO4- + 5
H2O2 + 6H+ = 5
O2 + 2 Mn2+ + 8H2O.
…crire l’ťquation
de la rťaction de l’eau oxygťnťe avec les ions iodure en solution aqueuse.
Proposer un mode opťratoire de dosage de l’eau oxygťnťe utilisant cette
derniŤre rťaction en prťcisant la prťparation de l’ťchantillon, le choix du
rťactif titrant ainsi que le repťrage de l’ťquivalence.
2I- =I2 + 2e-
oxydation
H2O2 +2e-
+2H3O+= 4H2O
rťduction
L'ťquation bilan de la rťaction :
H2O2 + 2I-
+2H3O+=
4H2O + I2.
Equation bilan du dosage du diiode formť par le
thiosulfate :
2S2O32- =
S4O62-+2e-
oxydation ; I2+2e-
=2I- rťduction
2S2O32- + I2 =
S4O62- + 2I-
d'oý n(I2)
=Ĺn(S2O32-).
Indicateur de fin de rťaction : en prťsence de diiode, l'empois d'amidon
donne une couleur violette foncťe.
Une eau oxygťnťe est
dite ŗ ę v
volumes Ľ, si un litre de cette solution dťgage par dťcomposition complŤte,
en eau et en dioxygŤne, v
litres de dioxygŤne, ŗ
Quantitť de matiŤre de dioxygŤne n(O2) = V / Vm = 110 / 22,4 = 4,91 mol.
H2O2(aq) =ĹO2(g) + H2O(l).
D'aprŤs les coefficients stoechomťtriques de cette ťquation n(H2O2(aq)) = 2 n(O2) ==2*4,91 =9,82 mol dans 1 L. [H2O2(aq)] = 9,82 mol/L.
|
|
Etude cinťtique de la dismutation de l'eau oxygťnťe. On considŤre la rťaction de
dismutation de l’eau oxygťnťe en solution aqueuse : 2 H2O2(aq) --> 2 H2O(l) + O2(g). Les ions Fe3+ catalysent cette rťaction.
Montrer que la relation suivante est vťrifiťe : VO2 / (Voo-VO2) = 2c0kt. 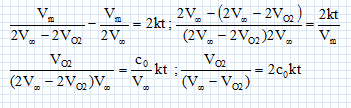 |
Vťrifier graphiquement que la rťaction est bien d'ordre 2 et en dťduire la valeur de la constante de vitesse k.
On trace le graphe VO2/(Voo-VO2) = f(t).
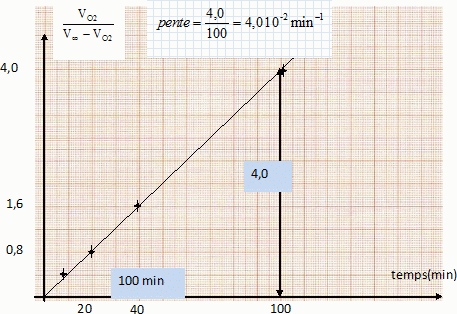
On obtient une droite ( ce qui confirme l'ordre 2 par rapport ŗ H2O2 ) de pente 0,04 = 2 c0 k.
k = 0,04 / (2c0) =0,04 / (2*2) = 0,010 L mol-1 min-1.