Structure d'un ťdifice covalent.
Ecrire la structure ťlectronique des atomes d'hydrogŤne, d'oxygŤne et de chlore.
H ( Z=1) : 1s1 ; O( Z=8) : 1s2 2s2 2p4 ; Cl( Z=17) : 1s2 2s2 2p6 3s2 3p5.
En dťduire le schťma de Lewis des molťcules d'eau et de chlorure d'hydrogŤne puis celui de l'ion oxoniumH3O+.
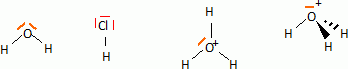
En
dťduire par la mťthode VSEPR le type et le nom de la gťomťtrie pour la
molťcule d'eau et l'ion oxonoim, puis les reprťsenter dans l'espace.
Molťcule d'eau : type AX2E2, triangulaire plan.
Ion oxonium : type AX3E, pyramide ŗ base triangulaire.
|
|
Dosage acido-basique.
A 25įC, pKa (CH3COOHaq / CH3COO-aq) = 4,8 ; pKe = 14.
On dose par pHmťtrie, un volume VA = 50,0 mL d'un mťlange
d'une solution aqueuse d'acide acťtique ( ou ťthanoÔque )
et d'une solution aqueuse d'acide chlorhydrique ( H3O+aq ; Cl-aq ) de concentration molair erespective CAH et CHCl ŗ l'aide d'une solution aqueuse de soude de formule Na+aq + HO-aq de concentration molaire CB =0,500 mol/L. Les rťsultats du titrage ont permis de tracer la courbe pH = f(VB), VB ťtant le volume de solution aqueuse de soude ajoutťe.
Ecrire les ťquations chimiques correspondantes aux deux rťactions de titrage.
CH3COOHaq + HO-aq = CH3COO-aq +H2O(l)
H3O+aq+ HO-aq =2H2O(l)
Ecrire et calculer les constantes d'ťquilibre de ces deux rťactions. En dťduire quel acide est dosť en premier.
K1 =[CH3COO-aq] /([CH3COOHaq][HO-aq]).
Or Ka1 = [CH3COO-aq][H3O+aq] / [CH3COOHaq]
d'oý : K1 = Ka1/ ([H3O+aq][HO-aq]) =Ka1/Ke = 10-4,8 / 10-14 = 109,2 ~1,6 109.
K2 =1/ ([H3O+aq][HO-aq])= 1 / Ke = 1014.
K2 est bien supťrieur ŗ K1 : l'acide chlorhydrique est dosť en premier.
K2 est trŤs diffťrent de K1 : les deux acides sont dosťs successivement.
Dťterminer graphiquement les coordonnťes des points d'ťquivalence E1 et E2.
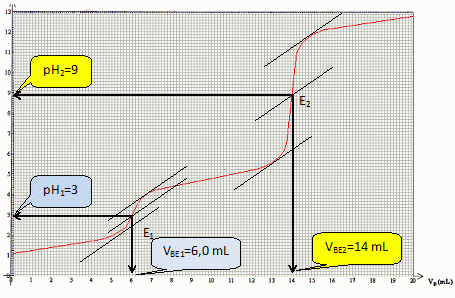
|
Calculer les concentrations molaires des deux acides dans le mťlange.
CHCl VA = CB VBE1 ; CHCl = CB VBE1 /VA = 0,500 *6,0 / 50,0 =6,0 10-2 mol/L.
CAH VA = CB (VBE2-VBE1 ) ; CAH = CB (VBE2-VBE1 ) /VA = 0,500 *8,0 / 50,0 =8,0 10-2 mol/L.
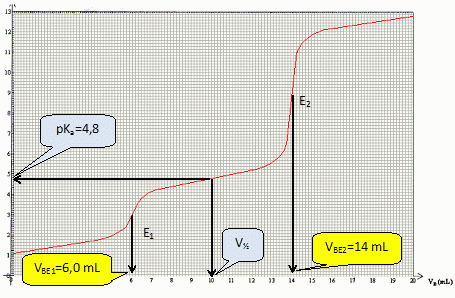
Justifier que le volume ŗ la demi ťquivalence, notť VĹ, du deuxiŤme dosage est ťgal ŗ 10 mL. Retrouver graphiquement la valeur du pKa du couple (CH3COOHaq / CH3COO-aq).
VĹ = VBE1 + Ĺ(VBE2-VBE1) = Ĺ(VBE2+VBE1) = 0,5( 14+6) = 10 mL.
Faire
l'inventaire des espŤces chimiques ioniques majoritairement prťsentes ŗ
la seconde ťquivalence. Justifier, sans calculs, que le pH soit
supťrieur ŗ 7 ŗ cette ťquivalence.
Cl- aq apportť par l'acide chlorhydrique. Cet ion n'est ni un acide, ni une base.
Na+aq apportť par la solution de soude : c'et ion n'a aucune propriťtť acidobasique.
CH3COO-aq ion formť lors du dosage de l'acide ťthanoÔque. Cet ion est une base, base conjuguťe de l'acide ťthanoÔque.
La solution contenant une espŤce aux propriťtťs basiques, aura un pH supťrieur ŗ 7.
|
|


