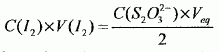|
Saponification
; dosage d'oxydoréduction :
bac ST2S Nlle Calédonie 2010 |
|||||||
|
|||||||
|
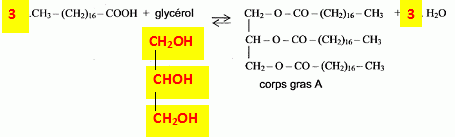
Connu et utilisé avant l'čre chrétienne, le savon étatit ŕ l'origine une mixture obtenue ŕ partir de cendres et de suif ( graisse animale ). A la fin du XVIIe sičcle, l'industrie marseillaise importait des matičres premičres de tout le bassin méditerranéen. Pour répondre ŕ une demande croissante, on mit au point un procédé de fabrication qui employait des corps gras végétaux ( ou graisses végétales) ŕ la place de corps gras animaux. La cendre, provenant de matičre végétale marine, contient de l'hydroxyde de sodium NaOH. celle, provenant de matičre végétale terrestre, contient de l'hydroxyde de potassium KOH. Ces deux espčces chimiques sont des bases. Donner la définition d'une base selon Brönsted. Une base est une espčce, ion ou molécule, susceptible de gagner un proton H+. Par dissolution des deux espčces chimiques NaOH et KOH dans l'eau, on obtient l'ion HO-. Donner le nom de cet ion et montrer qu'il se comporte comme une base. L'ion hydroxyde peut gagner un proton selon : HO- + H+ = H2O. L'ion hydroxyde se comporte comme une base. Le suif contient un triglycéride, corps gras noté A, obtenu ŕ partir de l'acide octadécanoďque de formule semi-développée CH3-(CH2)16-COOH et du glycérol ou propan-1, 2, 3-triol. Expliquer pourquoi l'acide octadécanoďque est saturé. Cet acide possčde une chaîne carbonée comptant n =17 atomes de carbone. La chaîne est dite " saturée" si elle compte 2n+1 =17*2+1 =25 atomes d'hydrogčne. CH3-(CH2)16 : 3 + 16*2 = 35 atomes d'hydrogčne : l'acide octadécanoďque est donc saturé. Expliquer le sufixe " triol dans l'appellation propan-1, 2, 3-triol. "triol" signifie trois "ol " : le glycérol possčde trois fonctions alcool. Recopier et compléter l'équation de la réaction ci-dessous en indiquant la formule semi-développée du glycérol et en ajustant les nombres stoechiométriques.
A quelle famille chimique appartient la molécule organique A obtenue ?
Une solution pharmaceutique contient du diiode I2. Elle est utilisée comme antiseptique sur les plaies, les brűlures, les mycoses car le diiode est un oxydant qui agit en tuant les microorganismes par des réactions d'oxydoréduction. Cette solution commerciale de concentration c0 est trop concentrée pour ętre directement dosée. Il convient de la diluer 10 fois. On dose le diiode présent dans la solution diluée par des ions thiosulfate S2O32- contenus dans une solution de thiosulfate de sodium de concentration C( L'équation de la réaction est la suivante : I2 +2 On dose un volume V(I2) =10,0 mL. L'équivalence est obtenue pour un volume de solution de thiosulfate de sodium versé Véq =13,0 mL. Pour chaque question, indiquer si la proposition a), b), ou c) est exacte sachant qu'il n'y a qu'une seule bonne réponse par question. a) I2. Vrai. b) I-; c) Analyse : I2 + 2e- = 2I-. I2 gagne des électrons, il joue le rôle d'oxydant. a) capter un proton H+. b) capter un électron. a) I2 / b) I-/ Analyse : I2 + 2e- = 2I-. Le couple oxydant / réducteur est I2 / I-. On écrit l'oxydant le premier. S2O32- a) une perte d'électrons. b) un gain d'électrons. Analyse : 2S2O32- =S4O62- + 2e- . S2O32- perd des électrons, il s'oxyde. a) une éprouvette graduée. b) une pipette jaugée.
|
|||||||
| |
|||||||
|
|