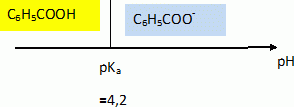|
Un conservateur alimentaire dans un soda : bac S Liban 2011. |
||||||||||||||||||||||
|
||||||||||||||||||||||
|
« Les conservateurs limitent, ralentissent ou stoppent la croissance des microorganismes (bactéries, levures, moisissures) présents ou susceptibles d’entrer dans l’aliment et préviennent donc l’altération des produits ou les intoxications alimentaires. L’acide benzoďque, par exemple, et ses sels de calcium, de sodium et de potassium sont utilisés comme antibactériens et antifongiques dans les denrées alimentaires ». D’aprčs le site www.eufic.org L’acide benzoďque est un conservateur qui figure dans de nombreuses boissons sans alcool, comme les sodas. Son code européen est E210. La formule de l’acide benzoďque est C6H5 – COOH ou encore 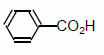 Données : - l’acide benzoďque est un solide blanc ŕ température ordinaire. - masse molaire de l’acide benzoďque : M = 122 g.mol-1. - pKa du couple acide benzoďque / ion benzoate : pKa (C6H5 – COOH / C6H5 – COO-) = 4,2
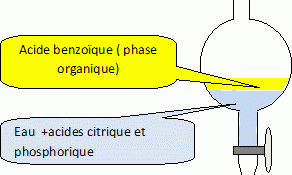
- le tolučne et l’eau ne sont pas miscibles. - l’acide phosphorique et l’acide citrique sont solubles dans l’eau. Extraction de l’acide benzoďque. On souhaite connaître la quantité d’acide benzoďque présente dans une boisson au cola en réalisant un titrage acido-basique. En dehors de l’acide benzoďque, la boisson contient également de l’acide phosphorique et de l’acide citrique, ainsi que de l’eau. Il s’agit donc, dans un premier temps, de séparer l’acide benzoďque, que l’on souhaite titrer, des autres acides. Dans un bécher on place un volume V = 100 mL de boisson et on laisse sous agitation magnétique pendant une heure afin d’éliminer le dioxyde de carbone dissous. On ajoute alors environ 100 mL de tolučne dans le bécher On verse ensuite le mélange dans une ampoule ŕ décanter.
On
élimine la phase aqueuse. On ajoute un excčs de solution aqueuse
d’hydroxyde de sodium dans l’ampoule ŕ décanter contenant la phase
organique puis on agite. Justifier l’apparition des cristaux blancs.
Préparation d’une solution d’acide benzoďque On désire connaître la quantité d’acide pur C6H5COOH présent dans les cristaux récupérés. Aprčs lavage et séchage, on pčse les cristaux ; leur masse est m = 0,38 g. On prépare alors une solution S0 par dissolution de la totalité des cristaux dans de l’eau distillée afin d’obtenir V0 = 250,0 mL de solution. Écrire l’équation de la réaction chimique entre l’acide benzoďque et l’eau. C6H5COOH aq + H2O(l) = C6H5COO-aq + H3O+aq. Exprimer la constante d’équilibre associée ŕ cette équation, puis la calculer. Ka = [C6H5COO-aq] [H3O+aq] / [C6H5COOH aq] = 10-4,2 =6,3 105.
En déduire la masse m0 d’acide pur correspondant. m0 = C0 M( acide benzoďque) =8,6 10-3 *122 =1,0492 ~1,0 g/L. Soit dans 250 mL : 1,0492 / 4 =0,2623 ~ 0,26 g. Déterminer le pourcentage d’acide benzoďque pur contenu dans les cristaux extraits de la boisson au cola. m0 / m*100 = 0,2623 / 0,38 *100 = 69 %. |
||||||||||||||||||||||
|
|