|
Spectroscopie : suivi cinťtique : bac S Liban 2011. |
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
|
…tude du fonctionnement d’un spectrophotomŤtre. Extrait d’une notice d’un spectrophotomŤtre : L’appareil comprend : - une source de lumiŤre polychromatique (lampe) qui ťmet un faisceau de lumiŤre en direction du monochromateur ; - un monochromateur (rťseau + fente) : le rťseau (systŤme dispersif) dťcompose la lumiŤre et dťvie les rayons suivant leur longueur d’onde (apparition des radiations colorťes de la lumiŤre). La fente (systŤme sťlectif) permet d’isoler une radiation lumineuse de longueur d’onde donnťe. Cette radiation est dirigťe vers la cuve contenant la solution ŗ analyser ; - une cuve (transparente aux radiations sťlectionnťes par le monochromateur) contenant la solution ŗ ťtudier ; - un photocapteur : c’est un ťlťment photosensible (en gťnťral une diode) qui transforme le signal lumineux en signal ťlectrique ; - un calculateur : il traite le signal ťlectrique pour calculer l’absorbance qui est proportionnelle ŗ l’intensitť du courant. …tude du rťseau. Le rťseau est un dispositif optique composť d’une sťrie de fentes parallŤles ou de rayures rťflťchissantes. Dans les deux cas, les traits sont espacťs d’une distance constante qu’on appelle le pas du rťseau. …tude d’une seule fente. On place perpendiculairement ŗ la fente un faisceau de lumiŤre monochromatique de longueur d’onde l. Le dispositif est schťmatisť ci- aprŤs : 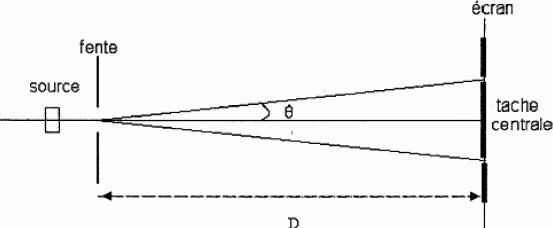 On observe sur l’ťcran, situť ŗ la distance D de la fente, la figure suivante : 
Lorsque les angles sont petits, on peut admettre que tan q ~ q (q en radian).
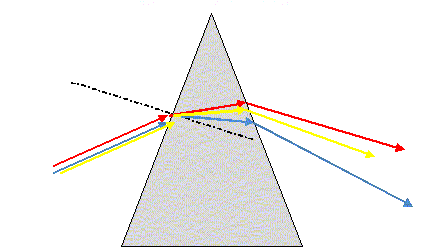
…tude du prisme. Un prisme permet ťgalement de dťcomposer la lumiŤre. Il est caractťrisť par son indice de rťfraction n. Dťfinir un milieu dispersif. Dans un milieu dispersif, la cťlťritť des ondes dťpend de leurs frťquences. On souhaite ťtudier la dťviation de rayons lumineux par un prisme de verre. Pour cela, on utilise deux radiations, l’une rouge de longueur d’onde lR = 750 nm, l’autre bleue de longueur d’onde lB = 460 nm. Les indices du verre pour ces deux radiations sont respectivement nR = 1,6 et nB = 1,7. L’indice de l’air nair est le mÍme pour toutes les radiations. Les deux radiations arrivent sur la face d’entrťe du prisme avec le mÍme angle d’incidence i1. Pour laquelle de ces deux radiations, l’angle de rťfraction dans le prisme est-il le plus grand ? On ne cherchera pas ŗ dťterminer la valeur des angles de rťfraction.
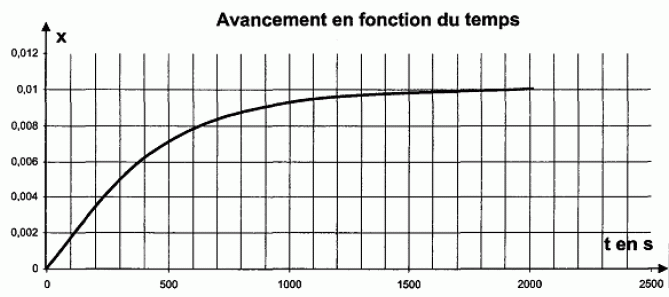
n air sin i1 = nR sin iR ; sin iR = n air sin i1 / nR ; nB > nR : donc sin iB > sin iR : le bleu sera le plus dťviť. Suivi cinťtique par spectrophotomťtrie d’une transformation chimique. On ťtudie la transformation des ions iodure par les ions peroxodisulfate, modťlisťe par la rťaction d’ťquation : S2O82-(aq) + 2 I-(aq) = 2 SO42-(aq) + I2(aq) Cette transformation est suivie ŗ l’aide du spectrophotomŤtre prťcťdemment ťtudiť, reliť ŗ un systŤme d’acquisition de donnťes. Le protocole est le suivant : On introduit dans la cuve du spectrophotomŤtre un volume V0 = 1,0 mL de solution aqueuse d’iodure de potassium (K+(aq) + I-(aq)) de concentration molaire en solutť apportť C0 = 2,0 10-2 mol.L-1. ņ t = 0 s, on ajoute V1 = 1,0 mL de solution aqueuse de peroxodisulfate de potassium (2K+(aq) + S2O82-(aq) ) de concentration molaire en solutť apportť C1 = 2,0 10-1 mol.L-1. On mťlange rapidement et on place la cuve dans le spectrophotomŤtre. Les mesures permettent de tracer la courbe ci-dessous donnant l’absorbance A du mťlange en fonction du temps t. 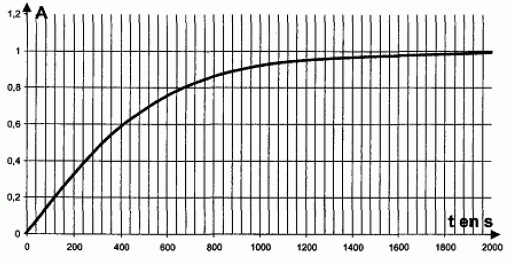
…tude de la vitesse volumique de rťaction. Dťfinir la vitesse volumique de rťaction vR. vR = 1/((V0+V1)) dx/dt. En prťcisant la mťthode utilisťe, dťcrire l’ťvolution de la vitesse volumique de rťaction au cours du temps. 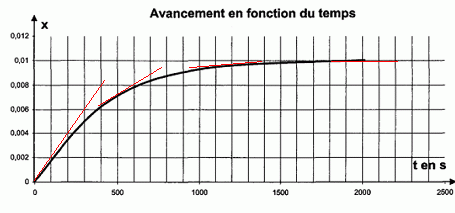 [dx/dt]t : coefficient directeur de la tangente ŗ la courbe ŗ la date t. Les tangentes sont de moins en moins inclinťes sur l'axe horizontal : [dx/dt]t diminue au cours du temps. VR est proportionnelle ŗ [dx/dt]t : VR diminue donc au cours du temps. Quel facteur explique cette ťvolution ? La concentration des rťactifs. Dťterminer le temps de demi-rťaction. 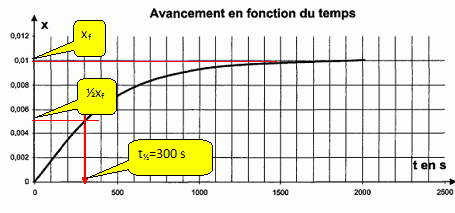 |
|||||||||||||||||||||||||||||||
|
|