Une
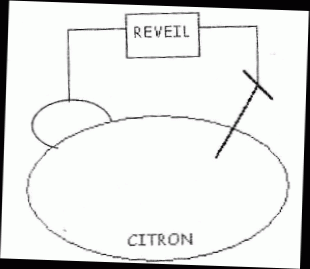
expťrience simple ŗ rťaliser pour ťpater la famille, consiste ŗ
alimenter un rťveil avec un citron !! Et oui ŗ l'aide d'une piŤce de
cuivre, d'un clou en zinc, de quelques fils ťlectriques et d'un citron,
on peut rťussir ŗ faire fonctionner un rťveil ou une calculatrice. Cet
exercice permet d'expliquer scientifiquement le phťnomŤne.
On donne : M(Zn) = 65,4 g/mol ; 1 F = 9,6 104 C / mol ; couples oxydant / rťducteur : Zn2+aq / Zn(s) ; H+aq / H2(g).
On
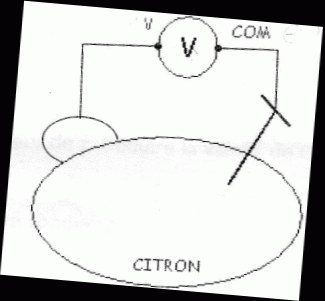
souhaite connaÓtre la force ťlectromotrice U de cette pile au citron.
Pour cela on branche un volmŤtre entre le clou et la piŤce. On mesure U
= 0,69 V
Dťterminer la polaritť de la pile au citron. Justifier.
U
est positive, donc le cuivre est la borne positive reliťe ŗ "V" du
volmŤtre ; le zinc est la borne nťgative de la pile, reliťe ŗ la
borne "COM" du voltmŤtre.
Au cours de son utilisation on constate une effervescence au niveau de
la piŤce. AprŤs analyse du gaz, on en dťduit qu'il s'agit de
dihydrogŤne.
Dťcrire simplement une expťrience permettant de mettre en ťvidence la nature du gaz ťmis.
Le
mťlange dihydrogŤne - air ( dioxygŤne ) est explosif en toutes
proportions. Approcher une flamme ( allumette) du gaz qui se dťgage :
on entend une petite explosion.
Donner les demi-ťquations des rťactions ayant lieu ŗ chaque ťlectrode. Prťciser le type de rťaction ( oxydation ou rťduction ). Quels noms donnent-on aux ťlectrodes ?
Oxydation du zinc ŗ l'anode nťgative : Zn(s) = Zn2+aq + 2e-.
Rťduction de H+aq ŗ la cathode positive : 2 H+aq + 2e- = H2(g).
Ecrire la rťaction globale de la rťaction se produisant au cours du fonctionnement de la pile.
Zn(s) +2 H+aq = Zn2+aq + H2(g).
D'oý proviennent les ions H+aq ?
Le jus de citron contient plusieurs acides. Ces derniers sont plus ou moins ionisťs , d'oý la prťsence des ions H+aq.
La
pile est utilisťe pour faire fonctionner une petite calculatrice
pendant 1 min 36 s. L'intensitť du courant dťbitť est ťgale ŗ 10 mA..
Quelle quantitť d'ťlectricitť est dťbitťe par la pile ?
Q = I t avec I = 0,010 A et t = 60 +36 = 96 s.
Q = 0,010 *96 = 0,96 C.
Dresser le tableau d'avncement pour la rťaction qui a lieu au niveau du clou.
|
avancement (mol)
|
Zn(s)
|
=Zn2+aq |
+ 2e- |
initial
|
0
|
n
|
0
|
0
|
en cours
|
x
|
n-x
|
x
|
2x
|
final
|
xmax
|
n-xmax |
xmax |
2xmax |
|
Calculer la quantitť de matiŤre de zinc consommťe. En dťduire la variation de masse Dm du clou.
Quantitť de matiŤre d'ťlectron : n(e-)= Q / 9,6 104 = 0,96 / 9,6 104 =1,0 10-5 mol.
Quantitť de matiŤre de zinc consommť : n(Zn) =Ĺ n(e-)= 5,0 10-6 mol.
Masse de zinc consommťe : Dm = -n(Zn) m(Zn) = -5,0 10-6 *65,4 = 3,3 10-4 g.
Le clou a ťtť pesť avant la fabrication de la pile : m i = 26,2 g
Peut-on vťrifier expťrimentalement la valeur de Dm ?
La prťcision de la balance utilisťe est le dťcigramme. On ne peut donc pas vťrifier, avec cet instrument, la valeur de Dm. Pour cela, il faudrait une balance beaucoup plus prťcise.
|
|