ModŤle de Rutherford de l'atome d'hydrogŤne.
- propose un mouvement circulaire uniforme du noyau autour de l'ťlectron. Faux.
" L'ťlectron gravite autour du noyau avec une vitesse uniforme en dťcrivant une
orbite circulaire".
- calcule une ťnergie quantifiťe. Faux.
- calcule une ťnergie inversement proportionnelle ŗ la distance noyau-ťlectron. Vrai.
- justifie les niveaux d'ťnergie discrets. Faux.
Polaritťs des liaisons.
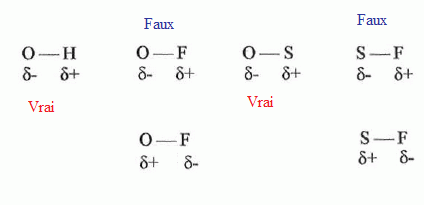
Le fluor est le plus ťlectronťgatif des ťlťments.
|
Acide, base forts ou faible.
L'acide propanoÔque C2H5-COOH est faible ; l'acide perchlorique HClO4 est fort ; l'ťthanol C2H5-OH est un "acide" spectateur dans l'eau.
C2H5-COO- est une base forte. Faux.
HO- est une base forte ; le pKa du couple acide base H2O/HO- vaut 14 ŗ 25įC.
ClO4- est une base faible. Faux.
ClO4-est une "base" spectateur dans l'eau.
C2H5-O- est une base forte. Vrai.
|
Avancement final xf.
0,05 mole de pentachlorure de phosphore PCl5(g) est en ťquilibre avec 0,09 mole de trichlorure de phosphore PCl3(g) et 0,05 mole de dichlore Cl2(g) ŗ une tempťrature donnťe.
On augmente la tempťrature et on ajoute 0,04 mole de PCl5(g) et 0,05 mole de Cl2(g).
Lorsque l'ťquilibre est rťtabli, une valeur possible de l'avancement final xf de la dťcomposition de PCl5(g) en PCl3(g) et Cl2(g) est :
+0,08 ; -0,15 ; -0,08 ; +0,1.
L'avancement d'une rťaction est un nombre positif : -0,15 et -0,08 sont donc exclus.
L'avancement final ne peut pas Ítre supťrieur ŗ l'avancement maximal, quantitť de matiŤre du rťactif limitant.
On dťfinit l'ťtat initial de la maniŤre suivante : PCl5(g) : 0,09 mole ; PCl3(g) : 0,09 mole ; Cl2(g) : 0,10 mole avant augmentation de tempťrature.
dans l'hypothŤse d'une ťvolution dans le sens direct, PCl5(g) est le rťactif limitant ; dans l'hypothŤse d'une ťvolution en sens indirect, PCl3(g) est le rťactif limitant.
xf ne peut donc pas Ítre supťrieur ŗ 0,09 mol.
Travail des forces de pression.
On note P la pression du systŤme et dV la variation ťlťmentaire du volume du systŤme, -PdV est l'expression :
- du travail des forces de pression pour une transformation ťlťmentaire. Faux.
dW = -Pextťrieure dV.
- du travail net. Faux.
- du travail des forces de pression pour une transformation irrťversible ťlťmentaire. Faux.
- du travail des forces de pression pour une transformation rťversible ťlťmentaire. Vrai.
dans ce cas la pression P du systŤme est ŗ chaque instant ťgale ŗ la pression extťrieure.
Elťments soufre et oxygŤne.
Les ťlťments S et O appartiennent ŗ la mÍme famille. La molťcule H2O est plus lťgŤre que la molťcule H2S, sulfure d'hydrogŤne : pourtant H2S est un gaz ŗ tempťrature ambiante alors que H2O est un liquide.
- ceci explique que les interactions de Van der Walls sont plus fortes dans le sulfure d'hydrogŤne que dans l'eau. Faux.
- ceci s'explique par des liaisons hydrogŤne intermolťculaires. Vrai.
- la tempťrature d'ťbullition de l'eau est plus ťlevťe que celle du sulfure d'hydrogŤne. Vrai.
- la tempťrature de fusion de l'eau est plus faible que celle du sulfure d'hydrogŤne. Faux.
Liaisons hydrogŤne.
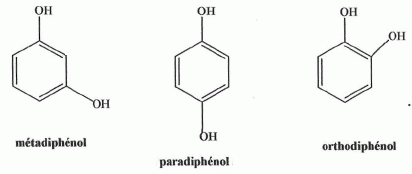
- Le paradiphťnol admet une tempťrature d'ťbullition plus ťlevťe que l'orthodiphťnol. Vrai.
- L'orthodiphťnol rťalise des liaisons hydrogŤne intramolťculaires. Vrai.
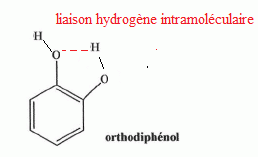
Dans l'orthodiphťnol il y a
moins de possibilitť de liaisons hydrogŤne entre molťcules : la
tempťrature d'ťbullition de l'orthodiphťnol est donc plus faible que
celle du paradiphťnol.
- Le paradiphťnol rťalise des liaisons hydrogŤne intramolťculaires. Faux.
- Le mťtadiphťnol rťalise des liaisons hydrogŤne intramolťculaires. Faux.
Variation d'entropie.
- est nulle au zťro absolu. Vrai.
ŗ 0 K, tous les corps purs sont cristallisťs et parfaitement ordonnťs : leur entropie est nulle.
- est calculable dŤs que l'on se donne une transformation rťversible de l'ťtat initial ŗ l'ťtat final. Vrai.
L'entropie est une fonction
d'ťtat. Sa variation ne dťpend que de l'ťtat final et de l'ťtat
initial, peu importe le chemin suivi. On peut donc imaginer une
transformation rťversible pour laquelle le calcul de la variation
d'entropie est facile.
- est toujours positive. Faux.
la variation d'entropie d'un systŤme thermodynamique est positive ou nulle.
- est ťgale ŗ la chaleur reÁue que multiplie la tempťrature. Faux.
dS = dQrťv / T .
Ion cobalt (III).
Combien d'ťlectron cťlibataire comporte l'ion Co3+ dans son ťtat fondamental ? On done 27Co. ( 1 ; 2 ; 3 ; 4 ).
Co3+ : 1s2
2s2 2p6 3s2 3p6
3d6 .
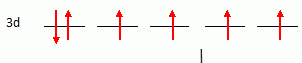
Configuration ťlectronique.
La configuration ťlectronique suivante de l'oxygŤne O :
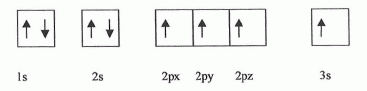
- viole le principe de stabilitť de Klechkovsky. Vrai.
Dans l'ťtat fondamental, le remplissage des orbitales par les ťlectrons va
s'effectuer par valeurs croissantes de : n + l. Lorsque n + l est le
mÍme pour deux orbitales, celle qui a la plus petite valeur de n est remplie la
premiŤre.
- viole le principe de Pauli. Faux.
Le nombre maximal d'ťlectrons pouvant appartenir ŗ une couche caractťrisťe par
le nombre quantique n est 2n2. Deux ťlectrons ne peuvent jamais exister dans le mÍme
ťtat quantique c'est ŗ dire avoir leurs quatre nombres quantiques :
n, l, m et s identiques
- est l'ťtat fondamental. Faux.
ťtat fondamental 1s2
2s2 2p4
- viole la rŤgle de Hund. Faux.
Dans
l'ťtat fondamental, lorsque plusieurs orbitales atomiques sont
dťgťnťrťes, les ťlectrons occupent d'abord le maximum d'orbitales
possibles et ils prennent des spins identiques.
|
Constante d'ťquilibre.
La rťaction ťquilibrťe d'ťquation : C(s) + O2(g) = CO2(g) de variation d'enthalpie libre standard DrGį, ŗ la tempťrature T, pi ťtant la pression partielle du constituant i, admet comme constante d'ťquilibre :

Pile.
Soit la pile : Pt(s) |Sn4+//Sn2+ ||Ag+ |Ag(s).
Eį(Ag+ |Ag(s)) = 0,80 V ; Eį( Sn4+/ Sn2+) = 0,151 V ŗ 298 K.
DrGį
: enthalpie libre standard de la rťaction chimique spontanťe
associťe ŗ la pile. Les coefficients de l'ťquation sont des
nombres entiers les plus petits possibles.
- Dans les conditions standard, la rťaction spontanťe provoque une diminution de la concentration en ion Ag+. Vrai.
Sn2+, rťducteur le plus fort s'oxyde : Sn2+ = Sn4++ 2e-.
Ag+ , oxydant le plus fort se rťduit : 2Ag+ +2e-= 2 Ag(s).
- Dans les conditions standard, la rťaction spontanťe provoque une augmentation de la concentration en ion Ag+. Faux.
DrGį = 2 *96500*(0,80-0,151) en joules/mole. Faux.
La rťaction ťtant spontanťe, DrGį est nťgative : DrGį = -2 *96500*(0,80-0,151) en joules/mole.
Acide phosphorique.
L'acide phosphorique est un triacide faible.
- La constante d'aciditť Ka du couple HPO42- / PO43- est supťrieure ŗ celle du couple H2PO4- /HPO42- . Faux.
Ce serait vrai dans le cas des pKa.
Si les constantes d'aciditť associťes ŗ H3PO4 sont : Ka1 > Ka2 > Ka3.
- le pH d'une solution de dihydrogťnophosphate de sodium H2PO4- +Na+ est :
pH = ĹpKa2 + ĹpKa3. Faux.
couples acide base : H3PO4 /H2PO4- : pKa1 ; H2PO4- / HPO42- : pKa2 ;
pH = ĹpKa1 + ĹpKa2.
- le pH d'une solution de phosphate de sodium ( PO43- + 3Na+ ) de concentration molaire c est : pH = ĹpKa3-Ĺlog c. Faux.
Formule approchťe dans le cas d'une base faible : pH = Ĺ(14 +pKa3+log c).
- L'acide H3PO4 est plus fort que l'acide H2PO4- (si on ne considŤre que ces propriťtťs acides). Vrai.
H3PO4 /H2PO4- : pKa1 ; H2PO4- / HPO42- : pKa2 ;
Ka1 > Ka2 donc pKa1 < pKa2 ; ŗ concentration ťgale, l'acide le plus fort a le plus petit pKa.
|





