|
Datation au carbone 14 : concours manipulateur radio St Germain 2010. |
|||||||
|
|||||||
|
Dans la haute atmosphŤre, soumis au rayonnement cosmique galactique constituť de protons, des neutrons secondaires interagissent avec les noyaux d'azote 14. Cette rťaction forme un isotope AZX du carbone : le fameux carbone 14. Immťdiatement formť le carbone 14 s'oxyde en se combinant avec l'oxygŤne pour former du dioxyde de carbone qui se mťlange avec le reste de l'atmosphŤre. Or le carbone 14 est radioactif. La teneur en carbone 14 est constante dans le monde ( dans l'atmosphŤre comme dans chaque organisme vivant ). Cela est du ŗ un ťquilibre entre la dťsintťgration et la production de carbone 14. Chaque gramme de carbone contient des atomes de carbone 14. On enregistre en moyenne 13,5 dťsintťgrations par minute et par gramme de carbone. Lorsqu'un arbre, par exemple, est abattu, le bois cesse de vivre, le processus de photosynthŤse s'arrÍte et il n'y a plus d'absorption de dioxyde de carbone. Le carbone 14 est alors libre de se dťsintťgrer sans compensation. On peut donc dater l'‚ge de la mort de l'organisme ( au moment oý cesse tout ťchange de CO2 avec l'atmosphŤre). Dans la haute atmosphŤre la rťaction qui a lieu entre le neutron et le noyau d'azote 14 s'ťcrit : 147N + 10n---> 146C + AZX. Enoncer les lois de conservation et identifier la particule X. Conservation du nombre de nuclťons : 14+1 = 14 +A d'oý A = 1. Conservation de la charge : 7+0 = 6+Z d'oý Z = 1 (ťlťment hydrogŤne) AZXest un proton 11H. 147N + 10n---> 146C +11H.
Un noyau radioactif est un noyau instable dont la
dťsintťgration (destruction) alťatoire
s'accompagne: Sachant que le carbone 14 prťsente une radioactivitť de type Ŗ-, ťcrire l'ťquation traduisant sa dťsintťgration.
On rappelle ťgalement la loi de dťcroissance radioactive. 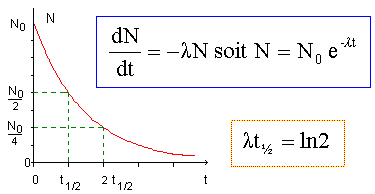 l est la constante radioactive, caractťristique d'un radioťlťment. Elle s'exprimera ici en an-1.
|
|||||||
| |
|||||||
|
|