|
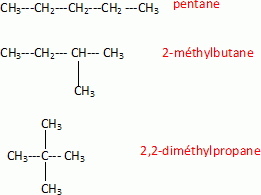
Polution au dioxyde de soufre, combustibles propres, concours technicien de l'industrie et des mines 2009. |
|||||||
|
|||||||
|
Une centrale thermique brule un charbon dont la teneur en soufre est de 1,0%. La consommation horaire en charbon est de 206 tonnes. Ecrire l'ťquation de la rťaction de combustion complŤte du soufre S dans le dioxygŤne. S(s) + O2(g) = SO2(g) Calculer la masse puis la quantitť de matiŤre ( moles) de soufre brulť en une heure. masse m = 206*0,01 = 2,06 t = 2,06 106 g. Masse molaire du soufre : M = 32 g/mol Quantitť de matiŤre de soufre n = m / M = 2,06 106 /32 =6,4375 104 ~ 6,4 104 mol. Dťterminer la quantitť de matiŤre de dioxyde de soufre formť en une heure. D'aprŤs les nombres stoechiomťtriques de l'ťquation , il se forme une mole de SO2 pour une mole de soufre brŻlť. n(SO2) = 6,4 104 mol.
Pour
lutter contre la pollution atmosphťrique par le dioxyde de soufre, on
mťlange le charbon avec du calcaire ou carbonate de calcium CaCO3 pulvťrisť avant de le faire brŻler. L'ťquation de la rťaction s'ťcrit : Combustibles propres. la production de dioxyde de carbone lors de la combustion
complŤte d'hydrocarbures accroÔt l'effet de serre. Par consťquent, dans
le choix d'un combustible, l'ťnergie de rťaction libťrťe par mole de
dioxyde de carbone formť est un critŤre intťressant.
L'ťquation de combustion du mťthane s'ťcrit : CH4 + 2O2 = CO2 + 2H2O. 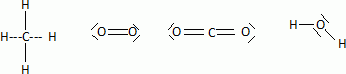 faire le bilan des liaisons rompues et des liaisons crťťes
|
|||||||
| |
|||||||
|
|