Acide formique.
L'acide formique est soluble dans l'eau ; sa formule semi-dťveloppťe
est HCOOH.
Cet exercice propose l'ťtude de quelques propriťtťs de la solution
aqueuse d'acide formique.
C : 12,0 ; H : 1,00 ; O : 16,0 g/mol ; constante d'aciditť Ka
( HCOOH / HCOO-) = 1,80 10-4 ;
lH3O+ = 35,0
mS m2 mol-1 ; lHCOO- = 5,46 mS m2
mol-1.
Quel est le nom de
l'acide formique dans la nomenclature officielle ?
Acide mťthanoÔque.
On intoduit une masse m d'acide formique dans une fiole jaugťe de
volume V = 100 mL ; on complŤte jusqu'au trait de jauge avec de l'eau
distillťe et on homogťnťise. On obttient une solution S de
concentration C = 1,00 10-2 mol/L.
Calculer
la masse m.
M= 2+12+32 =46,0 g/mol ; n= CV = 1,00 10-2 *0,100 = 1,00 10-3
mol ; m = n M = 1,00 10-3 *46,0 = 46,0 mg.
Ecrire
l'ťquation de la rťaction de l'acide formique avec l'eau.
HCOOH aq +H2O(l) = H3O+ aq
+ HCOO-aq.
Etablir
le tableau d'avancement relatif ŗ cette rťaction.
|
avancement
(mol)
|
HCOOH aq |
+H2O(l)
|
= H3O+
aq |
+ HCOO-aq |
initial
|
0
|
CV = 10-3
mol
|
solvant
|
0
|
0
|
en
cours
|
x
|
10-3
-x
|
en
|
x
|
x
|
final
( si ťquilibre)
|
xf
|
10-3
-xf |
large
excŤs
|
xf |
xf |
final
( si rťaction totale)
|
xmax
|
10-3
-xmax=0
|
|
xmax |
xmax |
Exprimer
le taux d'avancement final t en fonction de [H3O+ aq]ťq et de C.
t =xf / xmax
= [H3O+ aq]ťq / C.
|
Donner l'expression
du quotient de rťaction ŗ l'ťquilibre en fonction de [H3O+ aq]ťq et de C.
Q
r ťq = [H3O+
aq]ťq[HCOO- aq]ťq / [HCOOH aq]ťq
La solution est ťlectriquement neutre : [H3O+ aq]ťq= [HCOO- aq]ťq ;
Conservation de l'ťlťment carbone : C = [HCOO- aq]ťq + [HCOO- aq]ťq ;
Q r ťq =
[H3O+ aq]ťq2
/ ( C-[H3O+ aq]ťq).
|
Exprimer la
conductivitť s de la
solution d'acide formique ŗ l'ťtat d'ťquilibre en fonction des
conductivitťs molaires ioniques et de la concentration des ions oxonium
ŗ l'ťquilibre.
s = lH3O+ [H3O+ aq]ťq +lHCOO- [HCOO- aq]ťq = (lH3O+ + lHCOO-)[H3O+ aq]ťq.
La mesure de la
conductivitť de la solution d'acide formique donne s = 5,00 10-2 S m-1.
Calculer [H3O+
aq]ťq, t et Q r ťq .
[H3O+ aq]ťq = s / (lH3O+ + lHCOO-) = 5,00 10-2 / ((35,0 + 5,46) 10-3)
= 1,236 mol m-3 = 1,24 10-3
mol L-1.
t = 1,24 10-3 / 1,00 10-2 =0,124.
Q r ťq =
(1,24
10-3)2/(0,01-1,24 10-3) =1,76 10-4.
Comparer
la valeur de Q r ťq avec la valeur de
la constante Ka du couple HCOOH /
HCOO-.
Ces deux valeurs sont pratiquement identiques, l'ťcart relatif est :
(1,80-1,76) / 1,78 = 2,2 10-2 ( 2,2 %).
Quelle
est l'influence de la concentration de la solution sur le taux
d'avancement et sur le quotient de rťaction Q r ťq ?
Q r ťq =
Ka, il ne dťpend que de la tempťrature.
t =xf / xmax
= [H3O+ aq]ťq / C.
Si la concentration diminue, le taux d'avancement augmente.
SynthŤse de
l'aspirine.
En 1825 un pharmacien italien, Francesco Fontana isole le
"principe actif" de l'ťcorce de saule et le baptise salicine. Par la
suite la salicine donnera de l'acide salicylique, plus efficace, puis
un procťdť de synthŤse ŗ partir de l'acide salicylique produira l'acide
acťthylsalicylique. C'est la naissance de l'aspirine mise sur le marchť
en 1899.
Donnťes :
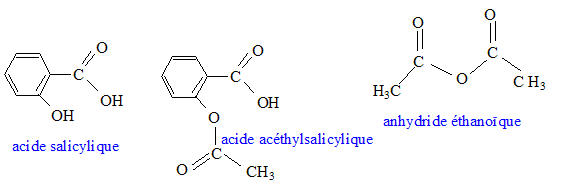
Masse molaire ( g/mol) : acide salicylique : 138,0 ; anhydride
ťthanoÔque : 102,0 ; acide acťthylsalicylique : 180,0.
Masse volumique de l'anhydride ťthanoÔque
r =1,08 g mL-1.
pKa du couple acide acťthylsalicylique / ion
acťthylsalicylate : 3,5 ŗ la tempťrature de l'expťrience.
L'acide acťthylsalicylique est trŤs peu soluble dans l'eau.
Entourer chaque groupe fonctionnel et le nommer.
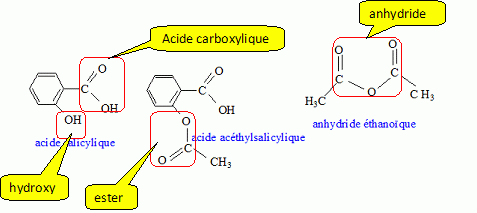
SynthŤse de l'aspirine au laboratoire.
Dans toute cette partie, on notera R-OH la formule de l'acide salicylique.
Lors d'une sťance de TP, un groupe d'ťlŤves propsoe de prťparer
l'aspirine en faisant rťagir l'acide salicylique sur l'acide ťthanoÔque
( acťtique).
Ecrire l'ťquation de la rťaction. De quel type de rťaction s'agit-il ?
R-OH + CH3-COOH = CH3-COOR + H2O, estťrification.
Pourquoi l'avancement maximal ne peut Ítre atteint avec ces deux rťactifs ?
L'estťrification est limitťe par l'hydrolyse de l'ester.
Citer un moyen pour augmenter l'avancement final, en conservant ces deux rťactifs.
Mettre l'un des rťactifs en excŤs, ou ťliminer par distillation l'un des produits au fur et ŗ mesure qu'il se forme.
|
AprŤs discussion, ce groupe dťcide de remplacer l'acide ťthanoÔque par l'anhydride ťthanoÔque.
Quel est l'intťrÍt de ce changement ?
Le milieu est anhydre, il n'y a pas d'hydrolyse de l'ester : la rťaction est totale.
Ecrire l'ťquation de la synthŤse de l'aspirine ŗ partir de l'acide salicylique et l'anhydride ťthanoÔque.
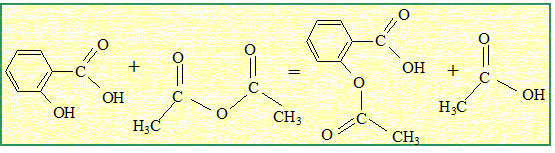 Dans
un ballon bien sec, ce groupe d'ťlŤves introduit : 13,8 g d'acide
salicylique en poudre, 25,0 mL d'anhydride ťthanoÔque liquide et 10
gouttes d'acide sulfurique concentrť. Ils adaptent au ballon un
rťfrigťrant ŗ boules et chauffent pendant 15 minutes. AprŤs
refroidissement, ils filtrent, rincent et sŤchent les cristaux obtenus
: la masse de cristaux est 12,0 g. Dans
un ballon bien sec, ce groupe d'ťlŤves introduit : 13,8 g d'acide
salicylique en poudre, 25,0 mL d'anhydride ťthanoÔque liquide et 10
gouttes d'acide sulfurique concentrť. Ils adaptent au ballon un
rťfrigťrant ŗ boules et chauffent pendant 15 minutes. AprŤs
refroidissement, ils filtrent, rincent et sŤchent les cristaux obtenus
: la masse de cristaux est 12,0 g.
Donner le nom et la formule chimique des ions apportťs par l'acide sulfurique. Quel est le rŰle du cation ?
H3O+ : oxonium ; HSO4- : hydrogťnosulfate ; SO42- : sulfate.
L'ion oxonium joue le rŰle de catalyseur.
Calculer la quantitť initiale de chaque rťactif et vťrifier que l'acide salicylique est le rťactif limitant.
n (acide salicylique) = m / M = 13,8 / 138 = 0,100 mol.
n( anhydride) = 25,0*1,08 / 102,0 = 0,265 mol ( donc en excŤs)
Dťfinir le rendement puis le calculer.
rendement = masse expťrimentale d'ester / masse thťorique.
On peut obtenir au mieux 0,100 mol d'ester soit 0,100 *180,0 = 18,0 g.
rendement = 12,0 / 18,0 = 0,667.
Pour terminer, ce groupe d'ťlŤves dissout totalement les 12,0 g de
cristaux dans de l'eau distillťe pour obtenir une solution S. Il dose
ensuite trŤs prťcisťment l'acide acťthylsalicylique contenu dans cette
solution par une solution titrante de soude. AprŤs calcul, ils montrent
que la solution S contient 6,20 10-2 mol d'acide acťthylsalicylique.
Que pouvez-vous en conclure concernant les cristaux ? Justifier par un calcul simple.
Si les cristaux sont purs, ils contiennent 12 / 180 = 6,66 10-2 mol d'acide acťthylsalicylique..
La solution S contient seulement 6,20 10-2 mol d'acide acťthylsalicylique : les cristaux ne sont donc pas purs.
|
|
|
|


