Prťparation
d'une solution de permanganate de potassium pour doser une
solution de fer (II).
La prťparation d'un volume de solution titrťe ŗ partir d'une substance
commerciale s'effectue en quatre phases :
- prťparation d'une solution trop riche, c'est ŗ dire de concentration
molaire lťgŤrement supťrieure ŗ la concentration demandťe
- ťtalonnage de cette solution trop riche
- ajustage de la concentration dťsirťe par dillution
- dosage de contrŰle.
Pour rťagir le permanganate a besoin d'Ítre en milieu acide sulfurique.
On prťparera d'abord un volume V' = 500,0 mL de solution environ 2
mol/L en acide sulfurique.
Sur la solution commerciale, on peut lire : H2SO4,
M~98,10 g/mol, puretť ou titre massique 96 %, densitť d = 1,83.
Quelles sont les
prťcautions ŗ prendre lors de l'utilisation de solution d'acide
sulfurique concentrťe ?
Port de blouse, gants et
lunettes de sťcuritť et travail sous hotte aspirante.
Calculer la
concentration en acide sulfurique de la solution commerciale.
Masse de 1 L : 1,83 kg = 1,83 103 g. Dans 1 L, masse d'acide
pur : 0,96 * 1,83 103 =1,7568 103 g.
Concentration en acide sulfurique : 1,7568 103 / 98,1 = 17,9
~18 mol/L.
Quel est
le volume d'acide sulfurique commerciale que l'on doit prťlever pour
prťparer 200 mL ?
Facteur de dilution F = concentration commerciale / concentration de la
solution fille diluťe
F = 18/2 = 9.
Volume de solution commerciale ŗ prťlever = volume de la solution fille
diluťe / F = 200 / 9 ~22 mL.
|
Quelle est la masse
de permanganate de potassium solide que l'on doit peser pour prťparer
200 mL d'une solution de concentration molaire exactement 0,050 mol/L ?
M(KMnO4) = 39,1 + 54,9 +4*16 =158 g/mol
Quantitť de matiŤre KMnO4 =
volume ( L) fois concentration (mol/L)
n = 0,200*0,050 =0,010 mol
masse (g) = masse molaire ( g/mol) * quantitť de matiŤre (mol)
n = 158 *0,010 = 1,58 ~1,6 g.
|
On dose
la solution de permanganate de potassium par pesťe d'oxalate de sodium
Na2C2O4 en milieu acide sulfurique.
Ecrire la
demi ťquation correspondant au couple MnO4-aq / Mn2+aq.
2 fois
{ MnO4-aq + 8H+aq + 5e-
= Mn2+aq +4H2O }.
Ecrire la demi
ťquation correspondant au couple CO2 aq / C2O4-aq.
5 fois
{C2O42-aq
=2 CO2 aq + 2e-}.
Ecrire
l'ťquation de la rťaction du permanganate sur l'oxalate.
2MnO4-aq +
16H+aq +5C2O42-aq
= 10 CO2 aq + 2Mn2+aq +8H2O.
Ecrire la
relation du dosage ŗ l'ťquivalence. En dťduire la masse d'oxalate de
sodium ( M= 134,0 g/mol) pour avoir une chute de burette de 10 mL ŗ 20
mL.
A l'ťquivalence, les quantitťs de matiŤre des rťactifs sont en
proportions stoechiomťtriques : n(C2O42-) =2,5 n(MnO4-).
Volume de solution titrante 15 mL ( compris entre 10 et 20 mL)
(MnO4-) = 0,015*0,050 =7,5 10-4
mol ; n(C2O42-) =2,5*7,5 10-4 =1,875 10-3 mol.
m = n(C2O42-) M = 1,875 10-3*134 =0,2513 ~0,25 g.
On procŤde enfin au dosage de la
solution S de fer (II) par la solution de permanganate.
Ecrire l'ťquation de
ce dosage.
MnO4-aq +
8H+aq + 5e- = Mn2+aq +4H2O
5 Fe2+aq = 5 Fe3+aq + 5e-.
MnO4-aq +
8H+aq +5 Fe2+aq = 5 Fe3+aq
+Mn2+aq +4H2O.
Donner la
relation ŗ l'ťquivalence et en dťduire l'expression littťrale de CFe en fonction de CMnO4- de la chute de la
burette ve et de la prise
d'essai E de la solution S.
A l'ťquivalence, les quantitťs de matiŤre des rťactifs sont en
proportions stoechiomťtriques : n(Fe2+) =5 n(MnO4-).
CFe E =5 CMnO4- ve ; CFe =5 CMnO4- ve / E.
Prťparations de
solutions tampon.
Vous avez
ŗ votre disposition les solutions suivantes :
- acide acťtique ŗ environ 0,2 mol/L ; CH3COONa en solution ŗ 0,2
mol/L
KH2PO4 solide ( M = 136 g/mol) ; Na2HPO4 en
solution ŗ 0,2 mol/L ; solution de NH4Cl ŗ environ 0,2 mol/L.
Solution d'acide chlorhydrique ŗ 0,1 mol/L et ŗ 0,2 mol/L.
Solution de soude ŗ 0,1 mol/L et ŗ 0,2
mol/L.
Solution d'ammoniac ŗ 1 mol/L.
Les caractťristiques des couples acido-basiques sont donnťes :
H3PO4 / H2PO4-
: pKa1 = 2,1 ; H2PO4-
/ HPO42- : pKa2 =
7,2 ; HPO42-
/ PO43- : pKa3 =
12,4 ;
NH4+ / NH3 : pKa =
9,25 ; CH3COOH / CH3COO- : pKa
= 4,75.
Comment
prťparer rapidement et simplement une solution tampon de pH voisin de 9
?
La solution prťparťe ne sera pas trop diluťe et son volume sera compris
entre 50 et 100 mL environ.
NH4+
/ NH3 : pKa = 9,25 ; les quantitťs de matiŤre
d'ion ammonium et d'ammoniac doivent Ítre ŗ peu prŤs identiques.
50 mL de solution
de NH4Cl ŗ environ 0,2 mol/L : n(NH4+) =50*0,2 =10 mmol.
10
mL de solution d'ammoniac ŗ 1 mol/L : n(NH3) = 10 * 1 =10 mmol.
Comment
pourrait-on opťrer pour ajuster la valeur de ce tampon ŗ 10 ?
pH = 9,25 + log ( [NH3]
/ [NH4+]
).
En ajoutant de la solution d'ammoniac ŗ 1 mol/L, le pH va croÓtre
lentement.
Titrage
d'une solution contenant du chlorure de sodium ( Na+
+ Cl-) ŗ environ 0,4
mol/L et de l'acide chlorhydrique ( H3O+ +
Cl-) ŗ environ 0,1
mol/L.
On dispose de la verrerie de laboratoire usuelle ainsi que du matťriel
physico-chimique suivant : pHmŤtre, conductimŤtre, millivoltmŤtre,
ťlectrodes.
Les solutions qui sont ŗ votre disposition sont les suivantes :
hydroxyde de sodium ŗ 0,200 mol/L et solution de nitrate d'argent ŗ
0,050 mol/L
Donner le
protocole du titrage pour dťterminer le titre exact en acide
chlorhydrique et en chlorure de sodium.
Titrage acide base avec suivi pHmťtrique pour dťterminer le titre en
acide chlorhydrique.
H3O+aq + HO- aq = 2H2O.
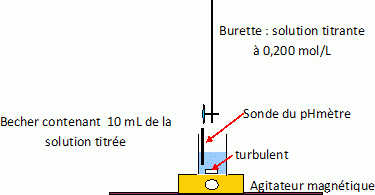
Tracer la courbe pH= f( volume ajoutť ) pour dťterminer l'ťquivalence.
A l'ťquivalence Cacide = 0,200 Vajoutť ŗ l'ťquivalence
/ 10.
|
Titrage par prťcipitation avec suivi
conductimťtrique pour dťterminer le titre total en ion chlorure.
Ag+aq + Cl- aq = AgCl(s).
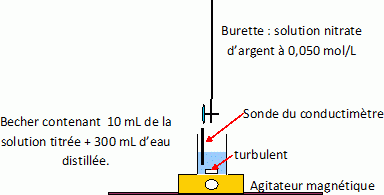
Tracer
la courbe conductivitť = f( volume ajoutť ). Cette courbe est
constituťe de deux segments de droites ; leur intersection donne le
volume ťquivalent Vťqui.
Cchlorure totale = 0,050 Vajoutť ŗ l'ťquivalence / 10.
Cchlorure de sodium = Cchlorure
totale - Cacide.
|
|
|
|

