Optique.
D'un point de vue optique un microscope est constituť essentiellement
d'un objectif et d'un oculaire que l'on assimilera chacun ŗ une
lentille .
A. l'objectif est une
lentille convergente. Vrai.
B. l'oculaire est une lentille convergente. Vrai.
C. Lors de la mise au
point, on modifie la distance entre l'objectif et l'oculaire. Faux.
On modifie la distance
objectif-objet gr‚ce ŗ une
crťmaillŤre.
D. On peut modifier le
grossissement du microscope en changeant d'objectif. Vrai.
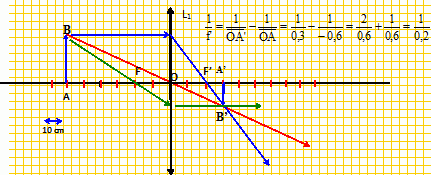
Un objet pacť ŗ 60 cm en avant d'une lentille
convergente de centre optique O et de distance focale f' inconnue a son
image A'B' de l'autre cŰtť de la lentille ŗ 30 cm de son centre optique.
La distance focale ( en cm) de la lentille vaut ( 20 ; 30 ; 60 ; 90 )
|
En plus du matťriel classique de connexion (
fils, interrupteur...) choisir parmi les
lots de matťriels suivants celui ou ceux qui permettent) d'ťtudier la
dťcharge oscillante d'un condensateur dans une bobine.
A. un condensateur,
une bobine, un conducteur ohmique, un gťnťrateur basse frťquence, un
oscilloscope numťrique.
B. un
condensateur, une bobine, un conducteur ohmique, un gťnťrateur basse
frťquence, un oscilloscope analogique.
C.
un condensateur, une bobine, un conducteur ohmique, une alimentation
stabilisťe, un oscilloscope analogique.
D.
un condensateur, une bobine, un conducteur ohmique, une alimentation stabilisťe, un oscilloscope numťrique.
E.
un condensateur, une bobine, un conducteur ohmique, une alimentation stabilisťe, un systŤme d'acquisition de donnťes reliť ŗ un
ordinateur.
|
Choisir le ou (les)
montage(s) correct(s) pour mesurer ou calculer l'intensitť du courant
traversant la diode.
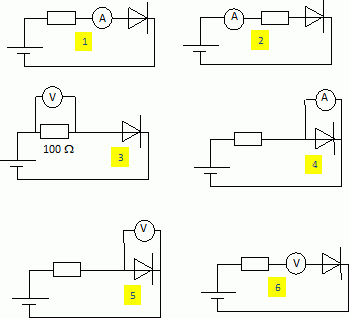
L'ampŤremŤtre doit Ítre montť en sťrie avec la diode et le
conducteur ohmique de protection. Montages 1
et 2.
Le volmŤtre doit Ítre montť en dťrivation aux bornes du conducteur
ohmique de rťsistance R = 100 ohms ; puis diviser la tension mesurťe en
volts par 100. Montage 3.
Une tension ťlectrique est appliquťe en voie 2 d'un
oscilloscope. L'ťcran affiche le tracť ci-dessous. Le zťro ( 0
V) est rťglť au centre de l'ťcran.
Dťterminer
la pťriode, la frťquence et la valeur maximale de cette tension.
CH1 : 1,0 V/div GND ; CH2 : 0,50 V / div DC ; TB = 200Ķs ; TR :
CH2+DC.
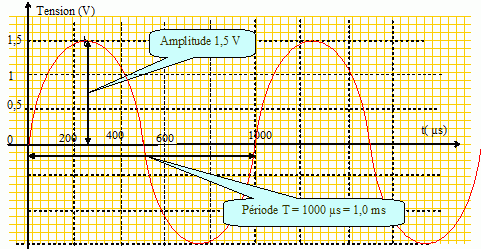
La frťquence est l'inverse de la pťriode exprimťe en seconde : f =
1/0,001 = 1000 Hz.
La cuve ŗ onde sert ŗ
:
A. produire des ondes
acoustiques. Faux.
B. Etudier des ondes ŗ la
surface de l'eau. Vrai.
C. Illustrer par exemple
des interfťrences. Vrai.
D. Etudier des vibrations
mťcaniques de frťquences supťrieures ŗ 10 kHz. Faux.
Un stroboscope est un
appareil qui : :
A. est indispensable ŗ la
dťtection de mouvements. Faux.
B. Emet des flashs
lumineux ŗ intervalle de temps rťgulier. Vrai.
C. Est adaptť ŗ la
mesure des frťquences d'oscillations mťcaniques situťes entre quelques
Hz et quelques kHz. Vrai.
D. Est adaptť ŗ
la mesure des frťquences d'oscillations mťcaniques situťes entre 50 kHz
et 500 kHz. Faux.
Pendule simple.
Proposer une liste de matťriel ŗ mettre ŗ la disposition du professeur
pour ťtudier une relation entre la pťriode du pendule et la
longueur de celui-ci. Schťmatiser le montage ŗ rťaliser.
Fils de
diffťrentes longueur ; masse marquťe, pince et support, mŤtre et
chronomŤtre.

On dispose au laboratoire d'une solution d'eau oxygťnťe de
concentration molaire volumique C = 5,0 10-1 mol/L. Pour
prťparer 250 mL d'une solution d'eau oxygťnťe ŗ 0,010 mol/L, il
faut utiliser pour la dilution :
A. 1 pipette jaugťe de 50
mL, une fiole jaugťe de 250 mL. Faux.
B. 1 becher de 50 mL, une fiole
jaugťe de 250 mL. Faux.
C. 1 pipette jaugťe de 5 mL, une
fiole jaugťe de 250 mL.Vrai.
D. 1 pipette jaugťe de 10 mL, une
fiole jaugťe de 500 mL. Faux.
A. 1 becher de
50 mL, un
erlenmeyer de 250 mL. Faux.
Le facteur de dilution vaut F =
0,50 / 0,010 = 50. le volume de la pipette jaugťe est ťgal ŗ 250 / 50 =
5,0 mL.
Une solution placťe dans un tube ŗ
essais contient des ions argent et des ions ferriques. On y ajoute une
solution de thiocyanate de potassium en excŤs, on observe :
A. l'apparition du
prťcipitť blanc et d'une coloration rouge. Vrai.
B. l'apparition d'un prťcipitť blanc
seulement. Faux.
C. l'apparition
d'un prťcipitť blanc seulement. Faux.
D. l'apparition d'un prťcipitť jaune
seulement. Faux.
Solution tampon.
Nį
|
Composants
|
mťlange
|
gamme
de pH ŗ 25 įC
|
|
A
|
B
|
|
|
1
|
KH2PO4
ŗ 0,1 M
|
NaOH ŗ
0,1 M
|
50 mL
A et x mL de B
Amener ŗ 100 mL ( eau )
|
6,2 -
8,0
|
2
|
Tris
0,2 M
|
HCl
0,1 M
|
50 mL
A et x mL de B
Amener ŗ 100 mL ( eau ) |
7,0 -
9,0
|
3
|
Na2B4O7
( borax) 0,025 M
|
HCl
0,1 M
|
50 mL
A et x mL de B
Amener ŗ 100 mL ( eau ) |
8,0 -
9,1
|
solution
tampon 1
|
solution
tampon 2
|
solution
tampon 3
|
pH
|
x(mL)
|
pH
|
x(mL) |
pH
|
x(mL) |
5,8
|
3,6
|
7,0
|
46,6
|
8,0
|
20,5 |
6,0
|
5,6
|
7,2
|
44,7 |
8,2
|
18,8 |
6,2
|
8,1
|
7,4
|
42,0 |
8,4
|
16,6 |
6,4
|
11,6
|
7,6
|
38,5 |
8,6
|
13,5 |
6,6
|
16,4
|
7,8
|
34,5 |
8,8
|
9,6
|
6,8
|
22,4
|
8,0
|
29,2 |
|
|
7,0
|
29,1
|
8,2
|
22,9 |
|
|
7,2
|
34,7
|
8,4
|
17,2 |
|
|
7,4
|
39,1
|
8,6
|
12,2
|
|
|
7,6
|
42,8
|
8,8
|
8,5
|
|
|
7,8
|
45,3
|
9,0
|
5,7
|
|
|
8,0
|
46,7
|
|
|
|
|
Un professeur a besoin de 500 mL de solution tampon ŗ pH = 7,00 pour
ťtalonner les pHmŤtres. Pour la confectionner il faut utiliser :
A. 233 mL HCl 0,1 M+ 250
mL KH2PO4 ŗ 0,1 M et complťter ŗ 500 mL avec de
l'eau distillťe. Faux.
On doit utiliser NaOH avec KH2PO4 et non HCl.
B. 145,5 mL NaOH
0,1 M + 250 mL KH2PO4 ŗ 0,1 M et complťter ŗ 500
mL avec de l'eau distillťe. Vrai.
ŗ partir de 250 mL de A il faudrait :
250*29,1/50 =2145,5 mL NaOH.
C. 233 mL HCl 0,1 M+ 250
mL de tris 0,2 M et complťter ŗ 500 mL avec de l'eau distillťe. Vrai.
ŗ partir de 250 mL de A il
faudrait : 250*46,6/50 =233 mL HCl.
A. 102,5 mL
HCl 0,1 M+ 250 mL Na2B4O7 ŗ
0,025 M et complťter ŗ 500 mL avec de l'eau distillťe. Faux.
La gamme de pH est 8,0 - 9,1
avec ce mťlange.
|
Pour le stockage de
longue durťe des ťlectrodes pH-mťtriques, on les place :
A. dans de l'eau
distillťe. Faux.
B.
dans de l'acide chlorhydrique ŗ 3,0 mol/L. Faux.
C.
dans une solution de chlorure de sodium ŗ 3,0 mol/L. Faux.
D.
dans une solution de chlorure de potassium ŗ 3,0 mol/L. Vrai.
E.
dans l'air. Faux.
Un enseignant dťsire faire rťaliser par ses ťlŤves, le titrage
pHmťtrique d'un volume VA = 20,0 mL d'une solution d'acide
sulfamique NH2SO3H ( dťtartrant pour cafetiŤre )
de concentration inconnue par la soude ŗ CB = 0,50 mol/L.
Ces deux solutions seront placťes dans des flacons ťtiquetťs. Faire la liste du
matťriel pour un poste de travail.
Burette graduťe, erlenmeyer, agitateur magnťtique, 2 flacons ťtiquetťs,
deux bechers de 50 mL, pipette jaugťe de 20,0 mL et pipeteur, pH-mŤtre.
Quelles
indications et/ou pictogrammes doivent Ítre portťes sur le flacon
de soude ?

Provoque de graves
brŻlures ; port de gants et lunettes de protection.
L'acide sulfamique se dissociant
totalement dans l'eau, il se trouve sous forme NH2SO3-aq
+ H3O+aq. L'ťquation du titrage est alors :
H3O+aq + HO-aq
= 2H2O(l).
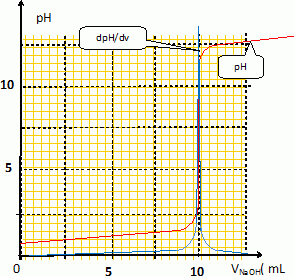
Dťterminer
la concentration de la solution d'acide sulfamique.
Le volume ťquivalent est ťgal ŗ VE = 10 mL ( Brusque saut
de pH et la courbe dpH/dv prťsente un pic ).
A l'ťquivalence les quantitťs de matiŤre des rťactifs sont en
proportions stoechiomťtriques :
CVA = CB VE ; C = CB VE / VA =0,5*10/20 = 0,25 mol/L.
On donne la zone de virage [10 - 12 ] du jaune d'alizarine.
Expliquer
pourquoi cet indicateur colorť ne convient pas pour repŤrer
l'ťquivalence.
Lors du titrage acide fort base forte, le pH de l'ťquivalence est ťgal
ŗ 7 ; la zone de virage de l'indicateur colorť doit contenir le pH du
point ťquivalent.
Pour mettre en ťvidence l'ťthanal dans l'expťrience de la lampe sans
flamme, le professeur place un rťactif dans un flacon comme le montre
les schťmas suivants. Afin d'entretenir la lampe sans flamme, il
demande au prťparateur que l'ensemble soit reliť ŗ une trompe ŗ
eau avec fiole de garde. Quel est le montage
qui convient ?
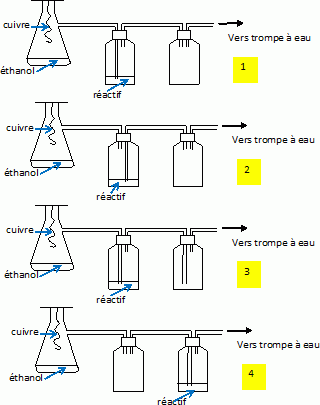
2 ne convient pas : le
produit issu de la rťaction doit barboter dans le rťactif.
3 ne convient pas : en cas de de retour d'eau, celle-ci pourrait
passer dans le flacon du rťactif.
4 ne convient pas : la fiole de garde doit Ítre placťe juste avant la
trompe ŗ eau.
|
Nommer
les diffťrents ťlťments de verrerie et indiquer ceux qu'il faudrait
utiliser pour un montage d'hydrodistillation.
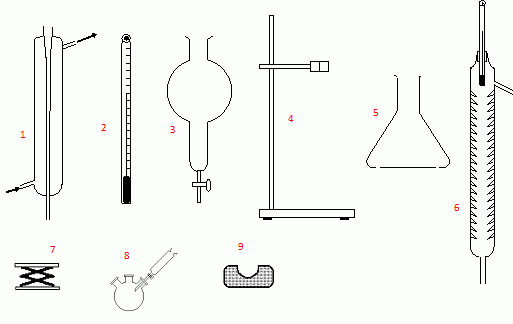
1 : rťfrigťrant ŗ eau ; 2 : thermomŤtre ; 3 : ampoule ŗ dťcanter ; 4 :
support ; 5 : erlenmeyer ; 6 : colonne Vigreux + thermomŤtre ; 7 :
ťlťvateur ŗ croisillons ; 8 : tricol avec ampoule de coulťe ; 9 :
chauffe ballon.
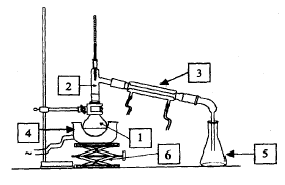
1 : ballon
; 2 : tÍte de colonne ou allonge coudťe ; 3 : rťfrťgirant ; 4 : chauffe
ballon ; 5 : erlenmeyer ; 6 : ťlťvateur ŗ croisillons. Le thermomŤtre
n'est pas utile. Un support doit maintenir le rťfrigťrant ŗ eau.
|








