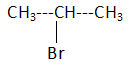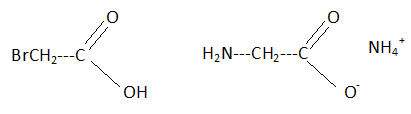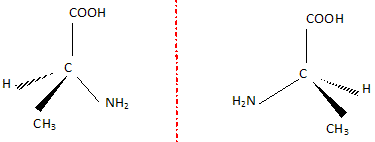Rťactions
d'addition :
Donner la
formule semi-dťveloppťe du 2-bromopropane.
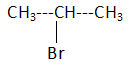
Parmi
les propositions ci-dessous, quel(s) est (sont) celui (ceux) qui
convient ( conviennent ) pour
traduire la relation existant entre le 2-bromopropane et le
1-bromopropane. Justifier.
IsomŤres de fonction, isomŤres de constitution, ťnantiomŤres,
diastťrťoisomŤres.
IsomŤres de constitution : l'atome de brome est portť par le carbone 1
ou le carbone 2.
L'addition de bromure d'hydrogŤne sur le propŤne conduit au
2-bromopropane.
Donner le
mťcanisme en discutant de l'orientation de l'addition.
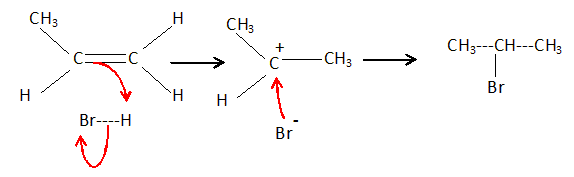
L'ťtape
dťterminante est la formation du carbocation secondaire, plus stable
qu'un carbocation primaire. Le 2-bromopropane est
le produit majoritaire.
L'addition
de bromure d'hydrogŤne HBr sur le propŤne en prťsence de peroxyde de
benzoyle ( C6H5CO-O-O-COC6H5)
conduit au 1-bromopropane.
Donner
le mťcanisme en discutant de l'orientation de l'addition. (effet Karasch )
C6H5CO-O-O-COC6H5 --> 2C6H5CO-O..
C6H5CO-O.+ HBr --> C6H5CO-OH + Br..
CH3-CH=CH2 + Br.--> CH3-.CH-CH2Br ( formation du radical le plus stable)
CH3-.CH-CH2Br + HBr --> CH3-CH2-CH2Br + Br..
|
Rťations
d'ťlimination.
La dťshydrobromation ŗ
tempťrature ťlťvťe du 3-bromo-3-mťthylpentane en prťsence d'ion
hydroxyde conduit ŗ un mťlange de trois produits dont les formules
topologiques sont indiquťes ci-dessous :
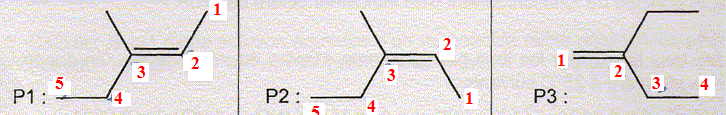
|
Donner les
noms des 3 produits.
P1
: (E) 3-mťthylpent-2-Ťne ; P2
: (Z) 3-mťthylpent-2-Ťne ; P3
: 2-ťthylbut-1-Ťne.
Il existe des ťliminations E1 et E2.
Dťfinir
ces ťliminations puis identifier en justifiant le type d'ťlimination
pour le 3-bromo-3-mťthylpentane en prťsence d'ion hydroxyde ŗ
tempťrature ťlevťe.
Elimination E2
bimolťculaire :
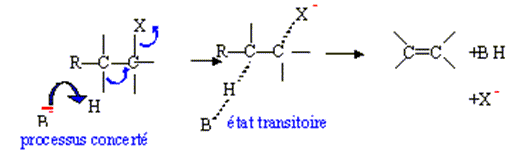
Elimination E1
monomolťculaire :
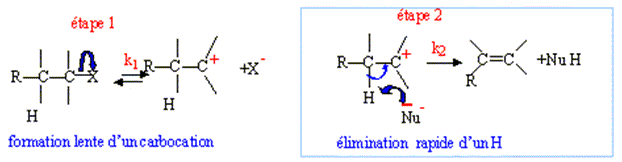
Pour le
3-bromo-3-mťthylpentane, l'ťlimination E1
conduit ŗ un carbocation tertiaire, particuliŤrement stable.
Donner le
mťanisme de la rťaction et expliquer la formation des trois
produits.
Il y a trois atomes d'hydrogŤne diffťrents en position bťta.
La base peut attaquer l'un ou l'autre de ces atomes, ce qui conduit ŗ 3 produits.
Pourquoi
P1 et P2 sont-ils obtenus
majoritairement ?
Lorsque
la base a le choix entre deux hydrogŤnes en position bťta,
c'est l'alcŤne le plus substituť qui est le produit prťdominant de
l'ťlimination ( rŤgle de Saytzev)
P1
est en quantitť plus importante que P2 : pourquoi
?
L'isomŤre Z, du fait de l'encombrement stťrique, est moins stable que l'isomŤre E.
Parmi les
propositions ci-dessous, quel(s) est (sont) celui (ceux) qui convient (
conviennent ) pour
traduire la relation existant entre P1
et P2. Justifier.
IsomŤres de fonction, isomŤres de constitution, ťnantiomŤres,
diastťrťoisomŤres.
isomŤres de constitution, diastťrťoismŤres ( isomťrie de type Z E ).
Amino-acides et peptides.
On se propose de faire la synthŤse du plus simple des amino-acides, l'acide aminoťthanoÔque de formule H2N-CH2-COOH encore appelť glycine.
On fait agir du dibrome en prťsence de phosphore sur l'acide ťthanoÔque. On obtient un produit A de formule C2H3O2Br.
A est mis en prťsence d'un excŤs d'ammoniac ŗ 50 įC, on isole un produit B de formule brute C2H8O2N2. ( B est un sel d'ammonium ).
B est ensuite acidifiť et on obtient la glycine.
Ecrire les formules semi-dťveloppťes de A et B.
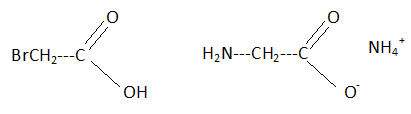
Donner
la formule semi-dťvelppťe d'une liaison peptidique puis citer un
exemple ( hormis peptide ) de molťcule du vivant contenant des liaisons
peptidiques.
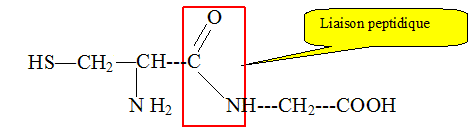
Dans les protťines, les acides aminťs sont reliťs par des liaisons peptidiques.
|
Erire
les rťactions de formation ( en utilisant les formules semi-dťveloppťes
) des 4 dipeptides que l'on peut former ŗ partir d'un mťlange de
glycine et d'alanine ( acide 2-aminopropanoÔque ).
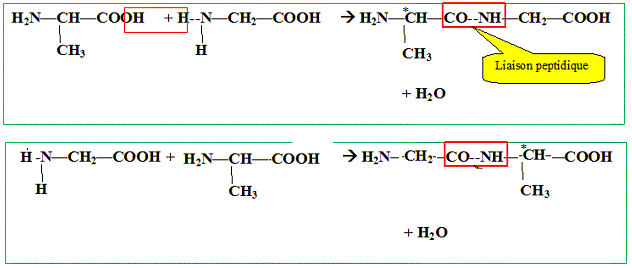
Chaque dipeptide possŤde un carbone asymťtrique : il y a donc deux couples d'ťnantiomŤres.
L'alanine prťsente deux stťrťoisomŤres.
Pourquoi ? Les reprťsenter en reprťsenation de Cram et indiquer le type de stťrťoisomŤres.
La prťsence d'un atome de carbone asymťtrique conduit ŗ l'existence de deux ťnantiomŤres.
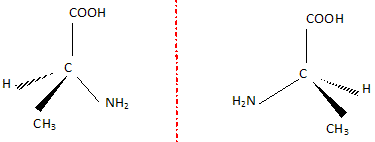
|