Dosage
des ions cuivre (II) dans la bouillie bordelaise ŗ 10 g/L.
La
bouillie bordelaise est constituťe de 80 % en masse de sulfate de
cuivre pentahydratť et de 20 % en masse de chaux ťteinte Ca(OH)2.
Calculer
les quantitťs de matiŤre en hydroxyde de calcium et en sulfate de
cuivre pentahydratť dans 1,00 L de bouillie ŗ 10 g/L.
2 g de chaux ťteinte ; M(Ca(OH)2) =
40+2*17 =74 g/mol
n = m/M = 2 / 74 = 2,70 10-2 mol.
8 g de CuSO4, 5H2O; M =
63,5+32+4*16+5*18 = 249,5 g/mol
n = 8 / 249,5 = 3,21 10-2
mol.
Dans une fiole jaugťe de 1,00 L, on introduit 10,0 g de bouillie
bordelaise et de l'eau permutťe jusqu'au trait de jauge. La solution
obtenue n'est pas homogŤne. On filtre le mťlange. Soit S0
le filtrat. On considŤrera que le volume du filtrat est 1,00 L.
Quelques gťnťralitťs sur les courbes intensitť-potentiel.
Pour
tracer la courbe intensitť-potentiel d'une solution S' de diiode sur
ťlectrode de platine, on rťalise le montage ŗ trois ťlctrodes prťsentť
ci-dessous.
On rappelle qu'une solution de diiode est prťparťe ŗ
partir d'une solution d'iodure de potassium et de cristaux de diiode et
que les espŤces maoritaires en solutions sont K+, I- et I3-. Dans la solution S' ťtudiťe, la concentration en ions triodure [I3-] vaut 0,10 mol/L et celle des ions iodure [I-] vaut 0,60 mol/L.
Schťma du montage ŗ trois ťlectrodes.
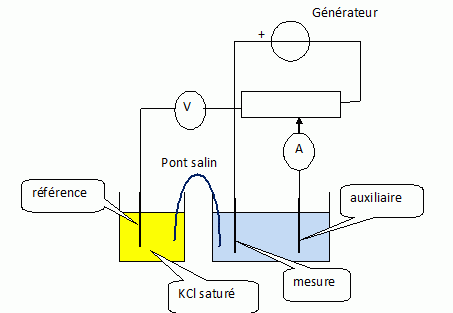
L'ťlectrode de travail ( mesure ) doit Ítre maintenue ŗ un potentiel
constant : aucun courant ťlectrique ne doit traverser l'ťlectrode
de rťfťrence (sinon son potentiel serait modifiť). Une troisiŤme
ťlectrode est donc nťcessaire. Le courant circule alors entre
l'ťlectrode de mesure et l'ťlectrode auxiliaire ; le potentiel
est imposť entre l'ťlectrode de mesure et l'ťlectrode de rťfťrence.
On sťpare physiquement l'ťlectrode de rťfťrence de la solution ŗ ťtudier.
|
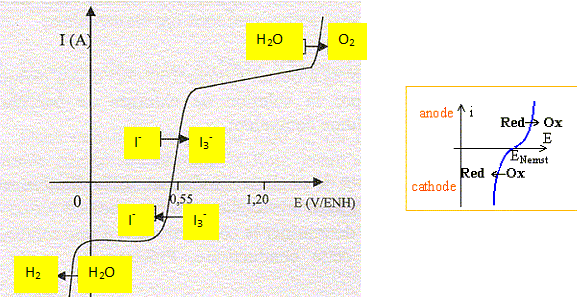
L'allure de la courbe intensitť-potentiel est la suivante :
|
Dans certains ouvrages techniques, l'intensitť est remplcťe par la densitť de courant j ( A m-2).
Quel intťrÍt pratique y a t-il ŗ effectuer ce remplacement ?
L'intensitť
mesurťe dťpend de la surface de l'ťlectrode. En utilisant la densitť de
courant, on s'affranchit de ce paramŤtre " surface de l'ťlectrode".
L'allure des courbes est plus gťnťral.
Au
regard de la courbe expťrimentale, quels systŤmes redox peuvent Ítre
considťrťs comme rapide ou lent dans ces conditions opťratoires.
Justifier.
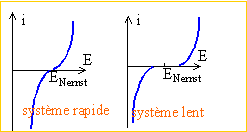
I3- / I- : ystŤme rapide ; H2O /H2 et O2/H2O : systŤmes lents.
Le caractŤre lent ou rapide dťpend essentiellement de la nature de l'ťlectrode oý se produit l'ťchange d'ťlectrons.
Le systŤme H+/H2 est rapide sur ťlectrode de platine et lent sur ťlectrode de graphite.
Deux paliers sont observťs sur la courbe expťrimentale.
Quel(s) phťnomŤ(s) physique(s) est (sont) responsable(s) de la limitation du courant ?
Vitesse de diffusion des ions au voisinage des ťlectrodes oý se dťroulent l'oxydation ou la rťduction.
Le transport de matiŤre est le facteur limitant : on observe un palier.
De quel(s) paramŤtre(s) dťpend la hauteur d'un palier ?
Le courant limite (hauteur du palier ) est proportionnel ŗ la concentration en rťactif et au nombre d’ťlectrons ťchangťs.
Expliquer pourquoi les paliers ne sont pas observťs dans les parties extrŤmes gauche et droite de la courbe.
Rťduction ou oxydation du solvant : il n'y a pas de limitation dŻ au transfert de matiŤre.
La concentration de l'eau est telle que l'on ne peut pas atteindre un palier de diffusion.
Dťterminer
d'un point de vue thťorique le potentiel ŗ courant nul de l'ťlectrode
de platine plongeant dans la solution de diiode ťtudiťe. Calculer sa
valeur.
I3- +2e- = 3 I- ; E = Eį(I3- / I- ) + 0,03 log ([I3-] / [ I-]) =0,54 +0,03 log(0,10 / 0,60) =0,54-0,03 = 0,516~0,52 V.
Dosage du cuive (II) par iodomťtrie : suivi colorimťtrique.
Dans un becher, introduire une prise d'essai V3 =25,0 mL de la solution S0. Ajouter 30 mL d'une solution d'iodure de potassium K+aq + I-aq ŗ 100 g/L ( 0,600 mol/L ). Attendre 10 minutes.
Titrer par une solution de thiosulfate de sodium ( 2Na+aq + S2O32-aq) de concentration C3 = 1,00 10-2 mol/L en ion thiosulfate.
Ecrire
l'ťquation de la rťaction traduisant la transformation chimique
observťe dans le becher avant ajout de thiosulfate de sodium.
Un prťcipitť d'oxyde de cuivre (I) se forme : 3I-aq +Cu2+aq = CuI(s) + I3-aq. (1)
La couleur jaune brun de la solution est due ŗ l'ion I3-aq.
Ecrire l'ťquation de la rťaction du dosage.
I3-aq +2S2O32-aq = 3I-aq + S4O62-aq.
Comment peut-on bien visualiser l'ťquivalence ?
I3-aq
est la seule espŤce colorťe : avant l'ťquivalence, ajouter de l'empois
d'amidon, ce dernier rťagit avec le diiode pour donner une coloration
violette assez foncťe.
A.N : Ve4 = 12,4 mL.
A l'ťquivalence n(S2O32-aq) = 2 n(I3-aq) ; n(I3-aq) =ĹC3Ve4 = 0,5 * 1,00 10-2 *12,4 10-3 =6,2 10-5 mol.
D'aprŤs (1) la quantitť de matiŤre d'ion cuivre (II) vaut : n(Cu2+aq) = n(I3-aq) =6,2 10-5 mol dans 25,0 mL.
[Cu2+aq] =6,2 10-5 / 0,025 =2,48 10-3 mol/L.
Dosage des ions cuivre (II) par iodomťtrie : suivi par potentiomťtrie.
La mťthode colorimťtrique n'est pas toujours adaptťe au dosage du
cuivre (II), soit parce que les solutions sont trop peu concentrťes,
soit parce que l'ťquivalence n'est pas dťtectable facilement
visuellement. Les mťthodes potentiomťtriques peuvent s'avťrer des
mťthodes de choix pour des concentrations pas trop faibles (
supťrieures ou ťgales ŗ 10-3 mol/L).
Etude thťorique prťliminaire :
Quatre
courbes intensitť-potentiel sur ťlectrode de platine ont ťtť tracťes
pour diffťrents volumes V de solution de thiosulfate de sodium versť au
cours de l'expťrience prťcťdente. Soit pour V=0 ; V < Ve ; V=Ve ; V > Ve. Ve reprťsente le volume de solution de thiosulfate de sodium versť ŗ l'ťquivalence.
AprŤs avoir dťterminť les espŤces prťdominantes ťlectroactives, justifier l'allure des courbes ?
Les ions tťtrathionate ne sont pas ťlectroactifs dans l'eau sur ťlectrode de platine, CuI(s) n'intervient pas. Le couple S4O62-aq / S2O32-aq est lent sur ťlectrode de platine.
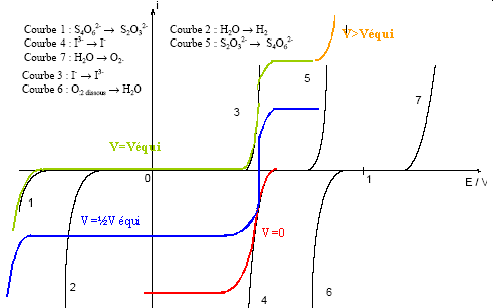
V=0 : I-aq ; I3-aq sont prťsents : le couple I3-aq / I-aq fixe le potentiel.
V < Ve ; [I3-aq] diminue, [I-aq] augmente, les ions S4O62-aq sont prťsents et S2O32-aq est en dťfaut. L'intensitť du courant
|iC| diminue linťairement avec
[I3-] lors de l'ajout du
thiosulfate.
V=Ve : les ions S4O62-aq et I-aq sont prťsents. |iC| s'annule.
V > Ve : les ions S4O62-aq et I-aq sont prťsents et l'ion S2O32-aq est en excŤs ( S2O32-aq s'oxyde ) : le couple S4O62-aq / S2O32-aq fixe le potentiel.
Dosage potentiomťtrique ŗ courant nul :
On introduit dans le becher une ťlectrode au calomel saturť et une ťlectrode de platine, la diffťrence de potentiel DE entre les deux ťlectrodes est mesurťe au cours du dosage, de faÁon ŗ pouvoir tracer DE
= f(V) oý V est le volume de la solution de thiosulfate de sodium. On
observe qu'aprŤs l'ťquivalence la diffťrence de potentiel mesurťe n'est
pas stable. Le relevť des mesures n'est possible qu'avant l'ťquivalence.
Expliquer pourquoi ŗ l'aide des courbes intensitť-potentiel.
Le couple S4O62-aq / S2O32-aq est lent sur ťlectrode de platine. Le potentiel de l’ťlectrode ŗ intensitť nulle n’est pas bien dťfini.
Un systŤme lent ne peut pas Ítre utilisť pour rťaliser un dosage potentiomťtrique ŗ courant nul.
Dosage potentiomťtrique ŗ courant imposť.
On introduit dans le becher deux ťlectrodes de platine dans lesquelles
circule un courant trŤs faible de l'ordre de 1 ĶA. L'une des ťlectrodes
joue le rŰle d'anode et l'autre de cathode. La diffťrence de potentiel
DE entre ces deux ťlectrodes est mesurťe au cours du dosage, de faÁon ŗ
pouvoir tracer DE = f(V).
Pourquoi le courant imposť est-il si faible ?
Les quantitťs de substances ťlectrolysťes doivent Ítre nťgligeables par rapport aux quantitťs ŗ doser.
Reprťsenter ia et ic respectivement courant anodique et cathodique qui circulent dans les ťlectrodes.
Le tracť sera rťalisť sur la courbe obtenue en V=0 ; echelle : 3 mm pour 1 ĶA.
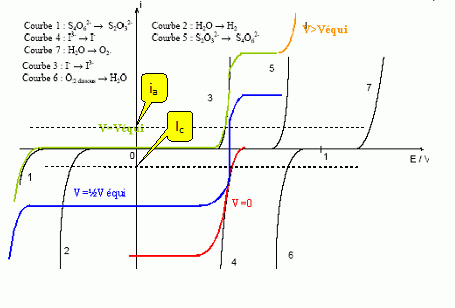
|
A
l'aide du faisceau de courbes intensitť-potentiel, on souhaite prťvoir
l'allure de la courbe de titrage que l'expťrimentateur devrait obtenir.
Dťterminer l'ordre de grandeur de DE0, diffťrence de potentiel entre anode et cathode pour i=1 ĶA ŗ V=0.
Anode : oxydation de I-aq ; cathode : rťduction de I3-aq:
Le systŤme I3-aq / I-aq ťtant rapide, DE0 ~ 0 V.
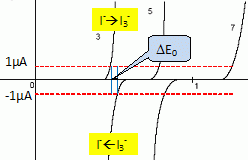
Dťterminer l'ordre de grandeur de DE1, diffťrence de potentiel entre anode et cathode pour i=1 ĶA ŗ V < Ve.
L'ion thiosulfate est en dťfaut.
Le systŤme I3-aq / I-aq ťtant rapide, DE1 ~ 0 V.
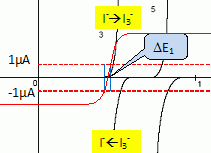
Dťterminer l'ordre de grandeur de DEť, diffťrence de potentiel entre anode et cathode pour i=1 ĶA ŗ V = Ve.
I3-aq a disparu ; l'ion thiosulfate est en dťfaut ;
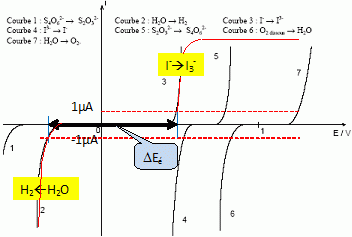
Dťterminer l'ordre de grandeur de DE2, diffťrence de potentiel entre anode et cathode pour i=1 ĶA ŗ V> Ve.
I3-aq a disparu ; l'ion thiosulfate est en excŤs ;
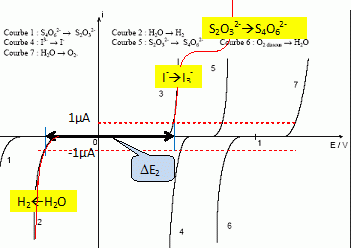
En dťduire l'allure de la courbe de titrage.
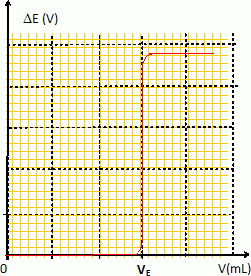
L'ťquivalence est repťrťe par la variation brutale de DE.
La variation DE ťtant trŤs rapide, il faut resserer les mesures autour du point ťquivalent.
|









