Cette
partie va traiter de l'apport de la chimie pour l'obtention des
matťriaux nťcessaires au dťveloppement des cellules photovoltaÔques.
Le
silicium semi-conducteur.
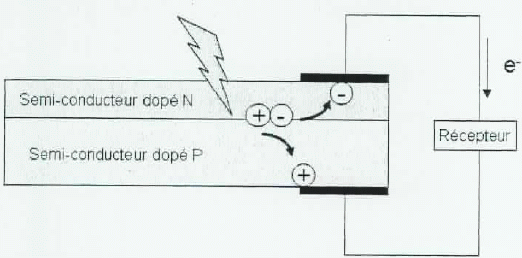
Les cellules photovoltaÔques ŗ base de silicium sont obtenues en crťant
une jonction P-N entre des semi-conducteurs de type P( dťfaut
d'ťlectrons) et N ( excŤs d'ťlectrons ). Sous l'action de la lumiŤre,
il y a formation d'une paire ťlectron-trou et l'action du champ
ťlectrique crťť par la jonction P-N permet la sťparation des charges.
Le courant ťlectrique rťsulte de la migration des charges chacune de
leur cŰtť.
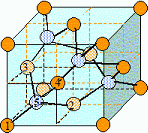
Le silicium cristallise dans une structure de type diamant.
Dťcrire cette
structure ŗ l'aide d'un schťma.
La structure de type diamant est une maille cubique ŗ
face centrťe avec occupation de la moitiť des sites tťtraŤdriques ( 4
sur 8) de faÁon alternťe, ce qui donne finalement 8 atomes par maille
ťlťmentaire.
Le paramŤtre de la maille a est ťgal ŗ 543 pm.
Calculer la densitť du silicium.
Volume d'une maille V= a3 =( 543
10-12)3 =1,60 10-28
m3.
masse de 8 atome de silicium : 8*28,1 10-3
/ 6,02 1023 = 3,73 10-25 kg
masse volumique : 3,73 10-25 / 1,60
10-28 = 2,33 103 kg
m-3 = 2,33 g cm-3 : d = 2,33.
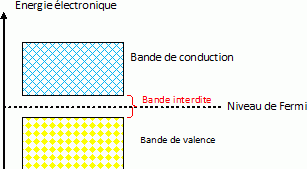
Indiquer
ŗ quoi correspond la bande de valence, la bande de conduction et la
bande interdite dans la thťorie des bandes pour un semi-conducteur
comme le silicium.
Les valeurs de l'ťnergie d'un ťlectron dans un solide sont comprises
dans certains intervalles que l'on nomme ę bandes permisesĽ, sťparťs par d'autres ę bandes d'ťnergie interditesĽ.
Le silicium peut Ítre dopť P ou N en faisant diffuser du gaz phosphine ( PH3) ou diborane ( B2H6) dans du silicium fondu.
Indiquer ŗ quoi correspond le dopage du silicium et quel type de dopage sera obtenu en fonction du gaz utilisť.
On remplace un petit nombre d'atome de silicium par des atomes
"impuretťs" de phosphore ou de bore dans le but de modifier la
conductivitť du semi-conducteur.
Si l'atome impuretť appartient ŗ la colonne prťcťdente ( cas du bore) ,
il manque un ťlectron ; cette carence en ťlectron, c'est ŗ dire
prťsence d'un trou, conduit au dopage P.
Si l'atome apportť appartient ŗ la colonne suivante ( cas du phosphore ), un ťlectron est excťdentaire. Il s'agit d'un dopage N.
|
Prťciser en quoi correspond la formation d'une paire ťlectron-trou sous l'action d'un rayon lumineux.
Un rayon lumineux peut apporter suffisamment d'ťnergie pour qu'un
ťlectron de la bande de valence soit excitť et passe dans la bande de
conduction. Ce dťpart de l'ťlectron laisse une place vide ( un trou )
dans la bande de valence.
Dťterminer
la valeur limite de la longueur d'onde du rayon lumineux pour que soit
crťťe une paire ťlectron-trou si la bande interdite est de 1,1 eV.
E = hc/l ; l = hc/E = 6,02 10-34 *3,0 108 / (1,1*1,6 10-19) =1,026 10-6 m ~1,0 Ķm.
|
Les cellules de type Grštzel.
Elles sont inspirťes de la photosynthŤse et dissocient l'absorption de
la lumiŤre et la sťparation des charges. La cellule est composťe d'un
semi-conducteur ŗ large bande interdite tel que le dioxyde de
titane TiO2 ( DE=3,2
eV) recouvert d'un colorant organique sous forme d'une couche
monomolťculaire et d'un ťlectrolyte contenant des ions iodure. Le
colorant absorbe la lumiŤre en donnant un ťtat excitť notť S* et ťjecte
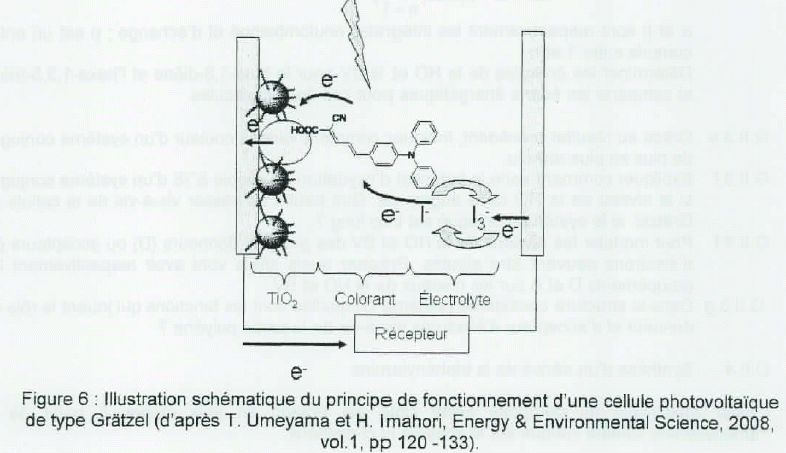
un ťlectron dans la bande de conduction de TiO2, en donnant un ťtat S+. Les ions iodures sont oxydťs par S+. Les ions triodure I3- formťs migrent vers la cathode oý ils sont rťduits par les ťlectrons provenant de la photo-anode lorsque la pile dťbite.
Indiquer
briŤvement ŗ quoi correspond la photosynthŤse effectuťe par les
plantes. Ecrire l'ťquation de la rťaction gťnťralement admise.
Les plantes synthťtisent de la matiŤre organique en utilisant l'ťnergie du soleil, du dioxyde de carbone et de l'eau.
6 CO2 + 6 H2O + lumiŤre = C6H12O6 + 6O2 .
Dťcomposer
chacune des ťtapes dťcrites dans la figure ci-dessus en ťcrivant les
ťquations des diffťrentes rťactions redox qui interviennent.
Les ions iodures sont oxydťs par S+ : 3I- = I3- +2 e- ;
Les ions triodure I3- formťs migrent vers la cathode oý ils sont rťduits par les ťlectrons provenant de la photo-anode : I3- +2 e- = 3I-.
Approche thťorique de la synthŤse des colorants.
Des
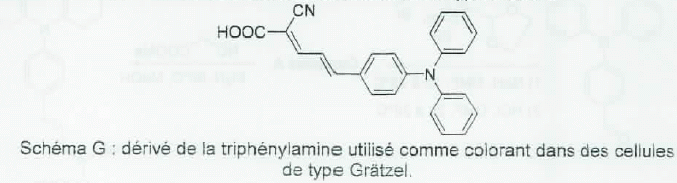
dťrivťs de la triphťnylamine ( schťma ci-dessous ) qui comportent une
partie linťaire conjuguťe ont ťtť rťcemment utilisťs comme colorant
dans les cellules de type Grštzel.
Pour que le systŤme fonctionne il faut que les ťnergies des
niveaux HO et BV du colorant soient respectivement plus bas que le
niveau imposť par le couple I3- / I- et plus ťlevť que le niveau de fermi de TiO2.
Les niveaux de la HO et BV pour la partie linťaire conjuguťe
peuvent Ítre prťdits par une approche thťorique telle que la thťorie de
HŁckel.
Donner la dťfinition d'un systŤme conjuguť linťaire.
SystŤme prťsentant une alternance de liaisons carbone simples (σ) et liaisons doubles (σ+π).
Dans un systŤme conjuguť on peut ťcrire plusieurs formes limites de la molťcule : les ťlectrons p, les doublets non liants sont dťlocalisťs sur plusieurs centres. La molťcule est stabilisťe.
A quoi correspondent les niveaux HO et BV.
HO : plus haute orbitale occupťe ; BV : plus basse orbitale vacante.
Prťciser les approximations faites dans la mťthode de HŁckel.
Le squelette de la molťcule plane est constituť d'orbitales molťculaires s ( recouvrement axial d'orbitale atomique s ou p). Le recouvrement latťral des orbitales atomique pz constitue les orbitales molťculaires p.
Les systŤmes s et p sont indťpendants et orthogonaux dans la thťorie de HŁckel.
De plus pour des atomes identiques les intťgrales coulombiennes
sont ťgales : elles sont notťe Ŗ pour des atomes liťs et valent zťro si
les atomes ne sont pas liťs.
Enfin les intťgrales de recouvrement Srs valent 0 si r diffŤre de s et Srr = 1.
Pour un polyŤne linťaire ŗ n atomes de carbone, les ťnergies
des orbitales molťculaires sont donnťes dans le modŤle de HŁckel par la
relation : Ep = a +2Ŗ cos [p p / (n+1)]
oý a et Ŗ sont respectivement les intťgrales coulombienne et d'ťchange ; p est un nombre entier compris entre 1 et n.
Dťterminer les
ťnergies de la HO et de la BV pour le buta-1,3-diŤne et
l'hexa-1,3,5-triŤne et comparer les ťcarts ťnergťtiques pour ces deux
molťcules.
Buta-1,3-diŤne : n=4 ; E1 = a+2Ŗ cos (p/5) = a+1,618 Ŗ.
E2 = a+2Ŗ cos (2p/5) = a+0,618 Ŗ. HO.
E3 = a+2Ŗ cos (3p/5) = a-0,618 Ŗ. BV.
Ecart entre la HO et la BV : 2*0,618 Ŗ = 1,236 Ŗ.
Hexa-1,3,5-triŤne : n=6 ; E1 = a+2Ŗ cos (p/7) = a+1,80 Ŗ.
E2 = a+2Ŗ cos (2p/7) = a+1,247 Ŗ.
E3 = a+2Ŗ cos (3p/7) = a+0,445 Ŗ. HO.
E4 = a+2Ŗ cos (4p/7) = a-0,445 Ŗ. BV.
Ecart entre la HO et la BV : 2*0,445 Ŗ = 0,89 Ŗ.
Indiquer comment varie la couleur d'un systŤme conjuguť de plus en plus ťtendu.
L'ťcart ťnergťtique est plus faible dans le cas de l'hexa-1,3,5-triŤne par rapport au buta-1,3-diŤne.
Cette transition doit donc nťcessiter un photon d'ťnergie moins ťlevťe
que dans le buta-1,3-diŤne ; donc de longueur d'onde plus grande. On
passe de 270 nm pour l'hexa-1,3,5-triŤne au spectre visible pour une
dizaine de doubles liaisons conjuguťes.
Expliquer comment varie le potentiel d'oxydation du couple S+/S
d'un systŤme conjuguť si le niveau de la HO de S augmente. Que peut-il
se passer vis ŗ vis de la cellule de Grštzel si le systŤme conjuguť est
trop long ?
La conjugaison rapproche les orbitales frontiŤres HO et BV. Le potentiel d'oxydation du couple S+/S va donc diminuer si la longueur du systŤme conjuguť augmente ; en consťquence les ions iodures ne seront plus oxydťs par S+si le systŤme conjuguť est trop long.
Pour moduler les niveaux de la HO et BV des groupes donneurs (D) ou accepteur (A) d'ťlectrons peuvent Ítre ajoutťs.
Prťciser quels effets vont avoir respectivement les groupes pements D et A sur les niveaux de la HO et de la BV.
Un
substituant donneur relŤve plus la HO que la BV, tandis qu'un accepteur
abaisse la BV plus que la HO : le rapprochement HO-BV est encore
accentuť.
Les groupes attracteurs CN, COOH, CHO, NO2 augmentent le potentiel d'oxydation. Les groupes donneurs diminuent le potentiel d'oxydation.
SynthŤse d'un dťrivť de la triphťnylamine.
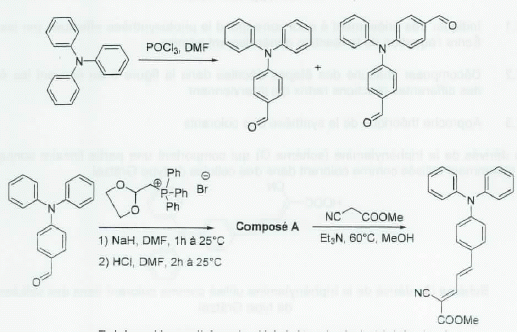
L'ester mťthylique du composť acide cible est obtenu en trois ťtapes ŗ partir de la triphťnylamine comme indiquť ci-dessous :
La
premiŤre ťtape est une rťaction de Vilsmeier-haack conduisant ŗ un
mťlange de deux produits qui sont sťparťs par une chromatographie sur
colonne avec du gel de silice comme phase stationnaire et un mťlange
d'acťtate d'ťthyle et de cyclohexane comme ťluant. Une ťtude par
chromatographie sur couche mince ( CCM) montre quen utilisant un
mťlange de 10 mL de cyclohexane avec 2 mL d'acťtate d'ťthyle, les
rapports frontaux( Rf) des deux composťs sont respectivement 0,7 et 0,3
pour le mono et dialdehyde.
Proposer un protocole dťtaillť permettant de rťaliser une CCM.
Cette CCM
doit permettre de comparer le produit rťcupťrť ŗ l'issue d'une synthŤse
au mÍme produit achetť dans le commerce. On expliquera soigneusement :
la prťparation de la cuve, la prťparation de la plaque, l'ťlution, la
rťvťlation, la mesure des rapports frontaux.
Prťparation de la plaque :
Tracer au crayon ŗ papier une ligne ŗ un
peu plus de 1 cm du bas de la plaque . Marquer au crayon sur
cette ligne les emplacements oý l'on dťposera
les solutions ŗ analyser. Les emplacements doivent
Ítre distants d'environ 1 cm, et ŗ au moins 1
cm des bords.
DťpŰt de l'ťchantillon :
A l'aide d'une pipette pasteur, ou d'un tube capillaire,
dťposer une goutte sur la plaque ŗ
l'emplacement marquť. Laisser sťcher . Si la
solution est trop diluťe, on peut faire plusieurs
dťpŰts au mÍme emplacement , ŗ
condition de bien sťcher la plaque entre deux
gouttes.
Dťveloppement du chromatogramme :
Lorsque les dťpŰts sont secs, placer la
plaque le plus verticalement possible dans la cuve, ligne de
dťpŰt vers le bas. La surface de
l'ťluant doit Ítre en de cette ligne. Couvrir.
Surveiller la plaque rťguliŤrement : quand
l'ťluant est ŗ environ 1 cm du bord
supťrieur, sortir la plaque, marquer le niveau
atteint par le solvant au crayon ŗ papier,
sťcher la plaque.
Rťvťlation :
Si les taches sont incolores, on les fera
apparaÓtre sous une lampe UV ou ŗ l'aide d'un
chimique.

|
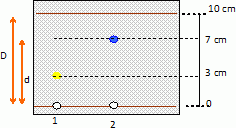
1 : espŤce pure, ťtalon ou rťfťrence.
2 : espŤce pure, ťtalon ou rťfťrence.
3 : produit du commerce
4 : espŤce obtenue par synthŤse
|
Faire un schťma de la plaque CCM obtenu dans l'expťrience ci-dessus.
|
La synthŤse du composť A se dťroule en deux parties effectuťes successivement dans le mÍme rťacteur comme dťcrit ci-dessous :
Un tricol maintenu sous diazote contenant une suspension d'hydrure de
sodium NaH ( 250 mg, 0,01 mol) dans 5 mL de DMF ( dimťthylformamide,
solvant ) est refroidie ŗ -5 įC. A l'aide d'une ampoule de coulťe
isobare, le sel de phosphonium (4,3 g , 0,01 mol) dissous dans 15 mL de
DMF est additionnťe goutte ŗ goutte ; le dťgagement gazeux doit Ítre
contrŰlť. AprŤs addition on laisse le mťlange revenir ŗ tempťrature
ambiante, et l'agitation est maintenue 15 min. Le triphťnylamine
monoaldehyde ( 2,7 g, 0,01 mol) dissous dans 20 mL de DMF est
additionnť avec un goutte ŗ goutte assez rapide et l'agitation est
maintenue pendant 1 h ŗ tempťrature ambiante. On ajoute alors
prudemment 10 mL d'une solution d'acide chlorhydrique ŗ 2 mol/L puis ŗ
nouveau 30 mL de la solution acide ; le mťlange est maintenu 2 h sous
agitation ŗ tempťrature ambiante.
Le composť organique extrait avec de l'ťther diťthylique est lavť avec
une solution saturťe d'hydrogťnocarbonate de sodium puis deux fois ŗ
l'eau. La phase organique est sťchťe sur sulfate de magnťsium anhydre
puis le solvant est ťvaporť pour donner un solide jaune qui est
recristallisť dans l'ťthanol.
Parmi les compťtences exigibles du programme de spťcialitť de terminale S on trouve :
- rťaliser les opťrations suivantes : lavage d'une phase
organique, sťchage d'une phase organique liquide, extraction
liquide-liquide, sťchage d'un solide, recristallisation.
- Appliquer les consignes de sťcuritť.
- Justifier les opťrations d'un protocole ŗ partir des donnťes
physico-chimiques ( tempťrature de changement d'ťtat, densitť, pH,
solubilitť ).
Illustrer ces diffťrentes notions en dťcrivant les opťrations citťes dans les deux derniŤres phrases du protocole ci-dessus.
" Le composť organique extrait avec de
l'ťther diťthylique est lavť avec une solution saturťe
d'hydrogťnocarbonate de sodium puis deux fois ŗ l'eau" :
L'ion hydrogťnocarbonate se comporte comme une base en milieu acide ; l'excŤs d'acide est ťliminť ( dťgagement CO2).
Les deux lavages ŗ l'eau ťlimine toute trace d'acide.
" Le composť organique
extrait avec de l'ťther diťthylique" : sťparation de la phase aqueuse (
la plus dense) de la phase ťthťrťe contenant entre autre, le produit
organique de la synthŤse. La phase la plus dense occupe la partie basse
de l'ampoule ŗ dťcanter.
"La phase organique est sťchťe sur sulfate de magnťsium anhydre" : ťlimination des derniŤres traces d'eau de la phase organique.
" le solvant est ťvaporť" : distillation simple, l'ťther est trŤs volatil.
" un solide jaune qui est recristallisť dans l'ťthanol" : procťdť de purification.
Elle permet de sťparer le produit des
impuretťs en jouant sur la diffťrence de solubilitť du produit et des impuretťs dans
un solvant. On dissout l'ensemble ŗ chaud dans le volume miminum de solvant,
puis on laisse refroidir. Le produit
cristallise alors que les impuretťs doivent rester dans le solvant.
Les impuretťs sont solules ŗ chaud comme
ŗ froid dans le solvant ; le produit n'est soluble qu'ŗ chaud dans le
solvant.
Donner la structure du rťactif obtenu par addition d'hydrure de sodium sur le sel de phosphonium. Indiquer la nature du dťgagement gazeux. Prťciser le nom de la rťaction effectuťe. Donner la formule semi-dťveloppťe de A.
L'ion hydrure est une base trŤs forte, conjuguťe de l'acide H2.
On va donc observer un dťgagement de dihydrogŤne et le rťactif obtenu est un ylure de phosphore.
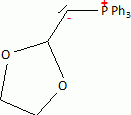
La rťaction de Wittig ( l'addition d'un ylure de phosphore sur un composť carbonylť ) donne un composť ťthylťnique.
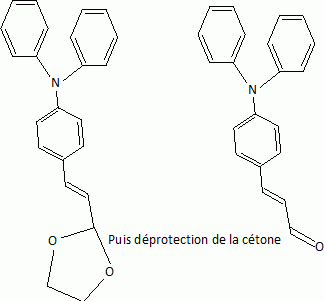
|
|









