Rťactions
de combustion et transfert thermique.
Rappeler
en une phrase le premier principe de la thermodynamique et exprimer la
variation de l'ťnergie interne et la variation d'enthalpie d'un systŤme
physico-chimique au repos en considťrant seulement le travail des
forces de pression.
Au cours d'une transformation d'un systŤme fermť,
la variation de son ťnergie est ťgale ŗ la quantitť d'ťnergie ťchangťe
avec le milieu extťrieur, sous forme de chaleur et de travail.
DU = W + Q.
Travail des forces de pression ŗ pression constante W = -P(Vfin
- Vdťbut ).
DU =Ufin - Udťbut = Q -P(Vfin -
Vdťbut ) ; Q = Ufin +PVfin -Udťbut-
PVdťbut ;
On dťfinit ainsi une autre fonction d'ťtat, la fonction enthalpie : H =
U + PV.
Q = Hfin - Hdťbut = DH.
La variation d'enthalpie lors d'une transformation ŗ pression constante
d'un systŤme thermodynamique, est ťgale ŗ la quantitť de chaleur
mise en jeu.
Dťfinir
l'enthalpie de rťaction et indiquer comment ťvolue l'enthalpie d'un
systŤme fermť siŤge d'une rťaction ŗ tempťrature et pression constante
en fonction de l'avancement de la rťaction.
La plupart des rťactions chimiques ont lieu ŗ pression constante.
L'enthalpie de rťaction permet de connaÓtre l'ťnergie libťrťe sous
forme de chaleur Q = DHT,
p.
Soit x l'avancement de la
rťaction : DHT,
p = x DrHT, p
avec DrHT, p :
enthalpie de rťaction en J mol-1.
Indiquer ŗ quoi
correspond l'enthalpie standard de formation d'un espŤce chimique.
Dťfinir les rťactions de formation en prenant comme exemples le
mťthane, l'eau et le mťthanol.
C'est l'enthalpie standard de rťaction DrHT, p de la rťaction de formation du corps pur ŗ
partir des corps simples stables dans l'ťtat standard T.
C(graphite) + 2 H2(g) = CH4(g)
H2(g) + ĹO2(g) = H2O(liquide)
C(graphite) + 2H2(g) + ĹO2(g) = CH4O(liquide).
Le pouvoir ťnergťtique (PE) d'un combustible ( en MJ kg-1)
correspond ŗ la quantitť d'ťnergie libťrťe lors de la combustion
complŤte d'un kg du combustible.
Calculer le PE pour
le carbone, le mťthane et l'hydrogŤne
C(graphite ) + O2(g) = CO2 (g) ; DrHT, p =
DfHT, p (CO2 (g)) - DfHT, p (O2 (g))- DfHT, p (C(graphite ))
DrHT, p
=-393 -0 -0 = -393 kJ mol-1 ; PE = -393*1000/12=3,28 104
kJ kg-1 = 32,8 MJ kg-1.
CH4(g) + 2O2(g) = CO2
(g) +2H2O(g) ; DrHT, p =
DfHT, p (CO2 (g)) +2 DfHT, p (H2O(g)) - 2DfHT, p (O2 (g))- DfHT, p (CH4(g))
DrHT, p
=-393 +2*(-242)-0 -(-75) = -802 kJ mol-1 ; PE =
-393*1000/16=5,01 104 kJ kg-1 = 50,1 MJ kg-1.
H2(g ) + ĹO2(g) = H2O(g) ; DrHT, p =
DfHT, p (H2O(g) - 0,5DfHT, p (O2 (g))- DfHT, p (H2(g ))
DrHT, p
=-242 -0 -0 = -242 kJ mol-1 ; PE = -242*1000/2=1,21 105
kJ kg-1 = 121 MJ kg-1.
|
Proposer une
expťrience simple, montrant les produits obtenus lors de la combustion
du carbone et du gaz de ville. Indiquer dans quelles conditions on peut
obtenir du carbone solide lors de la combustion du mťthane.
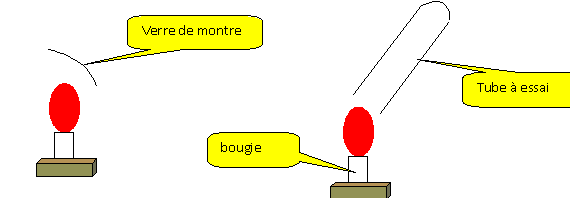
La partie froide du verre de
montre se couvre de buťe : la combustion de la bougie produit de l'eau.
Recueillir les gaz issus de la combustion de la bougie dans un tube ŗ
essais. Ajouter dans ce tube 2 mL d'eau de chaux. Boucher et agiter. L'eau de chaux se trouble : la
combustion de la bougie produit du dioxyde de carbone.
La combustion incomplŤte, dioxygŤne en dťfaut ou tempťrature peu
ťlevťe, donne du carbone solide.
|
Donner
la composition et une mťthode de prťparation de l'eau de chaux. Ecrire
les diffťrentes ťquations des rťactions qui interviennent lorsqu'on
fait barboter du dioxyde de carbone en continu dans l'eau de chaux.
Le lait de chaux
est obtenu en mťlangeant dans un bťcher un peu de chaux ťteinte (
solide blanc) avec 100 mL d'eau. Laisser dťcanter ;
filtrer : le filtrat obtenu est l'eau de chaux. L'eau de chaux est une
solution saturťe d'hydroxyde de calcium Ca(OH)2.
Le dioxyde de carbone, en prťsence d'eau de
chaux Ca(OH)2 donne un solide CaCO3.
Ca(OH)2 + CO2(g)
= CaCO3 (s) + H2O(l).
Le dioxyde de carbone en barbotant longtemps, rťagit avec l'eau, donne
un acide : le pH va donc diminuer et on observe une redissolution du
solide CaCO3 selon : CaCO3 (s) +CO2
(aq) + H2O = Ca2+ + 2HCO3-.
Un ťlŤve observe que lorsqu'on fait barboter de l'air dans l'eau de
chaux, il ne se passe rien mais que si l'air est inspirť puis expirťŗ
l'aide d'une paille dans de l'eau de chaux le test est positif.
Proposer
une explication ŗ cet ťlŤve en justifiant la prťsence de l'ťlťment
carbone.
A l'intťrieur des cellules de l'organisme, les rťaction
oxydantes consomment de l'oxygŤne pour dťgrader des matiŤres organiques
comme le glucose ou les lipides. Ce sont ces rťactions qui produisent
du CO2.La respiration, mouvement d'inspiration ( apport de
dioxygŤne ) -expiration ( rejet de dioxyde de carbone ) ventile le sang.
Le charbon.
Les rťserves mondiales de charbon sont extrÍmement importantes et
constituent pour certains pays la premiŤre source d'ťnergie. Le charbon
peut Ítre utilisť directement comme combustible ou pour la production
de dihydrogŤne.
Les oxydes de carbone.
Prťciser
le nombre d'oxydation maximal de l'ťlťment carbone. + IV.
Donner
les schťmas de Lewis du monoxyde de carbone et du dioxyde de carbone.
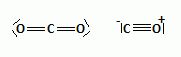
Le monoxyde de carbone est un composť toxique.
Indiquer
quel type de rťaction intervient lors de l'empoisonnement avec du
dioxyde de carbone. Que peuvent faire les pompiers pour essayer de
sauver une personne subissant cet empoisonnement ?
Le CO se lie aux sites ferreux de l'hťmoglobine, formant la
carboxyhťmoglobine, effet qui diminue la capacitť de transport en
oxygŤne du sang. Il faut soustraire immťdiatement la victime de
l'exposition, et lui faire inhalť du dioxygŤne pur ŗ l'aide d'un masque
ŗ oxygŤne bien ajustť.
Stabilitť thermique des
oxydes de carbone.
Indiquer
en quoi consiste l'approximation d'Ellingham.
On se place dans le cadre de l'approximation d'Ellingham : DrHį et DrSį
ne dťpendent pas de la tempťrature ( hors changement de phase ).
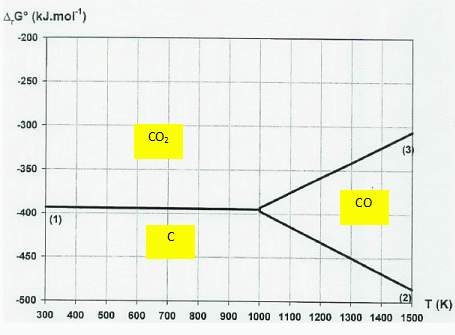
On donne le diagramme d'Ellingham pour C, CO et CO2 relatif
ŗ une mole de dioxygŤne.
Complťter
ce diagramme en prťcisant les espŤces qui prťdominent dans les
diffťrents domaines.
composť
|
C(s)
|
CO(g)
|
CO2(g)
|
O2(g)
|
DfHį kJ mol-1
|
0
|
-110
|
-393
|
0
|
Sį
J mol-1 K-1
|
6
|
197
|
213
|
205
|
Donner
l'ťquation des droites du diagramme.
(1) :
C(s) + O2(g) = CO2(g) ; DrHį = DfHį(CO2(g))=
-393 kJ mol-1 = -3,93 105 J mol-1.
DrSį =Sį(CO2(g))
- Sį(C(s)) -Sį(O2(g)) = 213-6-205=2 J mol-1 K-1.
DrGį =DrHį -TDrSį = -3,93 105 -2T.
(2) :
2C(s) + O2(g) = 2CO(g) ; DrHį
= 2DfHį(CO(g))=
-220 kJ mol-1 = -2,2 105 J mol-1.
DrSį =2Sį(CO(g)) -
2Sį(C(s)) -Sį(O2(g)) = 2*197-12-205=177 J mol-1 K-1.
DrGį =DrHį -TDrSį = -2,2 105 -177T.
(3) :
2CO(g) + O2(g) = 2CO2(g) ; DrHį = 2DfHį(CO2(g))
- 2DfHį(CO(g))=
-2*393+2*110=-566 kJ mol-1 = -5,66 105 J mol-1.
DrSį =2Sį(CO2(g))
- 2Sį(CO(g)) -Sį(O2(g)) = 426-6-2*197-205= -173 J mol-1
K-1.
DrGį =DrHį -TDrSį = -5,66 105 +173T.
Ecrire
l'ťquation de l'ťquilibre de Boudouard entre le carbone et ses deux
oxydes et calculer la variance de cet ťquilibre.
C(s) + CO2(g) = 2 CO(g)
3 constituants ; une relation entre les constituants ; 2 facteurs
physiques et 2 phases ( solide et gaz) : v = 3-1+2-2 =2.
Transformation du charbon en gaz
de synthŤse.
Le charbon peut Ítre utilisť pour la
production de dihydrogŤne par rťduction de la vapeur d'eau.
Tracer
sur le diagramme prťcťdent la droite correspondant au couple H2O(g)
/ H2(g).
2H2(g) + O2(g) = 2H2O(g) ; DrHį =-2*242 = -484 KJ
mol-1 = -4,84 105 J mol-1.
DrSį =2Sį(H2O(g))
- 2Sį(H2(g))
-Sį(O2(g)) = 2*189-2*130-205= -87 J mol-1 K-1.
DrGį =DrHį -TDrSį = -4,84 105 +87T.
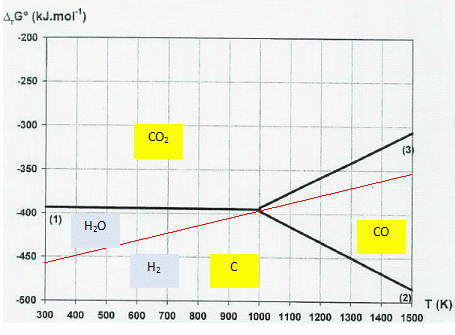
Dťterminer
les ťquilibres ŗ considťrer lorsque la vapeur d'eau est projetťe sur du
carbone en excŤs ŗ T = 800K et T = 1300 K.
T= 800 K : C(s) + 2H2O(g) = 2H2(g) + CO2(g).
(1)
T= 1300 K : CO(g) + H2O(g) = H2(g) + CO2(g).
(2)
Calculer les
constantes d'ťquilibre correspondant aux ťquilibres prťcťdents.
(1) : DrHį = DfHį(CO2(g))-2
DfHį(H2O(g))=
-393-2(-242) =91 kJ mol-1 = 9,1 104
J mol-1.
DrSį =Sį(CO2(g))
+2Sį(H2(g))-
Sį(C(s)) -2Sį(H2O(g))
= 213+260-6-2*189=89 J mol-1 K-1.
DrGį =DrHį -TDrSį = 9,1 104 -800*89
=19800 J mol-1.
DrGį = -RT
ln K1 ; ln K1 = -19800 / (8,31*800) = -2,98 ; K1 = 0,051.
(2) : DrHį = DfHį(CO2(g))-
DfHį(H2O(g))-DfHį(CO(g)) = -393-(-242)-
(-110) = -41 kJ mol-1 = -4,1 104 J mol-1.
DrSį =Sį(CO2(g))
+Sį(H2(g))-
Sį(CO(g)) -Sį(H2O(g))
= 213+130-197-189= -43 J mol-1 K-1.
DrGį =DrHį -TDrSį = -4,1 104
+1300*43 =14900 J mol-1.
DrGį = -RT
ln K2 ; ln K2 = -14900 / (8,31*1300) = -1,38 ; K2 = 0,25.
On veut
favoriser la formation de dihydrogŤne : il vaut mieux travailler
ŗ haute tempťrature ( K2 > K1)
Les
carburants.
Les carburants constituent environ 80 % des produits issus du
traitement du pťtrole. Les essences et le gazole peuvent Ítre
considťrťs comme un mťlange d'alcanes non cycliques.
Combustion des
carburants.
La combustion des carburants constitue la principale source ťnergťtique
utilisťe pour les transports. En plus de la diminution importante
des rťserves fossiles, leur utilisation massive crťe des problŤmes
environnementaux. L'ťmission de dioxyde de carbone par un vťhicule est
actuellement une donnťe importante qui est mise en avant pour l'achat
d'un vťhicule.
Indiquer
l'impact sur l'environnement d'une ťmission importante de dioxyde de
carbone.
Le dioxyde de carbone est un gaz ŗ effet de serre : il contribue au
rťchauffement global de la planŤte.
Donner la
formule d'une autre espŤce chimique courante qui pose le mÍme problŤme.
Le mťthane CH4, le protoxyde d'azote N2O.
La consommation d'un vťhicule et l'ťmission de CO2 doivent
obligatoirement apparaÓtre dans la fiche technique ou sur tout
affichage publicitaire. Pour une voiture ŗ essence de 120 ch les
donnťes suivantes sont indiquťes : - consommations en cycle urbain 11,2
L/100 km ; cycle extra-urbain : 6,4 L/100 km ; cycle mixte : 8,2 L /
100 km. Emission de CO2 : 194 g/km.
Au n iveau d'une classe de 1Ť S, on veut lors d'un exercice
de contrŰle, mettre en ťvidence la relation entre la consommation du
vťhicule et l'ťmission de CO2 qui est indiquťe. L'essence
sera considťrťe comme un mťlange d'isomŤre d'octane avec une densitť de
0,76.
Rťdiger
l'ťnoncť, justifier les ťtapes du questionnement retenu, donner la
rťsolution complŤte de l'exercice.
L'essence sera considťrťe comme un mťlange d'isomŤre d'octane C8H18
avec une densitť de 0,76. La consommation du vťhicule, en cycle mixte (
ville et campagne) et 8,2 L/100 km. On dťsire retrouver par le calcul,
l'indication de la fiche technique "194 g de CO2 par km".
Ecrire l'ťquation de la combustion complŤte de l'octane ; les produits
sont l'eau et le dioxyde de carbone.
C8H18
(l)+ 12,5O2(g) =8 CO2 (g)+ 9H2O(g)
Calculer la masse molaire de l'octane. M = 8*12+18 =114 g/mol.
Calculer la masse de 8,2 L d'essence. m = 8,2 * 0,76 = 6,232 ~6,2 kg
Calculer la quantitť de matiŤre d'octane : n = m/M = 6232/114 = 54,67 ~
55 mol.
En dťduire la quantitť de matiŤre de CO2 ( on pourra dresser
un tableau d'avancement) : 8*54,67 =437,3 mol.
En dťduire la masse de CO2 produit pour 100 km puis pour 1
km : 437,3*44 = 19,2 kg soit 0,192 g par km.
Toujours en classe de 1Ť S, on cherche ŗ calculer l'ťnergie
totale ( J) dťpensťe par le vťhicule prťcťdent lorsqu'il parcourt 100
km ŗ 90 km/h.
Indiquer
les ťtapes du raisonnement qui doit Ítre mis en place avec les ťlŤves
pour donner les ťlťments de rťponse ŗ cette question.
Pour calculer la chaleur de rťaction de combustion de l'octane, on
considŤrera que l'octane est en phase gazeuse.
On donne les enthalpies standard de dissociation de liaison :
liaison
|
C-C
|
C-H
|
C=O
|
O=O
|
OH
|
DdHį( kJ/mol)
|
345
|
415
|
804
|
497
|
463
|
Etablir la liste des
liaisons rompues ( rťactifs) et de liaisons crťťes ( produits).
Calculer l'ťnergie mise en oeuvre lors de la combustion complŤte d'une
mole d'octane.
Calculer la masse de 6,2 L d'essence ( 100 km parcourus ŗ 90 km/h).
Calculer la quantitť de matiŤre d'octane.
Calculer l'ťnergie consommťe lors de ce trajet.
|
Les
agrocarburants.
L'utilisation des biocarburants, tels que l'ťthanol issus de la
biomasse et les esters mťthyliques d'huiles vťgťtales ( diester) est
proposťe pour diminuer l'inmact de l'ťmission de dioxyde de carbone par
les moteurs thermiques.
Expliquer
pourquoi l'utilisation des agrocarburants contribue ŗ diminuer
l'ťmission de dioxyde de carbone.
Lors de leur croissance les plantes fixent le dioxyde de carbone de
l'air. Ces plantes conduisent aux agrocarburants. La combustion des
biocarburants libŤrent du dioxyde de carbone. Le bilan carbone est nul.
Donner
la formule gťnťrale d'un triglycťride d'une huile vťgťtale.
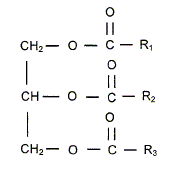
R1, R2,
R3 chaines carbonťes saturťes ou insaturťes.
Un diester est obtenu par traitement de
l'huile vťgťtale par un excŤs de mťthanol soit en prťsence d'un
catalyseur acide comme l'acide sulfurique, soit par catalyse basique
avec du mťthanolate de sodium.
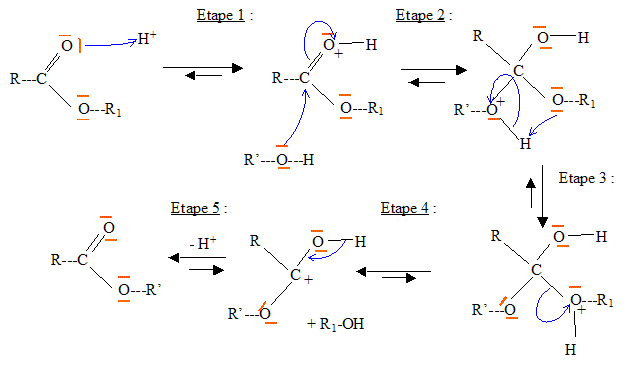
Indiquer
la formule du produit obtenu en plus du diester et donner le nom de la
rťaction effectuťe.
La transestťrification
correspond ŗ la rťaction chimique suivante :
Ester
1 + alcool = Ester 2 + autre alcool.
La transestťrification de glycťrides donne du glycťrol
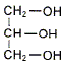 et des eters mťthyliques. et des eters mťthyliques.
|
|

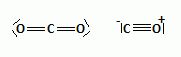



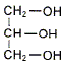 et des eters mťthyliques.
et des eters mťthyliques.