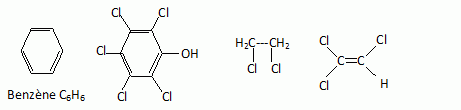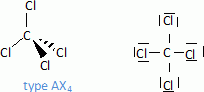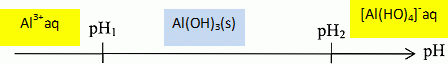Partie 1.
(4 points)
Ecrire
les formules du benzŤne, du 1,2-dichloroťthane, le pentachlorophťnol,
le trichloroťthylŤne ou 1,1,2-trichloroťthŤne.
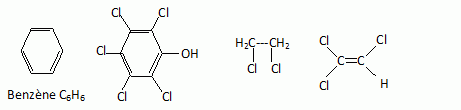
Ecrire la
formule semi-dťveloppťe du 1,4-hydroxynonylbenzŤne ou paranonylphťnol.
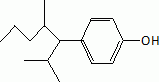
Donner la
reprťsentation de Lewis du tťtrachlorure de carbone puis le type de
gťomťtrie spatiale de cette molťcule selon la mťthode VSEPR. En faire
la reprťsentation.
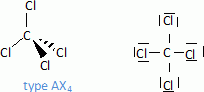
Electrocoagulation,
traitement de l'eau polluťe.(9 points )
Le coagulant est libťrť dans l'effluent in situ, en utilisant la
dissolution d'une anode sacrificielle, le plus souvent en aluminium ou
en fer. Lors de l'alimentation des ťlectrodes en courant, il y a
simultanťment une dissolution du mťtal ŗ l'anode et un dťgagement de
dihydrogŤne au voisinage de la cathode.
La dissolution de l'anode conduit ŗ la formation d'hydroxydes
mťtalliques entre autre. Ces composťs sont gťnťralement une meilleure
efficacitť de coagulation que celle des produits chimiques utilisťs
dans les techniques conventionnelles ( ajout de sulfate d'aluminium ou
de chlorure ferrique. Le dťgagement de dihydrogŤne sous forme de bulles
contribue fortement ŗ l'agitation du milieu et, dans certains cas,
favorise la flottation des solides formťs ( absorbant-polluant ).
|
Soit
la description simplifiťe d'un module d'ťlectrocoagulation : deux
ťlectrodes, dont une anode en aluminium, sont reliťes ŗ une source de
courant continu et plongent dans le bac contenant un effluent aqueux ŗ
traiter.
La nature de la cathode n'a pas besoin d'Ítre prťcisťe dans l'ťtude ŗ suivre.
Le couple mis en jeu ŗ l'anode est Al3+aq/ Al(s).
Donner pour chaque espŤce le degrť d'oxydation.
Le degrť d'oxydation de l'aluminium est nul dans Al(s) et vaut + III dans l'ion Al3+aq.
|
Ecrire la rťaction ŗ l'anode. S'agit-il d'une oxydation ou d'une rťduction ?
Une oxydation se produit ŗ l'anode positive : Al(s) = Al3+aq + 3e-.
A la cathode, l'eau est la source de dťgagement de dihydrogŤne. Le couple redox mis en jeu est H2O(l) / H2(g).
Ecrire
la rťaction ŗ la cathode, en milieu acide, puis en milieu basique.
Rťduction ŗ la cathode nťgative : 2e- + 2 H+aq = H2(g) en milieu acide.
2H2O(l) +2e-= H2(g) +2HO-aq en milieu basique.
S'agit-il d'une oxydation ou d'une rťduction ? Justifier.
H+aq ou H2O(l) gagnent des ťlectrons ; ce sont des oxydant qui se rťduisent ( rťduction).
On veut calculer la tension ŗ appliquer au module d'ťlectrocoagulation dans le cas d'un milieu acide.
Donner les relations de Nernst pour les deux couples prťcťdents.
E1 = Eį( Al3+aq/ Al(s)) + 0,02 log [ Al3+aq].
E2 = Eį( H+aq/ H2(g)) + 0,03 log( [ H+aq]2 / PH2).
Calculer le potentiel de chaque ťlectrode ŗ pH=3.
Potentiel standard ŗ pH=0 : Eį( Al3+aq/ Al(s))= -1,66 V ; Eį( H+aq/ H2(g)) = 0,00 V ; PH2= 1 bar ; [ Al3+aq] = 1 mol/L.
E1 = -1,66 V ; E2 =0,00 + 0,03 log 10-6 = -0,18 V.
En dťduire la tension minimale thťorique ŗ appliquer pour observer la dissolution de l'ťlectrode d'aluminium ŗ pH=3.
E1 - E2 =-0,18 +1,66 = 1,48 ~1,5 V.
Comment expliquer, qu'en pratique, il faut imposer une tension supťrieure ŗ celle calculťe prťcťdemment.
Certaines rťactions sont lentes ; le dihydrogŤne peut s'adsorber sur la cathode.
Lors
du fonctionnement du module d'ťlectrocoagulation, l'espŤce aluminium
apparaÓt majoritairement en fonction du pH, soit sous forme d'ion Al3+aq, soit sous la forme d'hydroxyde d'aluminium Al(OH)3(s), soit sous forme de complexe tťtrahydroxoaluminate (III) [Al(OH)4]-aq.
Ecrire l'ťquation de la rťaction de prťcipitation de
Al(OH)3(s).
Al3+aq+ 3HO-aq =Al(OH)3(s)
Soit pH1, le pH de dťbut de prťcipitation de Al(OH)3(s).
Le calculer pour une concentration en Al3+aq notťe C1 = 1,00 mol/L.
On donne le produit de solubilitť de Al(OH)3(s) : Ks1 = 10-33.
Ks1 = 10-33 =[Al3+aq][HO-aq]3 ; [HO-aq]3 =10-33 ; [HO-aq] = 10-11 mol/L ;
[H3O+aq] = 10-14 / [HO-aq]= 10-14 / 10-11 = 10-3 mol/L ; pH1 = 3,0.
Soient les rťactions : Al(OH)3(s) +HO-aq = [Al(OH)4]-aq ; K2.
Al3+aq + 4 HO-aq = [Al(OH)4]-aq ; K3 = 1035 ŗ 25įC.
Exprimer les constantes d'ťquilibre K2 et K3.
K2= [[Al(OH)4]-aq] / [HO-aq]. K3= [[Al(OH)4]-aq] / ([HO-aq]4[Al3+aq] ).
En dťduire l'expression de K2 en fonction de K3 et Ks1. Calculer K2.
Ks1= ([HO-aq]3[Al3+aq] ).
K3= [[Al(OH)4]-aq] / ([HO-aq]4[Al3+aq] ) = [[Al(OH)4]-aq] /( [HO-aq]Ks1)= K2 /Ks1.
K2= K3 Ks1= 1035 10-33 =100.
Vťrifier que le pH de redissolution totale de l'hydroxyde Al(OH)3 (s) est ŗ 25įC : pH2 = 12.
K2= [[Al(OH)4]-aq] / [HO-aq] avec [[Al(OH)4]-aq] = 1,00 mol/L.
[HO-aq] = 1/K2 : 1 / 100 = 10-2 mol/L.
[H3O+aq] = 10-14 / [HO-aq]= 10-14 / 10-2 = 10-12 mol/L ; pH2 = 12.
Complťter
le diagramme ci-dessous en indiquant sous quelle(s) forme(s)
dissoute(s) se trouve l'espŤce aluminium dans les 3 intervalles de pH.
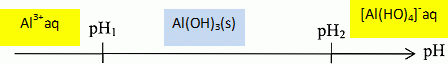
Ceci
justifie que dans la pratiquede l'ťlectrogoagulation, l'opťration
s'effectue sur des effluents de pH 5 ŗ 8. Dans ces conditions, la
solubilitť de l'hydroxyde amphotŤre est faible et la prťsence de
complexes chargťs nťgativement est minimisťe. Rappelons que les charges
nťgatives stabilisent les colloÔdes qui ne peuvent plus coaguler.
Partie 3.
(3 points)
L'alumine Al2O3(s) est une forme dťshydratťe de
l'hydroxyde d'aluminium. L'ion aluminate est une espŤce soluble de
formule AlO2-aq.
D'aprŤs
le diagramme potentiel-pH, prťciser pour les zones A, B, C et D, s'il
s'agit d'une zone de corrosion, passivation ou d'immunitť.
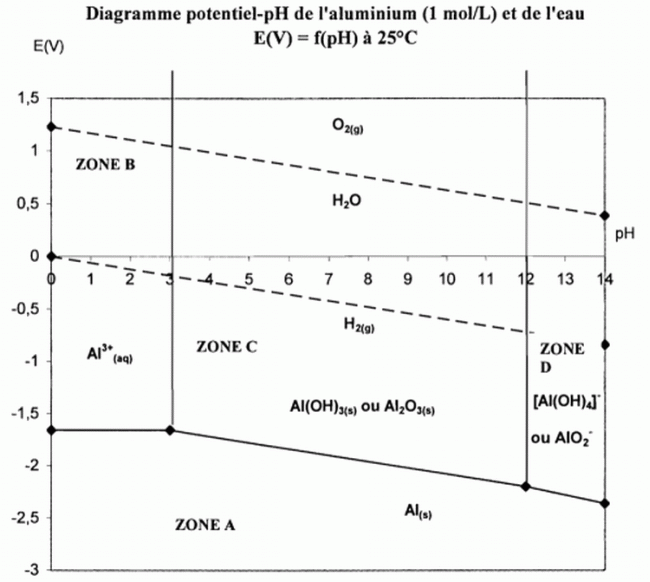
Zone A : zone de
stabilitť thermodynamique du mťtal Al, donc immunitť thermodynamique.
Zone B :
l'ťlťment aluminium est sous forme d'ion Al3+aq en solution
donc corrosion.
Zone C : l'ťlťment
aluminium est sous forme d'oxyde Al2O3(s)
protecteur
du mťtal, donc passivation.
Zone D : l'ťlťment
aluminium est sous forme d'ion AlO2-aq en solution donc
corrosion.
Un ťtudiant affirme
: " le dioxygŤne dissout rťagit avec le mťtal aluminium quel que soit
la valeur du pH".
A-t-il
raison ou tord ?
Al et O2
appartiennent ŗ des domaines disjoints quel que soit le pH. Le
dioxygŤne est capable d'oxyder le mťtal quel que soit le pH. L'ťtudiant
a raison.
L'eau rťagit
avec le mťtal aluminium, quel que soit le pH.
Justifier
cette affirmation. Ecrire le bilan de cette rťaction ŗ pH=7.
Couples redox : Al2O3(s)
/Al(s) et H2O(l) / H2(g).
Al et H2O
appartiennent ŗ des domaines disjoints quel que soit le pH. L'aluminium
est capable de rťduire l'eau quel que soit le pH.
2 Al(s) +3H2O(l)= Al2O3(s)
+ 6e- + 6H+.
3 fois { 2H++2e- =
H2(g) }.
2 Al(s) +3H2O(l)= Al2O3(s)
+ 3H2(g).
Dťcrire
succinctement le phťnomŤne de passivation.
En
prťsence de dioxygŤne de l'air le mťtal aluminium s'oxyde en
alumine : cette oxyde forme une couche protectrice. Le mťtal n'ťtant
plus en contact avec le dioxygŤne, l'oxydation s'arrÍte.
Au
niveau de l'anode de la cellule d'ťlectrocoagulation, l'aluminium
rťagit spontanťment en prťsence de dioxygŤne et d'eau pour former une
couche d'oxyde d'alumine. On se demande alors comment dans la pratique
l'EC peut Ítre efficace pour les pH intermťdiaire ( 5 ŗ 8 ).
Comment l'anode en
aluminium recouverte d'alumine peut-elle Ítre dissoute en ion Al3+
aq ?
Lorsque la diffťrence de potentiel appliquťe entre les deux ťlectrodes
est suffisamment importante, et gr‚ce ŗ la prťsence d'ion chlorure (
ťventuellement rajoutťs ŗ l'effluent ), la corrosion a lieu par
piqŻres. Les ions chlorures fragilisent les couches successives
d'alumine plus ou moins poreuses.
|
Partie 4.
( 4 points ).
Un pilote d'ťlectrocoagulation est constituť d'une cuve et de deux
ťlectrodes reliťes ŗ un gťnťrateur de courant continu. Les ťlectrodes
sont des plaques d'aluminium rectangulaires de surface active S de 175
cm2 et distantes de L = 2,0 cm. L'intensitť de travail
I est de 5,0 A. Une pompe alimente le pilote en effluent d'une
inductrie textile, avec un dťbit D de 600 L h-1.
L'effluent traitť prťsente une conductivitť g de 2,4 mS cm-1.
On donne l'expression de la rťsistance de
l'effluent entre les ťlectrodes R = L / (gS) en ohm.
Calculer la rťsistance de la solution entre les ťlectrodes.
gS
= 2,4*175 = 420 mS cm = 0,42 S cm ; 1
/ (gS) =2,38 S-1 cm-1 ; L / (gS) =2,0 *2,38 =4,76 ~4,8 S-1 ou W.
Exprimer
et calculer la puissance dissipťe par effet Joule lorsque le module
d'ťlectrocoagulation fonctionne.
P = R I2
=4,76 *5,02 = 119 ~ 1,2
102 W.
Vťrifier que
l'ťnergie dissipťe par effet Joule en une heure est 4,3 105 J.
W = P t = 119*3600 = 4,3 105 J.
On rťalise un bilan ťnergťtique sur une heure de fonctionnement du
module.
Evaluer
la variation de tempťrature
DT au
cours du traitement de l'effluent.
On donne ceffluent =4185 J kg-1 K-1 ; reffluent =1000 kg m-3.
Masse d'effluent par heure : m =D
reffluent
=0,600*1000 = 600 kg h-1.
Energie reÁue par l'effluent : m ceffluent
DT = 4,3 105
J.
DT =4,3
105 / (600*4185) =0,17 įC.
En
appliquant la loi de Faraday, ťvaluer la variation de la masse de
l'anode en aluminium Dm aprŤs une heure de
fonctionnement.
Quantitť d'ťlectricitť : Q = I t = 5,0*3600 =1,8 104 C.
Quantitť de matiŤre d'ťlectrons : ne- = 1,8
104 /96485 =0,1866 mol.
Al(s) = Al3+aq + 3e-.
Quantitť
de matiŤre d'aluminium n = ne-
/3 = 6,22 10-2 mol.
Dm = n M(Al) = 6,22
10-2*27 =1,68 ~1,7
g h-1. |
|
|
|