Le récepteur
solaire.
Les systèmes ‘parabole-moteur' sont destinés à l'électrification
décentralisée car leur puissance varie de quelques centaines de Watts à
quelques dizaines de kW. Ils sont destinés, par exemple, à
l’électrification de villages isolés.
Cette réalisation s'inscrit dans le cadre du projet international «
EnviroDish » financé par le Ministère allemand de l'Environnement et
plusieurs industriels de ce pays.
Il a pour objectif d'implanter sur différents sites (Espagne, Italie,
Allemagne, France, Inde) des systèmes « Parabole-Stirling » afin d’en
mesurer l'efficacité dans différentes conditions d'ensoleillement.

On
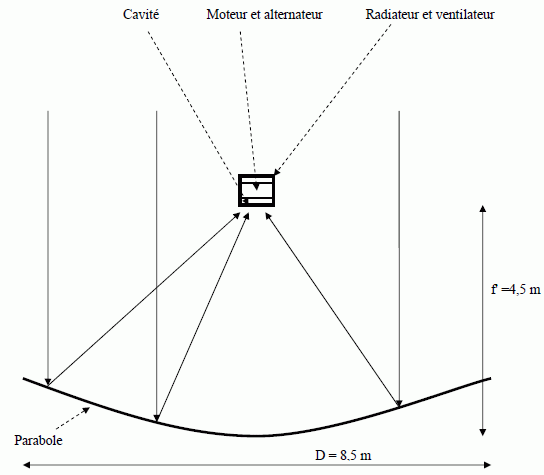
distingue sur cette photographie :
- la parabole servant à concentrer le rayonnement solaire ;
- le bloc « moteur Stirling et alternateur » permettant de transformer
l’énergie solaire en énergie électrique.
Le
concentrateur solaire.
Les
caractéristiques du concentrateur (réflecteur parabolique ou
"parabole") sont :
diamètre, 8,5 m ; surface projetée (collectrice), 56,7 m2 ;
distance focale, 4,5 m ; réflectivité, 94%.
On supposera que l'ensoleillement E est de 1000 W.m-2
("ensoleillement standard optimal").
Quelle est alors la
puissance du rayonnement solaire reçue par la parabole ?
Puissance reçue = ensoleillement fois surface collectrice
Preçue = 1000*56,7 =5,67 104 W.
Quelle est alors la
puissance transmise au capteur ?
94% de cette puissance est réfléchie vers le capteur :
Ptransmise = 5,67 104
*0,94 =5,33
104 W.
Le
moteur Stirling.
Cette machine thermique utilise un gaz qui reçoit de la chaleur d'une
source chaude (la cavité) et qui fournit de la chaleur à une source
froide (le radiateur à refroidissement à eau) et du travail à
l’alternateur.
La cavité assure le transfert thermique vers le gaz de l’énergie de
rayonnement solaire qu’elle reçoit.
Les caractéristiques du moteur Stirling (SOLO 161) sont :
- gaz utilisé : dihydrogène ;
- pression de fonctionnement : 20-150 bar ;
- température de fonctionnement : 650 °C.
Pour un éclairement de 1000 W.m-2, l’alternateur triphasé
400V-50Hz fournit une puissance électrique utile de 9,8 kW.
Rendement, puissance,
énergie.
Dans ces conditions d’éclairement (1000 W.m-2), la puissance
du rayonnement solaire reçue est de 53 kW.
Calculer
le rendement hT du dispositif.
hT
= puissance électrique utile / puissance reçue = 9,8 / 53 =0,185 ( ~18 %)
Le
comparer à celui d’une installation photovoltaïque sachant que le
rendement des meilleures photopiles (au silicium monocristallin) est de
l'ordre de 15 à 22 % dans ces mêmes conditions d’éclairement.
Le rendement de ce générateur solaire est comparable à celui
d'une installation photovoltaïque, dans les mêmes conditions
d'éclairement.
En supposant que le
rendement de l'alternateur hA est de l'ordre de
92%, estimer le rendement hS du moteur Stirling.
hT =hA * hS ; hS = hT / hA = 0,185 / 0,92 =0,20
( 20 %).
La puissance fournie au gaz par la source chaude est de 53 kW. La
puissance mécanique fournie à l’alternateur est de 10,5 kW.
Quelle
puissance le gaz cède-t-il à la source froide ?
Cette machine
thermique utilise un gaz qui reçoit de la chaleur d'une source chaude
et qui fournit de la chaleur à une source froide et du travail à
l’alternateur.
Puissance dédée à la source froide = 53-10,5 = 42,5 kW.
La vitesse de rotation du moteur est de
1500 tours par minute.
Sachant
qu’un tour du moteur correspond à un cycle thermodynamique, calculer la
durée d’un cycle.
1500/60 = 25 tours ( cycles ) par seconde.
Durée d'un cycle : 1/25 = 0,040 s = 40 ms.
Calculer,
pour un cycle, le travail W fourni par le moteur Stirling.
Travail ( kJ) = puissance ( kW) * durée (seconde)
W = 10,5 * 0,040 = 0,42 kJ = 420 J.
Etude du cycle
théorique de Stirling.
On se
propose dans cette partie de calculer le rendement théorique d’un cycle
de Stirling. On rappelle que le cycle théorique du moteur Stirling est
constitué de quatre transformations réversibles (dont deux sont
isothermes). Le dihydrogène est considéré comme un gaz parfait.
Sur le diagramme de Clapeyron ci-dessous, une des transformations
isothermes a lieu à la température qf
= 70 °C et l'autre à la température qc
= 650 °C.
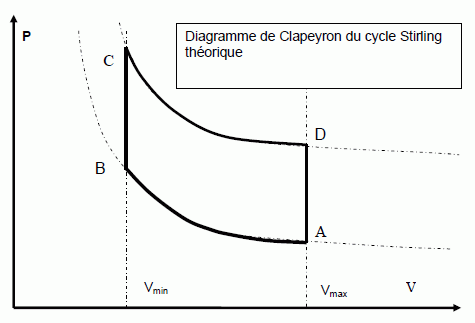
Au
point C la pression est de 15.106 Pa et la température de
650 °C.
Le volume de gaz évolue entre les valeurs Vmin = 184,5 cm3
et Vmax = 344,5 cm3.
On donne : - constante de gaz parfaits : R = 8,32 J.mol-1.K-1
- travail de compression isotherme d'un gaz parfait : W12 =
nRT Ln(V1/ V2)
- relation T(K) = 273 + q(°C).
Donner le
nom de chacune des transformations AB, BC, CD, DA, en indiquant s'il
s'agit de détentes ou de compressions.
Préciser
la transformation au cours de laquelle le gaz fournit du travail.
AB : compression isotherme où le gaz échange de la chaleur avec
la source froide, température qf = 70 °C et reçoit du
travail.
BC :
compression isochore ( pas de travail échangé )
CD : détente isotherme où le gaz échange de la chaleur avec la
source chaude, température qc = 650 °C et cède du
travail à l'extérieur.
DA :
détente isochore ( pas de travail
échangé ).
Montrer que le nombre de moles de gaz mises en jeu est n= 0,36 mol.
Loi des gaz parfaits : n = PC Vmin / (RTC) = 15.106 *184,5 10-6 / (8,32 *(650+273)) =0,36 mol.
Calculer la pression correspondant au point D du diagramme.
La transformation CD est isotherme : TD = TC = 273+650 =923 K.
PC = nRTC / Vmax =0,36 * 8,32 * 923 / 344,5 10-6 =8,025 106 ~8,0 106 Pa.
Calculer le travail WAB et le travail WCD reçus par le gaz lors des transformations AB et CD.
WAB =
nRTA Ln(Vmax/ Vmin) = 0,36*8,32*(273+70) ln (344,5 / 184,5) =641,5 J ~6,4 102 J.
WCD =
nRTC Ln(Vmin/ Vmax) = 0,36*8,32*(273+650) ln (184,5 / 344,5) = -1726,3 J~ -1,7 103 J.
Justifier que la variation de l'énergie interne du gaz lors des transformations AB et CD est nulle.
Au cours de l'évolution isotherme d'un gaz parfait, l'énergie interne
du gaz reste constante ; l'énergie interne d'un gaz parfait dépend de
la température.
En déduire les chaleurs QAB et QCD reçues par le gaz durant ces mêmes transformations.
DU =QAB +WAB =0 ; QAB = - WAB = -6,4 102 J.
DU =QCD +WCD =0 ; QCD = - WCD = 1,7 103 J.
Calculer le travail reçu par le gaz lors d'un cycle.
W = WAB + WBC + WCD + WDA=641,5 +0 -1726,3 +0 = -1085 ~-1,1 103 J.
On suppose que la chaleur n'est fournie au gaz que lors de la transformation CD.
Définir et calculer alors le rendement thermodynamique théorique hTh de ce moteur (ce rendement théorique est, pour des raisons de modélisation, très supérieur au rendement réel mesuré).
hTh = énergie utile / énergie dépensée = |W| / QCD =1085 / 1726 =0,63 ( 63 %).
|
Etude acoustique du moteur Stirling.
Le moteur utilisé produit un bruit de niveau L1 = 60 dB à une distance de 1 m.
On considère que l'émission sonore est la même dans toutes les directions.
On rappelle l’expression du niveau sonore en fonction de l’intensité : L = 10 log I/I0 avec I0 = 1,0 10-12 W m-2.
Calculer l'intensité acoustique I1 à 1 mètre du moteur.
I1 = I0 10 0,1 L =1,0 10-12 * 106 =1,0 10-6 W m-2.
En déduire la puissance acoustique du moteur.
Aire d'une sphère de rayon r = 1,0 m : A = 4 pr2 = 4*3,14 = 12,56 m2.
Puissance acoustique = A I1 = 12,56 *1,0 10-6 =1,256 10-5 ~ 1,3 10-5 W.
Calculer l'intensité sonore I20 à 20 mètres du moteur.
Aire d'une sphère de rayon r = 20 m : A = 4 pr2 = 4*3,14*202 = 5024 m2.
I20 = puissance acoustique / A = 1,256 10-5 / 5024 =2,5 10-9 W m-2.
En déduire le niveau d'intensité sonore L20 à cette même distance. Peu-on considérer que le moteur Stirling est nuisant d’un point de vue sonore ?
L20 = 10 log I20/I0 = 10 log 2,5 10-9 / 10-12 = 34 dB.
Cela correspond à une conversation à voix basse : ce moteur n'est
pas une source de nuisance sonore à une distance de 20 m.
Intérêt de la solution du point de vue environnemental.
On
se propose d’évaluer la réduction des rejets de dioxyde de carbone
obtenue par ce type d’installation solaire. On cherchera donc à
calculer la quantité de CO2 produite par une installation de puissance identique utilisant le méthane comme
combustible.
Données :
L'énergie thermique produite par la combustion d'une mole de méthane (CH4) est de 810 kJ, l'eau formée restant sous forme de vapeur. Les masses molaires : M(C) = 12 g.mol-1 M(O) = 16 g.mol-1 M(H) = 1 g.mol-1 M(N) =14 g.mol-1
Le volume molaire à 20 °C : V M = 24 L.mol-1.
La puissance thermique fournie est de 53 kW.
Calculer en joule l’énergie produite pendant une heure de fonctionnement.
énergie ( J) =puissance (W) * durée (s)
W = 53 103 *3600 = 1,908 108 ~1,9 108 J.
Calculer le nombre de moles de méthane consommé pendant cette durée.
n = 1,908 108 / 810 103 =2,3555 102 ~2,36 102 moles.
En déduire le volume, en mètre cube, de méthane consommé en une heure de fonctionnement. Le gaz est stocké à une température de 20 °C.
V = n VM = =2,3555 102 *24 =5,65 103 L = 5,65 m3.
Écrire l'équation de la combustion complète du méthane.
CH4 +2 O2 = CO2 +2H2O.
En déduire la masse de dioxyde de carbone produite par la combustion d'une mole de méthane.
Une mole de méthane donne une mole de dioxyde de carbone soit 12+2*16 = 44 g de CO2.
Le brûleur fournissant une puissance thermique de 53 kW, calculer la masse de dioxyde de carbone formée pendant une heure de fonctionnement.
44*nCO2 = 44*2,3555 102 ~1,03 104 g = 10 kg.
|
|
|
|