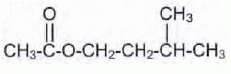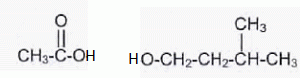L'eau,
bien prťcieux qupeut se faire rare dans de nombreuses rťgions, est
essentielle dans diffťrents domaines comme par exemple :
- en biologie : l'eau est le principal constituant des tissus animaux
et vťgťtaux
- dans l'idustrie :l'eau se prŤte ŗ des applications nombreuses et
variťes. ( solvant, agent de lavage et de rťfrigťration, matiŤre
premiŤre )
L'eau
en tant que boisson.
Les indications portťes sur une bouteille d'eau minťrale sont les
suivantes :
calcium Ca2+ : 555 mg/L ; magnťsium Mg2+ : 110
mg/L ; sodium Na+ : 14 mg/L ; hydrogťnocarbonate : HCO3- : 403 mg/L
rťsidu sec ŗ 180įC :1850 ; pH = 7,0.
pKa1(CO2, H2O/HCO3- ) =6,4 ; pKa2(HCO3- /CO32-)
=10,3. Masse molaire de HCO3- : 61 g/mol.
L'ion hydrogťnocarbonate.
Ecrire
les demi-ťquations acido-basiques associťes ŗ cet ion.
HCO3- aq = CO32- aq + H+aq.
HCO3- aq + H+aq= CO2, H2O
Tracer le
diagramme de prťdominance des espŤces acides et basiques des couples
auquels appartient l'ion hydrogťnocarbonate.
Quelle espŤce prťdomine dans l'eau minťrale ?

A pH=7, infťrieur ŗ pKa2, supťrieur ŗ pKa1, la
forme HCO3- aq prťdomine.
|
Teneur en ion hydrogťnocarbonate
:
On prťlŤve un volume V1 = 20 mL d'eau minťrale auquel est
additionnťe progressivement une solution d'acide chlorhydrique de
concentration C= 1,0 10-2 mol/L.
La rťaction chimique qui se produit s'ťcrit :
HCO3- aq +H3O+aq = CO2, H2O aq + H2O (1)
Donner
l'expression
du quotient de rťaction.
Qr, = [CO2, H2O aq]/ ([H3O+aq] [HCO3- aq] ).
Montrer
que Qr, ťq =2,5 106. Cette valeur
dťpend-elle de la composition initiale du systŤme ?
HCO3- aq + H+aq= CO2, H2O ; Ka1
= [CO2, H2O aq]/ ([H+aq] [HCO3- aq] ).
Qr, ťq =1 / Ka1 =1/ 10-6,4 =106,4
=2,5 106.
Cette valeur ne dťpend
pas de la composition initiale du systŤme ; elle ne dťpend que de la
tempťrature.
Prťciser,
sans calcul, la valeur du taux d'avancement ŗ l'ťquilibre, si
l'on veut utiliser la rťaction chimique (1) pour le dosage des ions
hydrogťnocarbonate. Justifier.
Une rťaction chimique, support d'un dosage doit Ítre rapide et totale :
le taux d'avncement ŗ l'ťquilibre vaut donc 1.
|
Dťfinir
l'ťquivalence d'un dosage.
A
l'ťquivalence, les rťactifs sont en proportions stoechiomťtriques ;
avant l'ťquivalence, l'un des rťactifs est en excŤs, aprŤs
l'ťquivalence, l'autre rťactif est en excŤs.
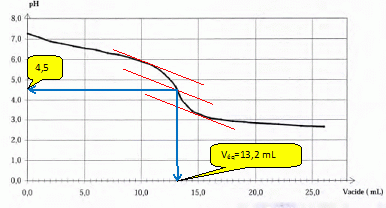
Dťterminer les
coordonnťes du point d'ťquivalence.
Calculer
la concentration des ions hydrogťnocarnonate dans cette eau. La
comparer avec l'indictaion de la bouteille.
A l'ťquivalence CVťq = C1V1 ; C1=CVťq
/V1 =0,010*13,2 / 20 = 6,6 10-3 mol/L.
Titre massique en ion hydrogťnocarbonate : 61*6,6 10-3 ~0,40
g/L = 4,0 102 mg/L ( en accord avec l'indication )
Le
dosage des ions hydrogťnocarbonate peut-il Ítre rťalisť par
colorimťtrie en utilisant un indicateur colorť ? Justifier et choisir
l’indicateur le plus appropriť dans la liste.
Vert de bromocrťsol : jaune 3,8 – 5,4 bleu
Bleu de bromothymol : jaune 6,0 – 7,5 bleu
PhťnolphtalťÔne : incolore 8,2 – 10,0 rose.
Toutes les espŤces, rťactifs et produits, sont incolores ; le dosage
peut Ítre suivi par colorimťtrie en utilisant un indicateur colorť.
La zone de virage de l'indicateur doit contenir le pH du point
ťquvalent ( pH=4,5). Le vert de bromocrťsol convient.
L’eau en chimie
organique :
Les esters, des
molťcules odorantes :
Les esters et les produits de leur hydrolyse sont des espŤces chimiques
trŤs rťpandues dans la nature. L’acťtate d’isoamyle est l’un des esters
ŗ odeur fruitťe contenus dans les bananes. Sa formule semi-dťveloppťe
est la suivante :
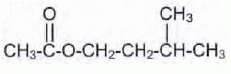
La synthŤse de l’acťtate d’isoamyle peut Ítre rťalisťe ŗ partir de deux
rťactifs : l’acide ťthanoÔque ou acťtique et le
3-mťthylbutan-1-ol ou alcool isoamylique.
Ecrire les formules semi-dťveloppťe des deux rťactifs citťs.
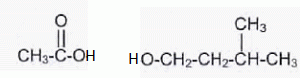
Dans un montage ŗ reflux, on introduit 6,5 g d’acťtate d’isoamyle et
0,90 g d’eau. Le mťlange rťactionnel est chauffť pendant une heure ŗ
75įC environ.
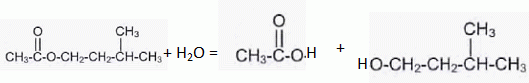
Ecrire l’ťquation de la rťaction produite.
Calculer les quantitťs de matiŤre initiales d’ester et d’eau
introduites dans le mťlange rťactionnel.
M(ester) =7*12+14+2*16 = 130 g/mol
n(ester) = m/M = 6,5 / 130 = ,050 mol ; n(eau) = m/M(eau) = 0,90/18 = 0,05 0 mol.
Le quotient de rťaction ŗ l’ťquilibre pour cette rťaction est Qr
ťq = 0,25.
Calculer le quotient de rťaction initial et dťduire le sens d’ťvolution
du systŤme chimique.
Qr i = [acide ťthanoÔque]i [alcool isoamylique]i / ( [ester]i[eau]i)
Or [acide ťthanoÔque]i =[alcool isoamylique]i =0 donc Qr i = 0.
Qr i < Qr
ťq : le systŤme chimique ťvolue dans le sens direct.
Complťter le tableau d’avancement et dťterminer l’avancement ŗ l’ťtat
d’ťquilibre.
|
avancement (mol)
|
ester
|
eau
|
acide ťthanoÔque
|
alcool isoamylique
|
initial
|
0
|
0,05
|
0,05
|
0
|
0
|
en cours
|
x
|
0,05-x
|
0,05-x
|
x
|
x
|
ťquilibre
|
xťq
|
0,05-xťq |
0,05-xťq |
xťq |
xťq |
Qr
ťq = 0,25 = [xťq / (0,05-xťq)]2 ; 0,5 =xťq / (0,05-xťq) ; 0,025 -0,5 xťq = xťq ; xťq = 0,0167 ~0,017 mol.
|
Influence des conditions initiales :
L’hydrolyse d’un ester est une rťaction limitťe.
Lorsque l’ťtat d’ťquilibre est atteint ŗ 75 įC, la quantitť de matiŤre
d’ester non hydrolysťe est ťgale ŗ 3,3 10-2 mol.
Prťciser s’il
reste la mÍme quantitť de matiŤre d’ester ŗ l’ťquilibre dans les
conditions suivantes :
- les quantitťs initiales d’ester et d’eau sont identiques ŗ celles de la
question prťcťdente, la tempťrature est ťgale ŗ 95 įC.
La tempťrature est un facteur cinťtique ; l'ťquilibre est plus
rapidement atteint ŗ 95įC qu'ŗ 75 įC, mais la composition du systŤme
chimique ŗ l'ťquilibre n'est pas modifiťe.
- la quantitť de matiŤre initiale d’ester est identique, on introduit
dans le mťlange initial 100 mL d’eau, la tempťrature est ťgale ŗ 75įC.
L'eau est en large excŤs ; l'ťquilibre est dťplacť dans le sens de la
consommation d'eau, dans le sens direct : il se forme d'avantage
d'acide et d'alcool. La composition du mťlange ŗ l'ťquilibre est
modifiťe.
|
|