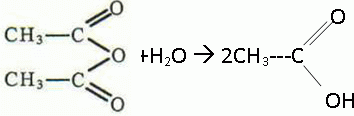|
L'aspirine
ne soigne pas que la douleur :
bac S Polynésie 09 /2010 |
|||||||
|
|||||||
|
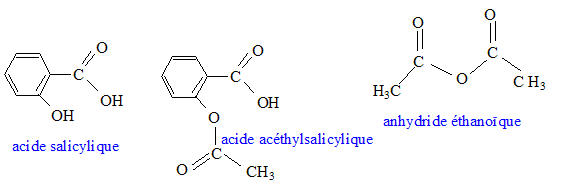
En 1829, le pharmacien français henry Leroux isole le principe actif de l'écorce de saule, la salicine. Il faudra encore prčs de trois quart de sičcle pour passer de la salicine ŕ l'acide acéthylsalicylique que la firme allemenande bayer commercialise finalement en 1899 sous le nom d'aspirine. Pendant plus de 100 ans, ce médicament a permis de soulager les douleurs et la fičvre. Récemment, de nouvelles indications thérapeuthiques sont apparues comme la prévention de certains cancers. Sa synthčse au laboratoire est relativement aisée. Données :
Masse volumique de l'anhydride éthanoďque r =1,08 g mL-1. pKa du couple acide acéthylsalicylique / ion acéthylsalicylate : 3,5 ŕ la température de l'expérience. L'acide salicylique et l'aspirine sont des solides peu solubles dans l'eau, solubles dans l'éthanol. l'anhydride éthanoďque est un liquide qui réagit vivement avec l'eau. Pictogrammes relevés sur le flacon d'anhydride éthanoďque : 
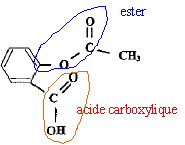
l'anhydride éthanoďque réagit vivement et totalement avec l'eau en donnant de l'acide éthanoďque. On peut obtenir l'aspirine ŕ partir d'anhydride éthanoďque et
d'acide salicylique ou d'acide éthanoďque et d'acide salicylique. 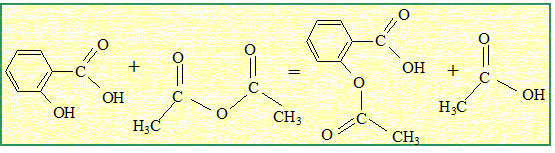 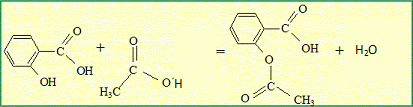 Quelle est la transformation qui permet d'atteindre l'avancement maximal ? Pourquoi ? La réaction entre l'acide salicylique et l'anhydride est totale. En absence d'eau, la réaction inverse, l'hydrolyse de l'ester ne se produit pas. L'avancement maximal est atteint. Quelles précautions doit-on prendre pour l'utilisation de l'un au moins des réactifs ? Pictogrammes relevés sur le flacon d'anhydride éthanoďque :  L'anhydride éthanoďque est corrosive : mettre des gants, des lunettes de protection et une blouse ; travailler sous hotte aspirante.
Choisir parmi les montages proposés celui qui convient pour cette synthčse. Indiquer le sens de circulation de l'eau de refroidissement dans le réfrigérant. 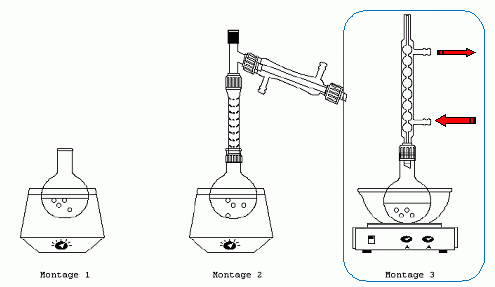 Pourquoi a-t-on choisi un ballon initialement bien sec ? L'anhydride éthanoďque réagit vivement avec l'eau en donnant de l'acide éthanoďque. Définir et calculer le rendement de la synthčse. Quantités de matičre initiales : acide salicylique n = m/M = 13,8 /138 = 0,10 mol ; anhydride éthanoďque : masse : 25*1,08 =27 g ; n' = 27/102 =0,265 mol L' Rendement : quantité de matičre réelle / quantité de matičre théorique *100 rendement : 0,050 / 0,10 *100 = 50 %.
|
|||||||
| |
|||||||
|
|