Dans cet exercice,
on s'interesse ŗ la mťcanique d'un feu d'artifice puis ŗ I'ťmission
lumineuse liťe ŗ I'ťlťment cuivre et ensuite au dosage de I'ťlťment
cuivre dans une piŤce de monnaie.
Mťcanique
du feu d'artifice.
La pyrotechnie, du grec ę pyros Ľ feu et ę teckhne Ľ savoir-faire, est
la technique des feux d'artifice.
Elle fut inventťe par les chinois, il y a plus de mi1le ans et
introduite en Occident gr‚ce ŗ Marco Polo au XIŤme siŤcle.
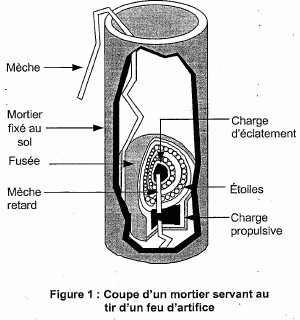
La fusťe pyrotechnique sphťrique est, sans con teste, Ie projectile Ie
plus employť
par les techniciens lors des feux d'artifices modernes. Elle est tirťe
depuis un mortier fixe au sol et est expulsťe ŗ grande vitesse par les
gaz produits par I'explosion de la charge propulsive.
A I'apogťe, une charge d'ťclatement provoque I'explosion de la fusťe et
disperse les garnitures pyrotechniques qu'on appelle ę ťtoiles Ľ.
L'etude des mouvements des centres d'inertie des diffťrents projectiles
est rťalisťe dans Ie rťfťrentiel terrestre supposť galilťen.
Etude thťorique
de la phase ascensionnelle de la fusťe pyrotechnique.
Une fusťe pyrotechnique de masse M= 400 g est tirťe verticalement avec
une vitesse initiale de valeur v0 = 50, 0 m/s.
On ťtudie Ie mouvement de son centre d'inertie G dans un repŤre
vertical (0, J ) orientť vers le haut.
On choisit l'instant t0 = 0 s lorsque Ie centre d'inertie G
est confondu avec I'origine du repŤre O.
On nťglige Ie mouvement de rotation de la fusťe pyrotechnique sur
elle-mÍme ainsi que les actions mťcaniques liťes ŗ I'air (poussťe
d'ArchimŤde et force de frottements). Lors du tir, la vitesse du vent
est considťrťe comme ťtant nulle et on admet que la fusťe pyrotechnique
ne subit pas de perte de∑ masse lors de son mouvement ascendant.
Un logiciel de simulation permet d'obtenir Ie
graphe de I'ťvolution temporelle de I'ťnergie cinťtique Ec, de I'ťnergie potentielle de pesanteur Ep et de
I'ťnergie mťcanique totale Em de la fusťe lors de son
mouvement ascendant. On prend I'origine de l'ťnergie potentielle de
pesanteur au point O.
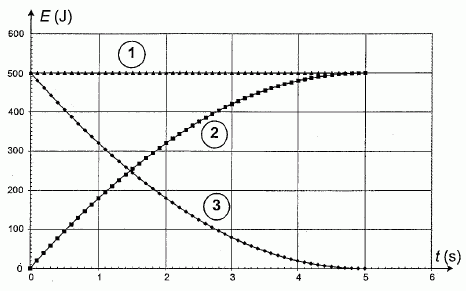
Identifier chacune
des courbes.
Courbe 1 : l'ťnergie mťcanique est la somme de l'ťnergie
potentielle et de l'ťnergie cinťtique.
Courbe 2 : l'ťnergie potentielle initiale est nulle, puis est croissante
Courbe 3 : la vitesse, donc l'ťnergie cinťtique initiale est maximale,
puis dťcroÓt.
En
s'aidant du graphique, dťterminer l'instant tA auquel la fusťe
pyrotechnique atteint son altitude maximale YA (apogťe). Justifier.
A l'apogťe, l'ťnergie potentielle est maximale, ťgale ŗ l'ťnergie
mťcanique, tandis que la vitesse, donc l'ťnergie cinťtique est nulle.
On lit tA ~ 4,8 s.
Donner
l'expression de l'ťnergie mťcanique aux instants t0 et tA.
Initialement l'ťnergie mťcanique est sous forme cinťtique : Em(0)
= Ĺmv02.
A l'apogťe l'ťnergie mťcanique est sous forme potentielle de pesanteur
: Em(tA) = mg YA.
En
dťduire que l'expression de la coordonnťe YA de l'apogťe
atteinte par la fusťe pyrotechnique s'exprime par la relation ci-dessous
:
YA =v02/(2g)
"On nťglige "
les actions mťcaniques liťes ŗ I'air (poussťe d'ArchimŤde et force de
frottements)".
l'ťnergie mťcanique se conserve : Em(0) =Em(tA)
Ĺmv02=mg YA ; Ĺv02=g
YA ; YA =v02/(2g).
Calculer
la valeur de l'altitude de l'apogťe sachant que l'accťlťration de la
pesanteur vaut g = 9,8 m.s -2.
YA =502/(2*9,8)=127,6 m ~1,3 102 m.
En rťalitť I'apogťe vaut 122 m, interprťter le fait
que cette valeur est diffťrente de celle calculťe.
Dans la rťalitť , il faut prendre en compte les actions
mťcaniques liťes ŗ I'air (poussťe d'ArchimŤde et force de
frottements) ainsi que la rotation de la fusťe.
Dispersion des
ę ťtoiles Ľ.
Dans Ie repŤre (0, i, j) de la figure, on ťtudie le mouvement d'une ę
ťtoileĽ produite lors de l'explosion de la fusťe ŗ l'apogťe de sa
trajectoire. Cette ę ťtoileĽ est projetťe ŗ partir du point A ŗ
une altitude YA = 122 m. Le vecteur vitesse initiale VA
appartenant au plan xOy, inclinť d'un angle a par rapport a l'horizontale a pour valeur VA=
54,0 m.s-1. On nťglige les actions mťcaniques liťes ŗ
l'air (forces de frottements et poussťe d'ArchimŤde) et on prend comme
nouvelle origine des temps l'instant oý l' ę ťtoileĽ est produite en A.
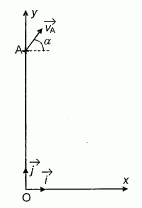
Dans le repŤre (0, i ,j ), en appliquant la seconde loi de Newton,
ťtablir l'expression des composantes vx(t) et vy(t)
du vecteur vitesse du centre d'inertie d'une ę ťtoileĽ de masse m.
L'ťtoile n'est soumise qu'ŗ son poids ; la seconde loi de Newton donne
les composantes de l'accťlťration dans le repŤre : ( 0 ; -g )
Le vecteur vitesse est une
primitive du vecteur accťlťration et les composantes de la vitesse
initiale sont : (v0 cos a
; v0 sin a ).
Par suite : vx(t) = v0 cos a et vy(t) = -gt +v0 sin a .
Les courbes ci-dessous, reprťsentent l'ťvolution temporelle des
composantes du vecteur vitesse.
Identifier, en justifiant, chacune de ces courbes.
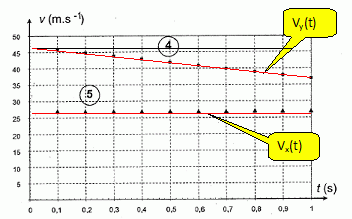
vx(t)
est une fonction constante positive : le graphe est une droite
horizontale.
vy(t)
est une fonction afine dťcroissante de coefficient directeur -9,8 ms-2.
En 1 s vy dťcroÓt d'environ 10 m/s.
Montrer que
l'ťquation de la trajectoire de l'ťtoile est : y =-Ĺg
x2 / ( vA cos a
)2 + x tan a + OA.
De quel
type de trajectoire s'agit-il ?
Le vecteur position est une
primitive du vecteur vitesse ; les
composantes du vecteur position initiale sont : (0 ; OA )
Les composantes du vecteur position sont donc : x(t) = vA
cos a t ; z(t) =-Ĺgt2
+ vA sin a t + OA.
x(t) = vA cos a
t donne t = x(t) / ( vA cos a )
repport dans y(t) : y =-Ĺg x2 / ( vA cos a )2 +x tan a + OA.
Il s'agit d'une branche de parabole.
|
Emission
lumineuse.
Les ę ťtoilesĽ en combustion produisent une f1amme colorťe dont la
couleur dťpend de leur composition chimique. La couleur bleue obtenue
est due a la dťsexcitation des molťcules de chlorure de cuivre (I) CuCl.
Le spectre d'ťmission de la molťcule CuCl excitťe est composť de
plusieurs bandes centrťes autour des longueurs d'onde suivantes dans le
vide: 395 nm ; 433 nm ; 435 nm ; 484 nm ; 488 nm ; 525 nm.
Donnees :
constante de Planck: h = 6,6 x 10-34 J.s
cťlťritť de la lumiŤre dans Ie vide: c = 3,0 x 108 m.s-1.
1 eV= 1,6 x 10-19 J
Le
spectre d'ťmission de la molťcule CuCl appartient-il au domaine du
rayonnement visible, ultraviolet ou infrarouge ?
395
nm : domaine UV ; 433 nm ;
435 nm ; 484 nm ; 488 nm ; 525 nm : domaine visible
A quelle valeur de
la frťquence v correspond la
longueur d'onde 435 nm dans Ie vide ?
n = c / l = 3,0 x 108
/435 10-9 =6,9 1014 Hz.
Calculer I'energie
du photon correspondant en eV.
E = h n = 6,6 x 10-34
*6,9 1014
=4,55 10-19 J.
puis diviser par 1,6 x 10-19
: E = 2,8 eV.
L'ťlťment
cuivre dans les piŤces de monnaie.
On se propose dans cette partie de vťrifier expťrimentalement, par
spectrophotomťtrie, le pourcentage massique en cuivre dans un
ťchantiflon servant ŗ fabriquer une piŤce de 10 centimes d'euro.
Donnťes:
Couples d'oxydorťduction Cu2+(aq) / Cu(s) ; N03-
(aq) / NO(g)
Masse molaire atomique: M(Cu) = 63,5 g.mol-1.
Masse molaire du sulfate de cuivre pentahydratť: M(CuS04, 5 H20)
= 249,6 g/mol
Le monoxyde d'azote NO(g) s'oxyde au contact du dioxygŤne de l'air en
dioxyde d'azote N02 (g), gaz roux et toxique, selon
l'ťquation chimique:
2 NO (g) + O2 (g) = 2 N02 (g)
Attaque du cuivre contenu dans la
piŤce par une solution d'acide nitrique.
L'acide
nitrique (H30+ + N03- (aq)) est un oxydant puissant
capable d'oxyder des mťtaux tels que le cuivre Cu. Sous une hotte, dans un
becher, on place l'ťchantillon et on ajoute de l'acide nitrique
concentrť en excŤs.
On observe au cours de cette transformation totale l'apparition d'une
teinte bleue foncťe dans
la solution revelant la prťsence d'ion cuivre (II) Cu2+
et un
dťgagement gazeux qui devient roux au contact de I'air.
Ecrire
les demi-ťquations d'oxydorťduction associťes ŗ chaque couple mis en
jeu lors de cette transformation
chimique.
oxydation : Cu(s) = Cu2+(aq) +2e-.
rťduction : N03-
(aq) + 4H+ aq + 3e-= NO(g) + 2H2O(l).
|
Dosage
spectrophotomťtrique des ions cuivre (II) prťsents dans la solution S.
Une fois le dťgagement gazeux achevť, on verse le contenu du becher
dans une fiole jaugťe de 1,0 L et on complŤte jusqu'au trait de jauge
avec de l'eau distillťe en homogťnťisant le mťlange afin de rťaliser la
solution S.
Afin de rťaliser une ťchelle de teintes, on prťpare un volume Va
= 100 mL d'une solution ę mŤreĽ S0 de sulfate de cuivre de
concentration molaire C0= 0,10 mol/L
Calculer
la masse de sulfate de cuivre pentahydratť ŗ peser pour prťparer cette
solution par dissolution.
Quantitť de matiŤre (mol) = volume de la solution ( L) * concentration
( mol/L)
n = Va C0 = 0,10*0,10 = 1,0 10-2
mol.
masse (g) = masse molaire (g/mol) * quantitť de matiŤre (mol)
m = 249,6 *0,01 = 2,496 g ~ 2,5 g.
La solution S0 permet de prťparer par dilution une ťchelle
de teintes constituťe des cinq solutions ę fille Ľ de volume V = 25,0
mL chacune. On mesure I'absorbance A ŗ la longueur d'onde l= 810 nm.
A cette longueur d'onde seul l'ion Cu2+ (aq) est responsable
du phťnomŤne d'absorption lumineuse.
solution
|
S0
|
S1 |
S2 |
S3 |
S4 |
concentration
(mol/L)
|
0,10
|
0,080
|
0,060
|
0,040
|
0,02
|
A
|
1,26
|
1,02
|
0,76
|
0,52
|
0,24
|
Calculer
le volume, notť VmŤre, de solution ę
mŤreĽ S0 ŗ prťlever pour
prťparer la solution " fille " S3. Justifier.
facteur de dilution : F = 0,10 / 0,04 = 2,5.
VmŤre =Vfille / F = V/F = 25 / 2,5 = 10 mL.
A I'aide
du spectre d'absorption d'une solution de sulfate de cuivre reprťsentť
justifier le choix de la longueur d'onde retenue pour cette ťtude
expťrimentale.
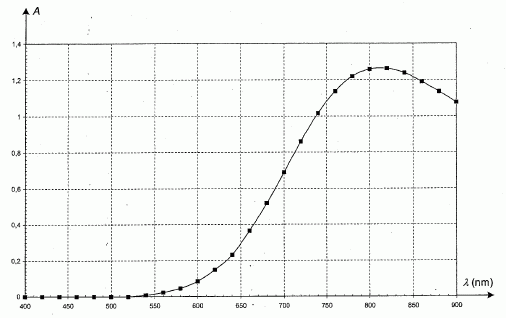
Afin d'obtenir la meilleur sensibilitť, on choisit la longueur d'onde
correspondant au maximum d'absorption.
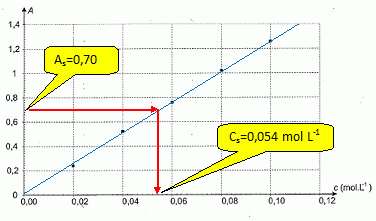
L'absorbance d'un ťchantillon de la solution S, mesurťe dans les
mÍmes conditions que prťcťdemment ŗ la longueur d'onde l= 810 nm, vaut As =
0,70. Le graphe donnant l'ťvolution de l'absorbance A en fonction de la
concentration c en solutť apportť des diffťrentes solutions ę fille Ľ
est reprťsentťe.
En
dťduire la concentration molaire volumique Cs de la solution S,
en justifiant graphiquement.
Pourcentage
massique de cuivre dans la piŤce.
Toutes les piŤces d'euros contiennent du cuivre mťtallique dans des
proportions particuliŤres. Ainsi, les piŤces de 10, 20 et 50 centimes
sont formťes d'un alliage appelť ę or nordiqueĽ dont la composition
massique est la suivante : 89 % de cuivre, 5% d'aluminium, 5% de zinc,
1 % d'ťtain.
En
utilisant Ie rťsultat de la question prťcťdente, calculer la valeur de
la masse m(Cu) de cuivre contenue dans l'ťchantillon ťtudiť prťcťdemment.
1 L de la solution contient 0,054 mol d'ion cuivre II issu de n =0,054
mol de cuivre mťtal.
m(Cu) = n M(Cu) = 0,054*63,5 =3,43 g ~3,4 g.
Sachant que la masse de l'ťchantillon est m = 4,1 g, en dťduire le
pourcentage massique du cuivre dans l'ťchantillon.
3,43 / 4,1 *100 = 83,6 ~84 %.
Comparer
ce rťsultat ŗ la valeur fournie dans l'ťnoncť en calculant l'ťcart
relatif.
diffťrence des valeurs / valeur moyenne * 100 = (89-83,6)*100 / 86,3 ~6,2 %.
|