|
Nucléaire
au service de la médecine : bac S France 2010 |
|||||||
|
|||||||
|
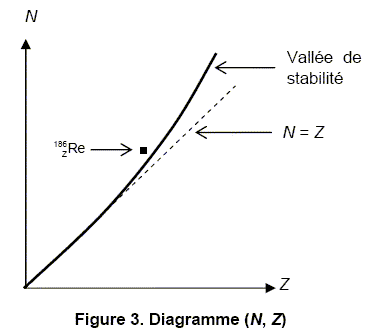
découverte et ŕ la maîtrise de nouveaux isotopes. La radiothérapie vise ŕ administrer un radiopharmaceutique dont les rayonnements ionisants sont destinés ŕ traiter un organe cible dans un but curatif ou palliatif. Ainsi on utilise du rhénium 186 dans le but de soulager la maladie rhumatoďde et du phosphore 32 pour réduire la production excessive de globules rouges dans la moelle osseuse. D’aprčs le site : http://www.asn.fr La premičre partie de cet exercice traite de l’utilisation du rhénium 186 et la seconde partie de l’utilisation du phosphore 32. On s’intéresse ŕ l'aspect physique des phénomčnes, les aspects biologiques ne sont pas pris en compte. Données : - temps de demi-vie du rhénium 186 : t˝( 186ZRe) = 3,7 j (jours) ; constantes radioactives : λ( 186ZRe) = 2,2 × 10−6 s− 1 ; λ( 3215P) = 5,6 × 10−7 s− 1 ; - masse molaire du rhénium 186 : M( 186ZRe) =186 g/mol ; - masses de quelques noyaux et particules : m( 3215P) = 5,30803 × 10−26 kg ; m( 3216S ) = 5,30763 × 10−26 kg ; m( 0-1e ) = 9,1 × 10−31 kg ; - célérité de la lumičre dans le vide : c = 3,0 × 108 m.s− 1 ; - constante d'Avogadro : NA = 6,0 × 1023 mol− 1 ; électron-volt : 1 eV = 1,6 × 10−19 J . Le rhénium 186 ( 186ZRe ) est un noyau radioactif β−. Sur le diagramme (N, Z) de la figure 3 ci-dessous oů N représente le nombre de neutrons et Z le nombre de protons, la courbe tracée permet de situer la vallée de stabilité des isotopes. Le point représentatif du noyau de rhénium 186 est placé au-dessus de cette courbe. Déduire de ce diagramme si cet isotope radioactif possčde un excčs de neutron(s) ou un excčs de proton(s) par rapport ŕ un isotope stable du męme élément. Le rhénium 186 est situé ŕ gauche de la vallée de la stabilité : il possčde un excčs de neutrons par rapport ŕ un isotope stable du męme élément. Quel nom porte la particule émise au cours d’une désintégration β− ? Electron.
Écrire l’équation de
la désintégration du noyau de rhénium 186 noté ( 186ZRe) sachant que le noyau fils obtenu correspond ŕ un isotope de l'osmium noté ( A76Os ). En énonçant les lois utilisées,
Injection intraveineuse d'une solution contenant du phosphore 32. Donner la composition du noyau de phosphore 32. 15 protons et 32-15 = 17 neutrons. Ŕ l’aide des masses données en début d’exercice et de la carte d’identité du phosphore 32, vérifier par un calcul la valeur E de l'énergie du rayonnement émis par la désintégration du phosphore 32. Défaut de masse : Dm = m( 3216S ) +m( 0-1e ) -m( 3215P) = 5,30763 × 10−26 +9,1 × 10−31 - 5,30803 × 10−26 = -3,09 10-30 kg. E = |Dm|c2 =3,09 10-30 * (3,0 × 108)2 = 2,78 10-13 J 2,78 10-13 / 1,6 × 10−19 =1,7 106 eV = 1,7 meV. Pour la trčs grande majorité d’entre eux, les noyaux fils obtenus lors de cette transformation ne sont pas dans un état excité. Ŕ quel type de rayonnement particuličrement pénétrant le patient n'est-il pas exposé ? Un noyau excité libčre son surplus d'énergie en émettant des photons g.
|
|||||||
| |
|||||||
|
|