Autoprotolyse
de l'eau.
L'ťquation de la rťaction d'autoprotolyse de l'eau est :
A. H3O+
+HO- = 2H2O. Faux.
Rťaction entre un acide fort et
une base forte.
B. H2O +H2O =H3O+
+HO-. Vrai.
C. 2H2O + 2e-
= H2 + 2HO-. Faux.
La prťsence d'ťlectrons indique
une rťaction d'oxydorťduction.
La
constante d'ťquilibre associťe ŗ l'ťquation de la rťaction
d'autoprotolyse de l'eau est appelťe :
A. Le produit de
solubilitť de l'eau. Faux.
B. Le quotient de rťaction de l'eau. Faux.
C. Le produit ionique de
l'eau. Vrai.
|
On peut ťgalement
interprťter cette constante d'ťquilibre comme :
A. La constante d'aciditť du couple H2O
/ HO-. Vrai.
H2O
+H2O =H3O+ +HO-. KE
= [H3O+]ťq [HO-]ťq.
B. La constante
d'aciditť du couple H3O+
/ H2O.
Faux.
C. La
constante d'aciditť du couple H3O+
/ HO-. Faux.
|
On met en
prťsence 0,6 mole d'acide carboxylique et 0,6 mole d'alcool, puis, sans
intervenir d'aucune faÁon, on laisse le mťlange ťvoluer ŗ tempťrature T
constante. le suivi cinťtique de la transformation qui se dťroule
a permis de tracer les courbes 1 et 2, reprťsentant l'ťvolution de
l'avancement en fonction du temps.
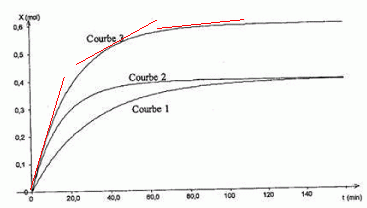
La vitesse volumique de la rťaction :
A. est nulle ŗ
l'instant t=0 s. Faux
La vitesse est proportionnelle au
coefficient directeur de la tangente ŗ la courbe ŗ la date
considťrťe. A t = 0 la tangente n'est pas horizontale..
B.
est
maximale ŗ l'instant t=0 s.
Vrai.
La tangente ŗ t = 0 possŤde le plus grand
coefficient directeur.
C.
s'exprime en mol min-1. Faux.
en
mol L-1 min-1.
La courbe 3 :
A. peut Ítre obtenue en rťalisant la transformation
ŗ une tempťrature T3 supťrieure ŗ T2. Faux
L'avancement final xf
est ťgal ŗ xmax =0,6 mol, ce qui indique une
rťaction totale. Or
l'estťrification peut Ítre rendue totale en utilisant un rťactif
en large excŤs ou en ťliminant l'un des produits au fur et ŗ mesure de
sa formation.
B.
peut Ítre obtenue en rťalisant la transformation
ŗ une tempťrature T3 supťrieure ŗ T2 et en prťsence d'un
catalyseur.
Faux.
C. ne peut pas Ítre
obtenue dans les conditions dťcrites. Vrai.
L'ester obtenu a pour formule semi-dťveloppťe :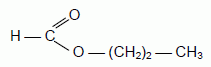 . Son nom est :
. Son nom est :
A.
le propanoate de mťthyle. Faux
L'acide carboxylique de dťpart ne
contient qu'un seul carbone donc mťthanoate et l'alcool de dťpart compte 3 atomes de
carbone donc propyle.
B.
le mťthanoate de propanyle.
Faux.
C. le mťthanoate de propyle.
Vrai.
A une transformation
chimique est associťe la rťaction d'ťquation 2A + B = 2 C + 3D oý les
espŤces A, B, C et D n'ont pas besaoin d'Ítre prťcisťes. Les mesures
ont permis d'ťtablir le tableau d'avancement suivant :
|
avancement
|
2A
|
+B
|
=2C
|
+3D
|
ťtat
initial
|
0
|
0,40
|
0,30
|
0
|
0
|
ťtat
final
|
xfinal
|
0,30
|
0,25
|
0,10
|
0,15
|
Le taux d'avancement final est :
A.
t = 0,25. Vrai.
t =xfinal / xmax
avec xfinal = 0,10/2 = 0,05 mol.
Si
A est en dťfaut : 0,40-2xmax = 0 ; xmax = 0,20 ;
si B est en dťfaut : 0,30-xmax = 0 soit xmax
=0,30 ( retenir laplus petite valeur )
t =0,05 / 0,20 = 0,25.
B. t = 0,50. Faux.
C. t = 0,75. Faux.
Dans
les conditions de l'expťrience, la constante d'ťquilibre K associťe ŗ
cette ťquation est K = 108. Cette valeur :
A.
dťpend de la composition initiale du systŤme. Faux.
La constante d'ťquilibre ne dťpend que de
la tempťrature.
B. dťpend de la
composition initiale du systŤme et de la tempťrature. Faux .
C. dťpend de la tempťrature. Vrai.
Le
taux d'avancement final de la transformation :
A.
dťpend de la composition initiale du systŤme et de la constante
d'ťquilibre. Vrai.
L'avancement
final dťpend de K et de la composition initiale du systŤme.
B. ne dťpend que de la
composition initiale du systŤme. Faux .
C. ne dťpend que de la constante
d'ťquilibre K. Faux .
On considŤre un acide notť AH. Lors de la
prťparation d'une solution aqueuse, la transformation de cet acide avex
l'eau eqt quasi-totale. On titre cette solution par une solution
aqueuse d'hydroxyde de sodium de concentration molaire en solutť
apportť connue.
l'ťquation de la rťaction de titrage est :
A.
AH + HO-
= H2O + A-. Faux.
Les couples acide
/ base sont : AH / A- et H3O+
/ H2O
( acide fort, entiŤrement dissociť dans l'eau ).
H3O+ + HO- = 2H2O.
B. H3O+
+ HO-
= 2H2O. Vrai .
C. H3O+
+ A-
= AH +H2O. Faux
Le
suivi pH-mťtrique de ce titrage a permis d'obtenir la courbe ci dessous
:
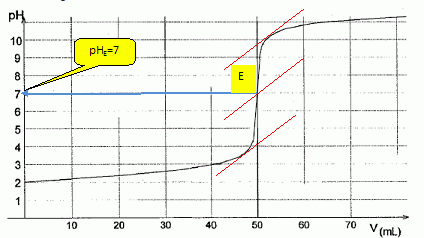
Pour rťaliser le suivi colorimťtrique de ce titrage :
A. seul
le bleu de bromothymol convient. Vrai.
La zone de irage
de l'indicateur colorť doit contenir le pH du point ťquivalent, 7 dans
ce cas.
B. Le
bleu de bromothymol et le rouge de crťsol conviennent. Faux.
C. Le
bleu de bromothymol, le rouge de crťsol et le bleu de bromophťnol conviennent. Faux.
indicateur
colorť
|
teinte
acide
|
zone
de virage
|
teinte
basique
|
bleu
de bromophťnol
|
jaune
|
3,0 -
4,6
|
bleu
|
bleu
de bromothymol
|
jaune
|
6,0 -
7,6
|
bleu
|
rouge
de crťsol
|
jaune
|
7,2 -
8,8
|
rouge
|
|
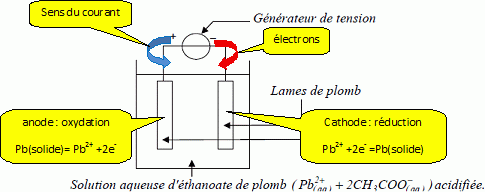
On rťalise le
montage suivant :
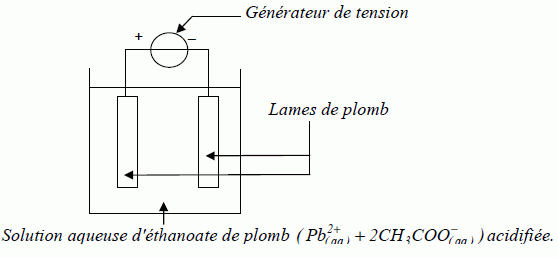
Seul le couple Pb2+/ Pb intervient.
Ce montage permet de rťaliser :
A- une pile. Faux.
B- une ťlectrolyse.
Vrai.
Le gťnťrateur impose le
sens du courant donc le sens de la transformation chimique.
C- une
trnasformation spontanťe. Faux.
Une ťlectrolyse est une
transformation forcťe qui nťcessite un apport d'ťnergie ťlectrique.
Au bout de quelques minutes on observe :
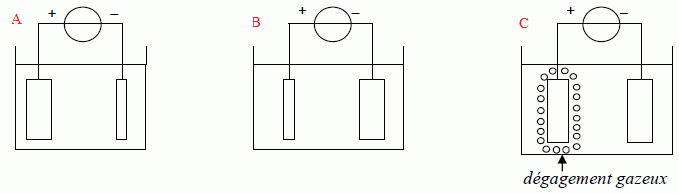
B est vrai
: seul
le couple Pb2+/ Pb intervient.
L'anode s'oxyde, diminue de volume et un dťpŰt de plomb se forme ŗ la cathode.
On considŤre une solution aqueuse S1 de nitrate de plomb
(II) ( Pb2+aq + 2NO3-aq ) telle que : [Pb2+aq] = 1,0 10-3
mol/L et une solution aqueuse de chlorure de fer (II) ( Fe2+aq + 2Cl-aq )
telle que : [Fe2+aq]
= 4,0 10-2 mol/L. La constante d'ťquilibre K associťe ŗ la
rťaction d'ťquation : Pb2+aq +Fe(s) = Pb(s) + Fe2+aq vaut 3,0 1010.
Une pile est constituťe des deux demi-piles suivantes, reliťes par un
pont salin :
- une lame de plomb plongeant dans la solution S1
- une lame de fer plongeant dans la solutuion S2.
On la branche aux bornes d'un conducteur ohmique de rťsistance R = 100
ohms.
AprŤs une durťe de fonctionnement de 30 minutes :
A.
La masse de la lame de fer a augmentť. Faux.
Qr i
= [Fe2+aq]i / [Pb2+aq]i = 4,0 10-2 /1,0 10-3
=40, valeur infťrieure ŗ K : ťvolution dans le sens direct.
Le fer
s'oxyde en ion Fe2+aq : la masse de la lame de fer diminue.
B.
La masse de la
lame de fer a diminuť. Vrai.
C.
la valeur de la
rťsistance R n'a aucune influence sur la variation de masse des lames.
Faux.
Si R augmente l'intensitť
du courant diminue ; or la variation de la masse des lames est
proportionnelle ŗ l'intensitť.
Dans un becher on plonge
une lame de plomb dans un mťlange de 20 mL de la solution S1
et de 20 mL de la solution S2.
A- le systŤme
n'ťvoluera pas. Vrai.
Le fer est absent
: Pb(s) + Fe2+aq = Pb2+aq +Fe(s) avec K' =
1/ 3,0 1010 = 3,3
10-11.
Qr
i = [Pb2+aq]i / [Fe2+aq]i = 1,0 10-3
/ 4,0
10-2 =0,025,
valeur supťrieure ŗ K' : ťvolution dans le sens inverse.
Le critŤre d'ťvolution
spontanť prťvoit une ťvolution dans le sens inverse, ce qui est
impossible du fait de l'absence de fer.
B- on observe un dťpŰt de fer sur la
lame de plomb. Faux.
C- la masse de la lame de plomb va
augmenter. Faux.
|
|
|
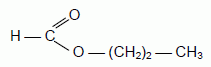 . Son nom est :
. Son nom est :



