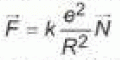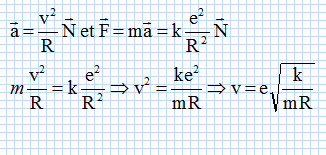|
On se
propose d'ťtudier
le modŤle de l'atome d'hydrogŤne proposť par Niels Bohr en 1913. Ce
modŤle est une continuitť du modŤle planťtaire proposť par Ernest
Rutherford, avec cette diffťrence essentielle que Niels Bohr introduit
un nouveau concept, ŗ savoir la quantification des niveaux d'ťnergie
dans l'atome.
Mouvement
de l'ťlectron dans l'atome.
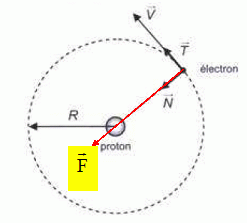
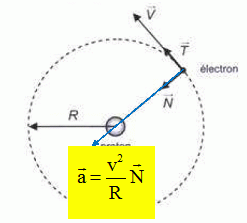
POur commencer cette ťtude, on suppose que l'ťlectron est animť
d'un mouvement circulaire uniforme de rayon R autour du proton. Les
caractťristiques du mouvement de l'ťlectron sont exprimťes dans la base
mobile de vecteurs unitaires N et T comme indiquť sur le schťma :
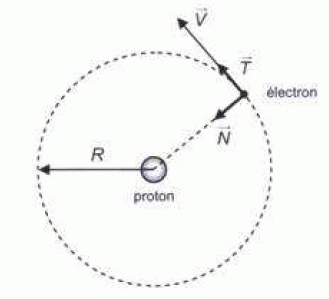
L'ťlectron
est soumis ŗ une force d'interaction ťlectrostatique centripŤte.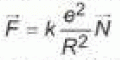
R
: rayon de l'atome ; e valeur de la charge ťlťmentaire et k une
constante.
Reprťsenter sur un
schťma cette force d'interaction.
Dťterminer l'unitť
de la constante k. ( e s'exprime en coulomb C).
k = F R2 /
e2 ; [k] = N m2 C-2.
Dans le
cas d'un mouvement circulaire uniforme, ťcrire l'expression du vecteur
accťlťration.
En appliquant une
loi dont on donnera le nom, montrer que la valeur de la vitesse V est :
V = e [k/(mR)]Ĺ.
Ecrire la
seconde loi de Newton suivant l'axe N.
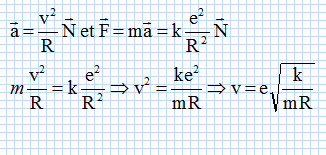
Calculer cette
vitesse.
m = 9,109 10-31 kg ; e = 1,602 10-19 C ; R = 5,3
10-11 m ; k = 9,0 109 SI.
v = 1,602 10-19 [9,0 109 / ( 9,109 10-31*5,3
10-11 )]Ĺ =2,2 106 m/s.
Donner
l'expression de l'ťnergie cinťtique puis la calculer en J et eV.
Ec =Ĺmv2 =Ĺke2/R =0,5 *9,0 109
*(1,6 10-19)2 / 5,3 10-11
=2,174 10-18 ~2,2
10-18 J.
2,174 10-18 / 1,6 10-19 = 13,6 ~14 eV.
La
quantification de Bohr.
Dans
le modŤle de Bohr, l'ťnergie de l'atome est quantifiťe.
Expliquer
ce qu signifie l'adjectif " quantifiť".
Seules un petit nombre de valeurs sont possibles pour l'ťnergie de
l'atome.
Dans la mťcanique de Newton, ŗ l'ťchelle humaine, toutes les valeurs
sont possibles pour l'ťnergie.
L'ťnergie de l'atome d'hydrogŤne se met sous la forme : En =
-13,6 / n2 ( eV).
n est un nombre entier strictement positif appelť nombre quantique
principal.
A chacune de ces ťnergies est associťe une orbite circulaire de
l'ťlectron dont le rayon rn vťrifie : rn = a0n2.
a0 est une grandeur appelťe " rayon de Bohr", valeur du
rayon de l'atome pour la plus petite valeur de n, ŗ savoir n=1.
Complťter
le tableau suivant :
n
|
1
|
2
|
3
|
4
|
5
|
En
( eV)
|
-13,6
|
-3,40
|
-1,51
|
-13,6
/ 16 = -0,850
|
-13,6
/ 25 = -0,544 |
rn
|
a0
|
4a0 |
9a0 |
16a0 |
25a0 |
Vers
quelle valeur ťvolue l'ťnergie En de l'atome lorque
la valeur de n devient trŤs grande ? MÍme question pour rn.
En tend vers zťro et rn tend vers l'infini.
|
l'image
que l'on peut donner de l'ťlectron en interaction avec le proton de
l'atome d'hydrogŤne est celle d'un puits dans lequel l'ťlectron serait
"piťgť".

Quelle
ťnergie minimale faut-il fournir ŗ l'atome pour libťrer l'ťlectron de
ce puits ?
13,6 eV.
Quelle modification
subit l'atome d'hydrogŤne si l'ťlectron est libťrť de ce puits ?
L'atome perd son unique ťlectron ;
l'atome est ionisť.
On apporte ŗ l'atome, dans son ťtat de plus basse ťnergie, une ťnergie DE = 10,2 eV.
Dans
quel ťtat ťnergťtique se retrouve alors l'atome aprŤs avoir reÁu cette
ťnergie ?
L'atome gagne de l'ťnergie et se retrouve dans un ťtat dit "excitť".
dans ce nouvel ťtat, l'atome est instable et va chercher ŗ retrouver
son ťtťt de plus basse ťnergie. Ce phťnomŤne s'accompagne de l'ťmission
d'un photon.
Dťterminer
sa frťquence puis sa longueur d'onde dans le vide.
E =10,2 *1,6 10-19 =
1,632 10-18 J.
E = h n ; frťquence n = E/ h = 1,632 10-18 / 6,62 10-34
=2,47 1015 Hz.
longueur d'onde l = hc /E
= 6,62 10-34 *
3,00 108 / 1,632 10-18
=1,22 10-7 m = 122
nm.
A
quel domaine spectrale appartient la radiation ťmise ?
122 nm est infťrieure ŗ 400 nm, limite entre le visible et le domaine
UV.
122 nm appartient au domaine UV.
|
|